Файл: Рр 2 Кинетика простых реакций Учебное задание 5 Расчет константы скорости реакции второго порядка.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 11.01.2024
Просмотров: 16
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
РР 2 «Кинетика простых реакций»
Учебное задание 5: «Расчет константы скорости реакции второго порядка»
Вариант 1
Кинетика гомогенной реакции A + B = C описывается кинетическим уравнением второго порядка. Известна константа скорости и начальные концентрации исходных веществ: k = 0,00238 м3 моль-1 мин-1; сA,0 = 25 моль/м3; сB,0 = 50 моль/м3.
Необходимо:
1) выразить зависимость концентрации реагирующих веществ и продуктов реакции от времени;
2) рассчитать текущие концентрации реагирующих веществ и продукта реакции;
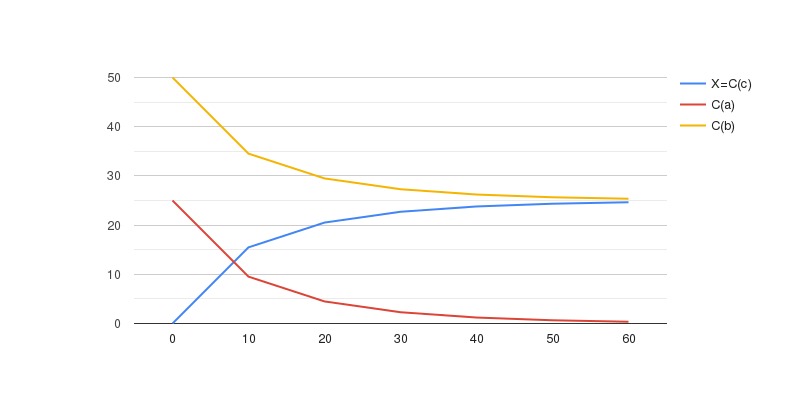
3) построить кинетические кривые всех участников реакции в интервале времени от 0 до 60 мин с шагом 10 мин.
Дано:
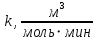 | 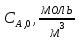 | 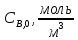 |
| 0,00238 | 25 | 50 |
Решение:
1) Для реакции второго порядка при неравенстве концентраций исходных веществ плотность глубины реакции (х) рассчитывается по уравнению:
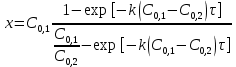
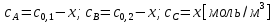
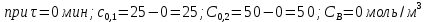
Рассчитаем плотность глубины реакции ко времени 10 мин.
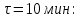
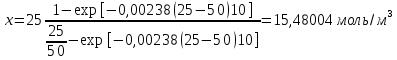
Тогда
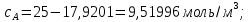
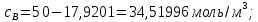
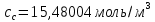
-
Сведем данные в таблицу
| τ, мин | x = 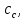 моль/м3 моль/м3 | CA, моль/м3 | CB, моль/м3 |
| 0 | 0 | 25 | 50 |
| 10 | 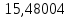 | 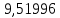 | 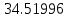 |
| 20 | 20,51502 | 4,48498 | 29,48498 |
| 30 | 22,71045 | 2,28955 | 27,28955 |
| 40 | 23,78699 | 1,21301 | 26,21301 |
| 50 | 24,34519 | 0,65481 | 25,65481 |
| 60 | 24,64303 | 0,35697 | 25,35697 |
-
Построим по данным таблицы кинетические кривые