Файл: Расчет ректификационной колонны по дисциплине Процессы и аппараты химической технологии.docx
Добавлен: 11.01.2024
Просмотров: 203
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
2.2 Построение х-у диаграммы, кривых изобар пара и жидкости
2.4 Расчет однократного испарения бинарной смеси
2.5 Расчет материального баланса ректификационной колонны
2.7 Расчет числа тарелок на комбинированной и x-y-диаграмме
2.8 Расчет профиля концентраций и нагрузок по высоте колонны
2.9 Расчет фактического числа тарелок
2.10 Расчет диаметра ректификационной колонны
2.11 Расчет высоты ректификационной колонны
По полученным данным строим ????′−????′ диаграмму и ????−????′,????′ диаграмму.
Рисунок 3 – ????−????′,????′ диаграмма (изобара)
2.4 Расчет однократного испарения бинарной смеси
2.4.1 Расчет x*F и y*F
Материальный баланс процесса однократного испарения может быть представлен уравнениями:
Общее: F = GF + gF (15)
Для НКК:
F · x'F = GF · y*F + gF · x*F, (16)
где GF и gF – мольные расходы пара и жидкости;
x*F и y*F – мольные доли НКК в равновесных жидкой и паровой фазах, полученных в результате однократного испарения сырья на входе в колонну.
Отношение массы образовавшихся паров G к массе исходной смеси F называется массовой долей отгона и обозначается через е. Отношение G' к F' есть мольная доля отгона, обозначаемая через е'.
Процесс однократного испарения проанализируем при помощи х-у диаграммы и изобары.
Найдем точки А и N на x-y диаграмме с помощью уравнения:
x'F = e' · y*F + (1 – e') · x*F, (17)
Если в уравнении (17)
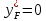 , то:
, то: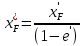 (18)
(18)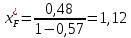
Отложим на x'-у'-диаграмме точку А (1,12; 0)
Если в уравнении
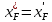 , то
, то 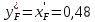 .
.Отложим на x'-у'-диаграмме точку N (0,48; 0,48)
Соединив точки А и N (рис.6), получим линию однократного испарения – ANF. По координатам точки F определим мольные доли низкокипящего компонента в жидкости и в паре, полученные в результате ОИ:
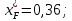
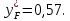
Рисунок 5 – х'-y'- диаграмма
2.4.2. Расчет равновесной температуры
Температура находится по изобаре из t-x-y диаграммы (рис.3). Для этого в данной диаграмме находим точки и xF* (0,36) и yF* (0,57) и проводим по ним горизонтальную линию (изобару), на линии жидкости получим расход жидкости gF, на линии пара – расход пара GF. Нода gF GF параллельна оси абсцисс. Точка F находится на ноде, причем ее абсцисса соответствует величине xF'=0,48. По ноде определяем температуру сырья: t = 111 °С.
Рисунок 6 – График нахождения равновесной температуры
2.4.3 Проверка значения мольной доли отгона
Проверка значения е осуществляется в сравнение исходного значения ет=0,57 и значения ер, полученного с помощью правила рычага:
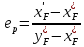 (19)
(19)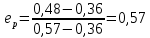 .
.ет=ер – следовательно, xF* и yF* найдены верно.
2.5 Расчет материального баланса ректификационной колонны
2.5.1 Определение молекулярной массы сырья, дистиллята и остатка
Составим материальный баланс без учета теплопотерь в окружающую среду для участка 1 ректификационной колонны, изображенной на рисунке 7.
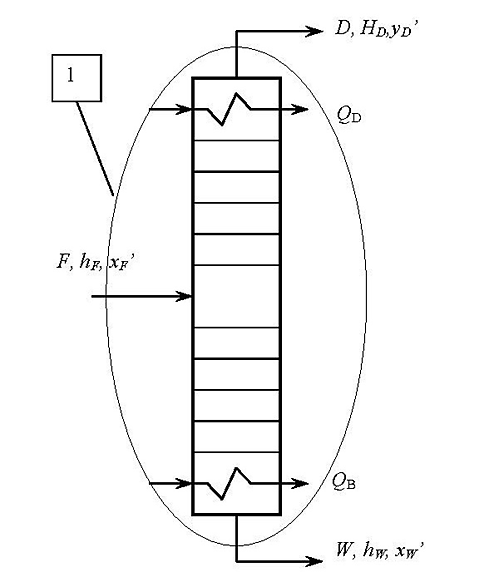
Рисунок 7 – Принципиальная схема ректификационной колонны
Материальный баланс в целом для ректификационной колонны:
F=D+W, (20)
Материальный баланс по низкокипящему компоненту:
F' · x'F = D' · y'D + W' · x'W, (21)
Материальный баланс по высококипящему компоненту
Fꞌ∙(1-xꞌF) =Dꞌ∙(1-yꞌD)+Wꞌ∙(1-xꞌW), (22)
где F, D, W – расходы сырья, дистиллята и остатка;
x'F, y'D, x'W – мольные доли низкокипящего компонента в сырье, дистилляте и остатке.
Материальный баланс составим в мольных и массовых единицах. По условию задания имеем производительность колонны, т.е. расход сырья, F=36 т/час.
Средняя молекулярная масса сырья:
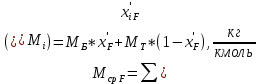 (23)
(23)Средняя молекулярная масса дистиллята:
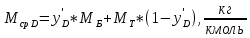 (24)
(24)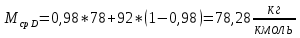
Средняя молекулярная масса остатка:
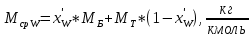 (25)
(25)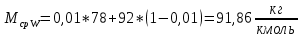
Переведем расход сырья в мольные единицы, для чего по закону аддитивности рассчитаем среднюю молекулярную массу:
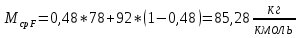
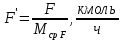 , (26)
, (26)где F' – расход сырья, кмоль/ч;
F – расход сырья, кг/ч;
Mср F – средняя молекулярная масса сырья.
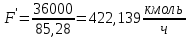
Рассчитаем расход дистиллята и остатка по правилу рычага


 W’ F’ D’
W’ F’ D’
X’W X’F Y’D
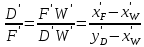 . (27)
. (27)Из уравнения (20) выразим D':
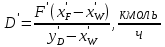 , (28)
, (28)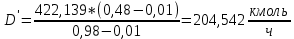 .
.Аналогично рассчитаем выход остатка:
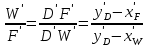 , (29)
, (29)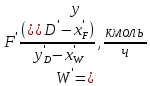 , (30)
, (30)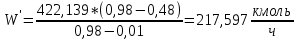 .
.Таким образом, расход дистиллята и остатка по сырью:
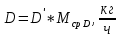 , (31)
, (31)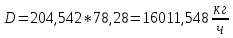
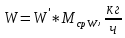 , (32)
, (32)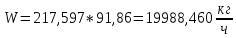
Проверка по уравнению (20)
F’=D’+W’
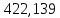 =
=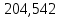 +
+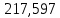 – верно.
– верно.2.5.2 Покомпонентный расчет материального баланса РК
Рассчитаем материальный баланс по каждому компоненту.
Сколько бензола в кмоль/ч в исходной смеси:
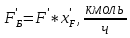 , (33)
, (33)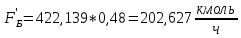 .
.Переведем мольные единицы в массовые.
Найдем содержание бензола в исходной смеси в кг/ч:
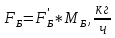 , (34)
, (34)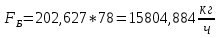 .
.Аналогичным образом рассчитаем мольную и массовую долю для толуола.
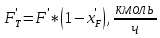 , (35)
, (35)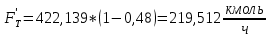 ,
,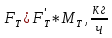 , (36)
, (36)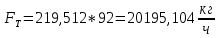
.
Далее рассчитаем, сколько бензола будет в дистилляте:
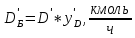 , (37)
, (37)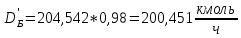 ,
,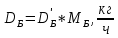 , (38)
, (38)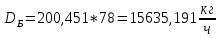 .
.Сколько толуола будет в дистилляте:
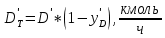 , (39)
, (39)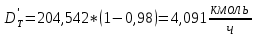 ,
,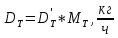 , (40)
, (40)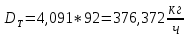 .
.Сколько будет бензола в остатке:
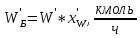 , (41)
, (41)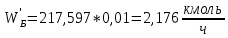 ,
,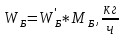 , (42)
, (42)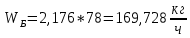 .
.Сколько будет толуола в остатке:
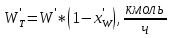 , (43)
, (43)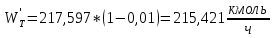 ,
,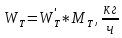 , (44)
, (44)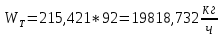 .
. 2.5.3 Проверка материального баланса
По
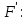
 *0,48=
*0,48= *0,98+
*0,98+ *0,01
*0,01202,627=202,627
По
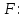 36000=
36000=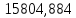 +
+ 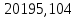
36000=35999,988
% ошибки =
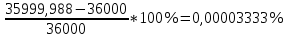
Таблица 6 – Материальный баланс ректификационной колонны
| Компонент | сырье(F) | дистиллят(D) | остаток(W) | |||||
| кг/ч | кмоль/ч | кг/ч | кмоль/ч | кг/ч | кмоль/ч | |||
| Бензол | 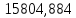 | 202,627 | 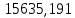 | 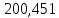 | 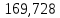 | 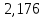 | ||
| Толуол | 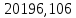 | 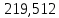 | 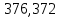 | 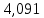 | 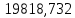 | 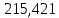 | ||
| Σ | 36000 |  | 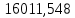 |  | 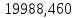 |  | ||