ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 08.07.2024
Просмотров: 17
Скачиваний: 0
Тема № 22. Біохімічні функції нуклеотидів та нуклеїнових кислот. Біологічні мембрани.
Актуальність теми
Нуклеїнові кислоти становлять істотну небілкову частина нуклеопротеїнів. Нуклеопротеїни – це складні білки, в яких небілкова частина представлена нуклеїновими кислотами (ДНК і РНК). ДНК, що локалізується в ядрі, зберігає генетичну інформацію про особливості будови всього організму. Різні види РНК відіграють важливу роль у біосинтезі білка. Крім важливої ролі нуклеїнових кислот у зберіганні та реалізації спадкової інформації, проміжні продукти їх обміну - нуклеотиди, виконують регуляторні функції, контролюючи біоенергетику і швидкість метаболічних процесів.
Мембрани - найбільш розповсюджені клітинні органели. Основними мембранними структурами клітини є плазматична мембрана, ендоплазматичний ретикулум, апарат Гольджи, мітохондріальна і ядерна мембрани. Кожна з них має свої структурні особливості і виконує специфічні функції, але усі вони побудовані по єдиному типу. Вивчення біологічних мембран необхідно для розуміння таких процесів, як взаємодія клітин при утворенні тканин, харчування тканин, фагоцитозу, секреції, трансформації енергії в клітині. Структура і функція мембран порушуються при ряді захворювань і нерідко складають істотний етап патогенезу хвороби.
Мета заняття.
-
Знати хімічну будову складових частин нуклеопротеїнів, будову і функціонування нуклеїнових кислот, їх роль у матричних синтезах.
-
Уміти провести якісні реакції на складові частини нуклеопротеїнів.
-
Уміти на підставі аналізу хімічного складу ліпідів клітинних мембран трактувати їхні фізико-хімічні властивості, необхідні для виконання їх функцій і оцінювати порушення цих функцій при зміні ліпідного складу мембран.
Конкретні завдання.
-
Знати хімічну будову складових частин нуклеопротеїнів, будову і функціонування нуклеїнових кислот, їх роль в процесах біосинтезу білка.
-
Вміти виділити нуклеопротеїни з тканин і провести якісні реакції на їх складові компоненти: а) біуретова проба на поліпептиди; б) реакція Тромера на пентози; в) срібна проба на пуринові основи; г) молібденова проба на фосфатну кислоту.
-
Трактувати амфіфільність ліпідів клітинних мембран як основу їхньої виборчої проникності.
-
Інтерпретувати фізико-хімічні властивості складних ліпідів мембран, що визначають їх взаємодію з білковими компонентами.
Теоретичні питання
-
Компоненти нуклеотидів та нуклеозидів. Мінорні азотисті основи та нуклеотиди. Роль нуклеотидів в утворенні молекул нуклеїнових кислот.
-
Нуклеїнові кислоти: структура, властивості, історичні етапи вивчення.
-
Первинна структура нуклеїнових кислот, полярність полінуклеотидів, особливості первинної структури ДНК та РНК.
-
Вторинна структура ДНК, роль водневих зв’язків у її утворенні (правила Чаргафа, модель Уотсона-Кріка), антипаралельність ланцюгів.
-
Третинна структура ДНК. Фізико-хімічні властивості ДНК: взаємодія з катіонними лігандами; гіпохромний ефект; денатурація та ренатурація ДНК.
-
Будова, властивості й біологічні функції РНК. Типи РНК: мРНК, тРНК, рРНК; особливості структурної організацїї (вторинної та третинної) різних типів РНК.
-
Перетворення ДНК і РНК в шлунково-кишковому тракті.
-
Вільні біологічно активні нуклеотиди та їх біохімічні функції: участь у метаболічних реакціях (АТФ, НАД, НАДФ, ФАД, ФМН, ЦТФ, УТФ) та їх регуляції (циклічні нуклеотиди – 3’,5’-АМФ, 3’,5’-ГМФ).
-
Біохімічний склад біологічних мембран.
-
Ліпіди
-
Білки
-
Вуглеводи
-
Гліколіпіди
-
Глікопротеїни
-
Рідинно-мозаїчна модель біомембран, їх морфо-функціональна асиметрія.
-
Функції біологічних мембран
Практична робота
Якісні реакції на складові частини нуклеопротеїнів
Принцип методу. Для вивчення хімічного складу нуклеопротеїнів зручно користуватися дріжджовими клітинами. Продукти гідролізу можна виявити в гідролізаті реакціями, специфічними для кожної речовини.
Хід роботи: У велику широку пробірку (15 x 1,5 см) кладуть 500 мг пекарських дріжджів або 100 мг сухих дріжджів, заливають 4 мл 10 % розчину H2SO4. Пробірку закривають корком, у який вставлена трубка довжиною 25-30 см, яка служить холодильником, збовтують і ставлять у киплячу водяну баню.
Через 1 – 1,5 год після початку кипіння рідину охолоджують і фільтрують. У фільтраті виявляють продукти гідролізу нуклеопротеїнів: поліпептиди, пуринові та піримідинові азотисті основи, рибозу, дезоксирибозу і фосфатну кислоту.
Дослід 1. Біуретова проба на поліпептиди.
Принцип методу. Біуретова реакція – характерна на сполуки, що містять у своєму складі не менше двох пептидних зв’язків. Такі речовини у лужному середовищі утворюють з СuSO4 комплекс рожево-фіолетового забарвлення. В утворенні цього комплексу беруть участь пептидні зв’язки поліпептидів і білків.
Хід роботи: До 5 крапель гідролізату дріжджів додають 10 крапель 10 % розчину NaOH і 1 краплю 1 % розчину CuSO4. Рідина забарвлюється в рожево-фіолетовий колір.
Зробити висновок.
Дослід 2. Срібна проба на пуринові основи.
Принцип методу. Пуринові основи з аміачним розчином аргентуму нітрату утворюють осад, що забарвлюється у світло-коричневий колір. Реакція відбувається за рівнянням:
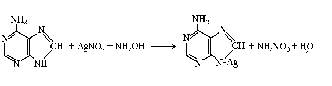
Хід роботи: 10 крапель гідролізату дріжджів нейтралізують концентрованим аміаком і додають 5 крапель 1 % розчину AgNO3. При стоянні через 3-5 хв випадає невеликий пухкий осад світло-коричневого кольору срібних солей пуринових основ (аденіну, гуаніну).
Зробити висновок.
Дослід 3. Проба Тромера на рибозу і дезоксирибозу.
Принцип методу. Моно- і дисахариди, які мають у своєму складі вільний півацетальний гідроксил, здатні у лужному середовищі відновлювати метали (аргентум, купрум, вісмут та інші). Метали у цій реакції відновлюються з одночасним розривом вуглеводневого ланцюга цукрів та полімеризацією.
Хід роботи: До 5 крапель гідролізату дрожей додають 10 крапель 30 % розчину NaOH і 5 – 10 крапель 7 % розчину CuSO4 до появи муті Cu(OH)2, яка не зникає. Рідину змішують і верхній її шар нагрівають до кипіння. Випадає червоний осад закису міді (внаслідок окиснення рибози і відновлення гідрату окису міді до закису).
Зробити висновок.
Дослід 4. Молібденова проба на фосфатну кислоту.
Принцип методу. Фосфати у кислому середовищі утворюють з молібдатами забарвлені фосфатно-молібденові комплекси. Молібденова проба на фосфатну кислоту:
 H3PO4
+ 12 (NH4)2MoO4
+ 21 HNO3
(NH4)3PO4MoO2
+ 21 NH4NO3
+ 12 H2O
H3PO4
+ 12 (NH4)2MoO4
+ 21 HNO3
(NH4)3PO4MoO2
+ 21 NH4NO3
+ 12 H2O
Хід роботи: До 10 крапель молібденового реактиву (розчин молібденового амонію в нітратній кислоті) додають 5 крапель гідролізату дріжджів і кип’ятять декілька хвилин на відкритому вогні. В присутності фосфатної кислоти рідина забарвлюється в лимонно-жовтий колір. При охолодженні випадає жовтий кристалічний осад комплексної сполуки амонію фосфатномолібденового.
Зробити висновок.
Результати досліджень оформляють у вигляді таблиці:
|
Назва реакції |
Продукти гідролізу нуклеопротеїнів |
Компоненти нуклеопротеїнів |
|
|
|
|
Клініко-діагностичне значення. Аналіз ДНК є стандартним дослідженням для діагностики спадкових захворювань. Він може бути використаний для генотипування фетальної тканини в пренатальній діагностиці, яку застосовують для виявлення потенційних батьків.
Похідні азотистих основ широко застосовуються у практичній медицині. Так, меркаптопурин має антилейкемічну активність, що зумовлена його біологічною активністю як антиметаболіта пуринів. Фторурацил і фторофур як структурні аналоги піримідинів мають протипухлинну активність, що пов’язана з перетворенням їх у 5-фтор-2-дезоксиуридин-5’монофосфат, який є конкурентним інгібітором тимідилатсинтази.
Література
Основна:
-
Губський Ю.І. Біологічна хімія. – Київ-Тернопіль: Укрмедкнига, 2000. – 508 с.
-
Вороніна Л.Н., Десенко В.Ф., Мадієвська Н.Н. та ін. Біологічна хімія.- Харків.: Основа, 2000.-.608с.
-
Гонський Я.І., Максимчук Т.П., Калинський М.І. Біохімія людини. – Тернопіль: Укрмедкнига, 2002. – 744 с.
-
Клінічна біохімія/За ред.. Склярова О.Я. - Київ: Медицина, 2006. – 432 с.
-
Лекції, які читаються на кафедрі.
Додаткова:
1. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. – М.: Медицина,1990. – 542 с.
2. Строев Е.А., Биологическая химия.М.:Высшая школа,1986. – 479с.