Файл: Реферат Выпускная магистерская диссертация по теме Формирование микробных сообществ под культурами сосны обыкновенной ( Pinus silvestris L.) в почвогрунтах Бородинского угольного разреза и их участие в процессе почвообразования.doc
Добавлен: 07.11.2023
Просмотров: 79
Скачиваний: 1
СОДЕРЖАНИЕ
1.1 Рекультивация нарушенных земель
1.2 Характеристика Бородинского угольного разреза
1.3 Роль микроорганизмов в процессах почвообразования. Их влияние на
1.4 Ферментативная активность почв
1.4.1 Ферментативная активность техногенно-поверхностных
образований (ТПО). Характеристика почвенных ферментов
2.2 Методы микробиологического анализа фоновой почвы и почвогрунтов
2.2.1 Микробиологические методы
2.2.2 Определение ферментативной активности
Глава 3. Результаты исследований
3.1. Химическая оценка исследуемых участков почвогрунтов (№16 и №19) и фоновой почвы
3.2 Микробиологические характеристики почвогрунтов и фоновой почвы в 2014 г.
3.3 Микробиологические характеристики почвогрунтов и фоновой почвы в 2015 г.
Активность инвертазы - один из наиболее устойчивых показателей, обнаруживающий наиболее четкие коррелятивные связи с воздействующими факторами. Исследованиями А. Ш. Галстяна [47, 50] установлена корреляция инвертазы с активностью других почвенных карбогидраз. Активность инвертазы исследована во многих почвах. Инвертазная активность в почве убывает по профилю, коррелирует с содержанием гумуса [47, 62, 63]. Корреляция с гумусом может отсутствовать при значительном содержании в почве алюминия, железа, натрия. Тесная связь активности инвертазы с количеством почвенных микроорганизмов и их метаболической активностью свидетельствует о преимуществе в почве инвертазы микробного происхождения [64, 65, 66]. Однако такая зависимость не всегда подтверждается, активность инвертазы значительно более устойчивый показатель и непосредственно может быть не связана с колебаниями численности микроорганизмов.
Оксидоредуктазы представлены такими ферментами как каталаза, пероксидаза и полифенолоксидаза, которые играют важную роль в процессах гумусообразования.
Класс оксидоредуктаз.
Полифенолоксидаза катализирует окисление полифенолов в хиноны в присутствии свободного кислорода воздуха. Пероксидаза же катализирует окисление полифенолов в присутствии перекиси водорода или органических перекисей. При этом ее роль состоит в активировании перекисей, поскольку они обладают слабым окисляющим действием на фенолы. Далее может происходить конденсация хинонов с аминокислотами и пептидами с образованием первичной молекулы гуминовой кислоты, которая в дальнейшем способна усложняться за счет повторных конденсаций [67].
Замечено [51], что отношение активности полифенолоксидазы к активности пероксидазы, выраженное в процентах, имеет связь с накоплением в почвах гумуса, поэтому эта величина получила название условный коэффициент накопления гумуса (К).
Глава 2. Материалы и методы
2.1 Объекты исследования
Объектами исследования служили почвогрунты двух участков №16 и №19 (литостраты), сформированные на отвалах Бородинского угольного разреза в 2005 г. (рис. 3,4), контрольным участком являлась фоновая почва березняка разнотравного (50 лет) (рис.2).
[Изъята 1 страница]
На участках рядами произрастают культуры сосны обыкновенной 8-10 лет (ряд), между рядами развивается травянистая растительность (междурядье). Далее по тексту, термином «ряд» обозначается почва ризосферы сосны обыкновенной, под «междурядьем» подразумевается почва под травостоем. Следовательно, на данном этапе развития искусственные сообщества представлены двумя разностями: древесной и травяной. Процессы почвообразования на таких участках идут по-разному, что характерно только для начальных этапов формирования культур, после того как кроны культур сомкнутся, напочвенный покров, как правило, становится скудным и характеризуется как мертвопокровный.
2.2 Методы микробиологического анализа фоновой почвы и почвогрунтов
Образцы почв для химического, микробиологического и биохимических анализов отбирали в течение двух вегетационных сезонов - 2014 г (июль, август) и 2015 г. (июль, сентябрь) из прикопок с глубины 0-5, 5-10 см. Почва контрольного участка, находящегося на территории Бородинского угольного разреза, определена как серая лесная [68, 69]. При отборе образцов почвы и почвогрунтов замеряли температуру портативным цифровым термометром «HANNA ChekTemp1» с выносным датчиком. После доставки образцов в лабораторию в них традиционными методами определяли влажность почвы, значения рН измеряли в водной вытяжке, приготовленной из 1 г почвы, растворенной в 10 мл дистиллированной воды (1:10) в течение 1 часа, при помощи портативного потенциометра «Аквилон-410».
Эксперимент по скорости утилизации различных субстратов микробными группами (ЭТГМ) был заложен 11 июня 2015 года. Его продолжительность составила 1 месяц (дата окончания 2 июля 2015 года). Образцы почвы для микробиологических анализов были отобраны в сентябре 2014 г. с двух нерекультивированных (литостраты) участков №16 м/р (междурядье) и №16 р (ряд), сформированных на отвалах Бородинского угольного разреза в 2005 г. Всего было 29 образцов, исследуемый почвенный профиль 0-10 см. Каждый слой почвы был взят в трех повторностях, с добавлением: 1) воды, 2) сульфат аммония + вода 3) пептон + вода. Почву инкубировали в течение 4 недель при оптимальных показателях влажности (60% от полной влагоемкости) и температуры (28°С).
2.2.1 Микробиологические методы
Общую численность и состав эколого-трофических групп микроорганизмов определяли классическими методами с использованием ряда диагностических сред [70, 71] мясо-пептонный агар (МПА), крахмалоаммиачный агар (КАА), сусло-агар (СА) и почвенный агар (ПА) для выявления и количественного учета олиготрофных бактерий. На поверхность всех сред вносили почвенную суспензию (разведение 1:103), засеянные чашки Петри помещали в термостат (27°С) на 3–7 суток. Для оценки разложения и накопления органических веществ в верхней части горизонта торфяных почв рассчитывали коэффициенты микробиологической минерализации (КМИН), согласно соотношению численности микроорганизмов, выросших на КАА и МПА (КАА/МПА), и олиготрофности (КОЛИГ), как соотношение ПА/МПА [72]. Результаты численности микроорганизмов, выросших на питательных средах, выражали в колониеобразующих единицах (КОЕ) на 1 г почвы [70].
К
 оличество колониеобразующих единиц (КОЕ) рассчитывали по [70]: ( ±2σ ) *К*1/V, где
оличество колониеобразующих единиц (КОЕ) рассчитывали по [70]: ( ±2σ ) *К*1/V, где 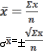 – среднее число колоний, выросшее при высеве из данного разведения; – среднее квадратичное отклонение; 2 – t- критерий при Р0,95; К –
– среднее число колоний, выросшее при высеве из данного разведения; – среднее квадратичное отклонение; 2 – t- критерий при Р0,95; К – разведение, из которого проведен высев; V – объем суспензии, взятый для посева, мл;
Респирометрические микробиологические показатели (базальное дыхание, микробная биомасса, микробный метаболический коэффициент), в том числе и пространственно-распределенные, исследовали методом субстратиндуцированного дыхания (СИД) [73].
Субстрат-индуцированное дыхание (СИД) контрольной почвы и почвогрунтов оценивали по скорости начального максимального дыхания микроорганизмов после добавления в почву глюкозы. Во флаконы (250 мл) помещали 2 г почвы (60% полной влагоемкости) и добавляли 0.1 мл глюкозоминеральной смеси (ГМС) [73, 74]. Флаконы герметично закрывали пробками, фиксировали время и инкубировали при 25°С. Через 3 ч инкубации пробу воздуха из флакона (5 мл) отбирали шприцем и вводили в газовый хроматограф Agilent Technologies 6890N Network GC (USA). Скорость СИД выражали в мкг СО
2 -С / г почвы в час.
Микробную биомассу почвы (МБ) определяли путем пересчета скорости субстрат-индуцированного дыхания (СИД) по формуле:
Смик=МБ (мкг С / г почвы) = 40.04 (мкл СО2 / г почвы в час) + 0.37 [74].
Базальное (фоновое) дыхание (БД) почвы и почвогрунтов измеряли по скорости выделения СО2 за 24 ч инкубации при 25° С. Скорость продуцирования СО2 определяли хроматографически, как описано для определения СИД, только вместо внесения раствора ГМС в почву, вносили воду. Скорость базального дыхания выражали в мкг С - СО2 / г почвы / час.
Микробный метаболический коэффициент (qCO2) рассчитывали как отношение БД и МБ[75].
Для выявления зависимостей между микробиологической активностью разных участков и гидротермическими и химическими параметрами ТПО проведены дисперсионный и корреляционный анализы; коэффициенты корреляции (r) значимы при р<0.05 (р<0.01). Полученные данные обработаны при помощи статистического пакета программ Microsoft Excel 2003 (2007) .
2.2.2 Определение ферментативной активности
Ферментативную активность почвогрунтов и контрольной почвы определяли методами, предложенными Ф.Х. Хазиевым [76] и выражали: инвертазу мг/глюкозы / 1г почвы, уреазу мг/N-NH4/ 1г почвы, пероксидазу мг бензохинона/ 1 г почвы, полифенолоксидазу мг бензохинона/ 1 г почвы (далее по тексту единицы фермента – ед. ф.).
Определение пероксидазы и полифенолоксидазы. Методы определения пероксидазной активности почвы основаны на учёте количества продуктов окисления полифенолов, используемых в качестве субстратов фермента, путём фотометрических измерений интенсивности их окраски в случае образования окрашенных соединений или методом титрования. В коническую колбу помещали 1 г почвы, заливали 10 мл 1% раствора гидрохинона и 1 мл 0,05% раствора перекиси водорода. Перемешивали и ставили в термостат на 30 минут при 30°С. В качестве контроля ставили смесь растворов гидрохинона и перекиси водорода без почвы. После инкубации добавляли по 10 мл спирта в опытные и контрольные колбы и фильтровали. Далее вытяжку колориметрировали при длине волны 400 нм в 1 см кювете напротив контрольной вытяжки без почвы.
Методы определения полифенолоксидазной активности почвы основаны на измерении скорости окисления внесённых в почву полифенолов.
Полифенолоксидазу определяли точно также, но, без добавления перекиси водорода.
Двухатомный фенол – гидрохинон окисляется под действием в одном случае при участии перекиси водорода, в другом случае естественным путем (в присутствии кислорода воздуха) до 1,4-п-бензохинона. Результат выражали в мг 1,4-п-бензохинона на 1 г почвы за 30 мин. Хиноны принимают непосредственное участие в процессе гумусообразования, так как реакция конденсации хинонов с пептидами и аминокислотами ведет к образованию первичных молекул гуминовой кислоты [76].
Коэффициент гумификации находили при помощи соотношения ПФО и ПО (Кг=ПФО / ПО).
Определение инвертазы. В коническую колбу помещали 5 г почвы (подстилки 1 г), затем добавляли 5 мл 20% сахарозы и 5 мл ацетатного буфера. Чтобы приготовить который, необходимо 120 мл ледяной уксусной кислоты разбавить водой до 1 л, затем 164 г безводного CH3COONa растворить в 1 л воды, и после смешать два раствора в пропорции 1:8. Далее ставили в термостат на 3 часа при температуре 370°С. После,