Файл: Общая характеристика группы веществ, изолируемых из биологического материала настаиванием с полярными растворителями.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 08.11.2023
Просмотров: 279
Скачиваний: 5
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Токсические дозы барбитуратов вызывают первоначально наркотическое опьянение, затем коматозное состояние, которое осложняется сердечнососудистой или дыхательной недостаточностью.
Тяжелые отравления характеризуются глубокой комой, редким поверхностным дыханием, слабым пульсом, цианозом. Зрачки у пострадавшего узкие, не реагирующие на свет.
В заключительной стадии отравления, вследствие поражения дыхательного центра, дыхание становится неравномерным, после чего наступает его остановка. Токсическое действие барбитуратов усиливают наркотики, алкоголь, транквилизаторы. Токсическими дозами для для барбамила - 1-3 г, этаминала-натрия 1,5-2,5
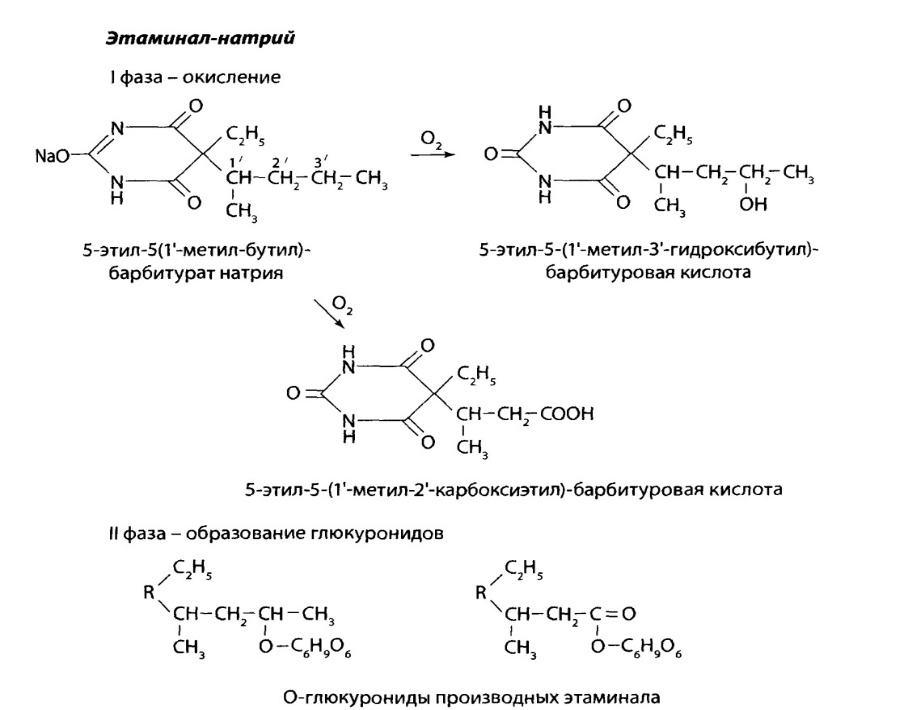
ЭТАМИНАЛ-НАТРИЙ
представляет собой белый порошок, растворимый в воде и этиловом спирте, практически не растворимый в диэтиловом эфире. Этаминал экстрагируется органическими растворителями из кислых водных растворов.
Обнаружение этаминал-натрия
1. Этаминал-натрий дает фиолетовую окраску с солями кобальта и изопропиламином.
2. С солями кобальта и щелочами этаминал-натрий дает розовую окраску.
3. Этаминал-натрий дает реакцию образования мурексида.
4. Этаминал-натрий дает оранжево-красную окраску с родамином 6Ж. Окрашенное соединение хорошо экстрагируется четыреххло-ристым углеродом. Эта реакция может быть использована для обнаружения этаминал-натрия в порошках, таблетках и др.
5. После прибавления концентрированной серной кислоты к этаминал-натрию через 10—15 мин образуется осадок (сростки из призматических кристаллов). Предел обнаружения: 5 мкг этаминал-натрия в пробе.
6. При взаимодействии этаминал-натрия с хлорцинкиодом образуется коричневый или оранжево-коричневый кристаллический осадок (призмы или сростки из них). Предел обнаружения: 4 мкг этаминал-натрия в пробе.
7. Этаминал-натрий со смесью хлорида железа (III) и иодида калия дает кристаллический осадок коричневого или оранжево-коричневого цвета (призмы и сростки из них).
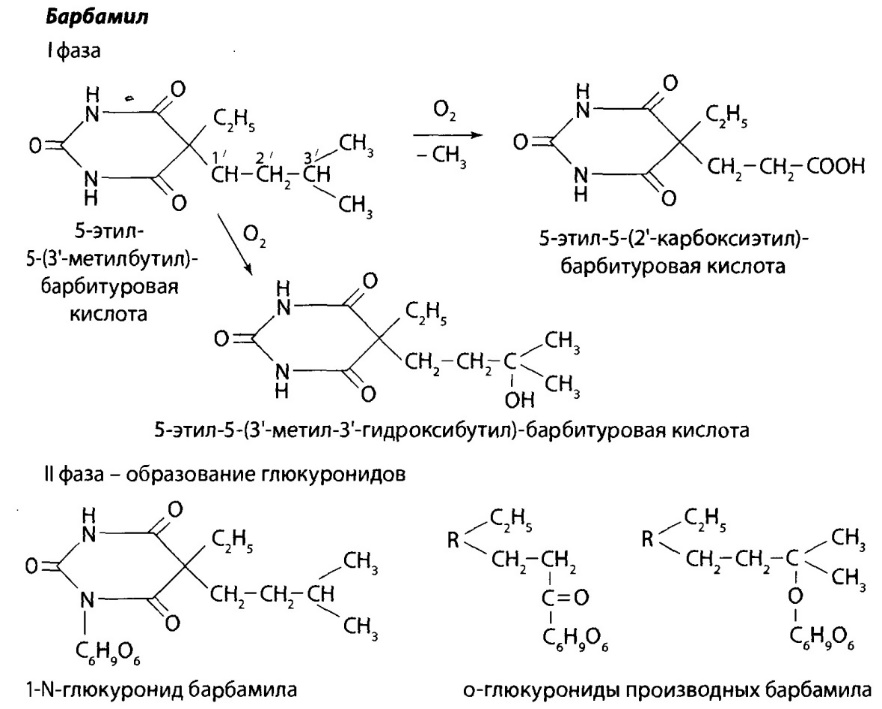
БАРБАМИЛ
Барбамил- белый аморфный гигроскопический порошок
без запаха. Хорошо растворяется в воде и этиловом спирте
Обнаружение барбамипа
-
Барбамил с изопропиламином и солями кобальта дает фиолетовую окраску. -

2. При взаимодействии барбамила с солями кобальта и щелочами появляется розовая или красная окраска.
3. Барбамил дает положительную мурексидную реакцию.

4. Барбамил с родамином 6Ж образует ионный ассоциат, раствор которого в четыреххлористом углероде имеет оранжевую окраску.
5. При действии H 2 SO 4 на барбамил выделяется кислотная форма этого препарата, образуется осадок, частицы которого имеют форму пластинок или призм, сгруппированных в виде сфероидов. Предел обнаружения: 21 мкг барбамила в пробе.
6. Хлорцинкиод с барбамилом образует темно-красные или золотистые прямоугольные пластинки или сростки из них. Предел обнаружения: 7 мкг барбамила в пробе.
7. Барбамил со смесью, растворов хлорида железа (III) и иодида калия образует кристаллический осадок (призмы или сростки из них) оранжево-коричневого или коричневого цвета.
Методы определения барбитуратов в биологических объектах
Объекты анализа:
• трупный материал (внутренние органы);
• биологические жидкости (кровь, моча);
• лекарственные препараты.
12. Производные пиразолона: амидопирин и антицирин в химико-токсикологическом, отношении.
Случаи острого отравления производными пиразола редки и встречаются, как правило, среди детей младшего возраста. При отравлении наиболее характерно поражение ЦНС. Через 5-10 мин после приема наблюдают потерю сознания, цианоз кожных покровов и слизистых оболочек, клоникотонические судороги. Смерть наступает через 1-3 часа после приема вещества вследствие остановки дыхания. Патологоморфологическая картина неспецифична. В диагностике острого отравления иногда отмечают красноватый цвет мочи из-за наличия в ней рубеановой кислоты.
Антипирин- бесцветные кристаллы или белый кристаллический порошок без запаха, слабогорького вкуса. Растворяется в воде (1 : 1), этиловом спирте (1 : 1), хлороформе (1 : 1), диэтиловом эфире (1 :50).
Метаболизм 1-окисление, гидроксилирование, 2 коньюгация с укс. Кислотой, глюкуроновой.
Около 30—40 % введенной дозы антипирина связывается с глюкуроновой кислотой и выделяется в виде глюкуронида. Некоторое количество антипирина подвергается гидроксилированию с образованием 4-гидроксиантипирина.
Общие методы обнаружения. Анализ на производные пиразола проводится с остат-ками, полученными после испарения хлороформных экстрактов из водных вытяжек при значениях рН=2 и рН=8-10. При проведении ТСХ-скрининга в общей системе растворителей производные пи-разола обнаруживаются в виде окрашенных пятен при обработке пластинки хлоридом железа(II1) или реактивом Драгендорфа (см. раздел 7.1.2). Производные пиразола дают осадки с общими осадительнымиреактивами. Для обнаружения индивидуальных веществ используют реакции окрашивания, УФ-спектрофотометрию, ИК-спектроскопию и ВЭЖХ.
Предварительное обнаруж. 1. С хлоридом железа- оранжево-красное
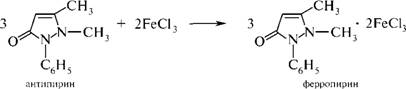
2. тсх-скрининг хлороформ: ацетон(9:1) при исслед. Из кислой среды.
Частные реакции
1.Реакция образования нитрозоантипирина. При взаимодействии антипирина с азотистой кислотой образуется нитрозоантипирин, имеющий зеленую окраску:
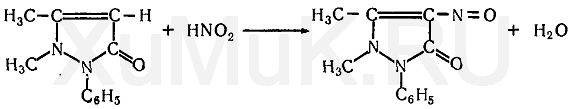
2. Реакция образования азокрасителя. Если к антипирину прибавить раствор нитрита натрия и уксусную кислоту, то образуется нитрозоантипирин (см. предыдущую реакцию), который при взаимодействии с α-нафтиламином образует пиразолоновый азокраситель, имеющий красную окраску.
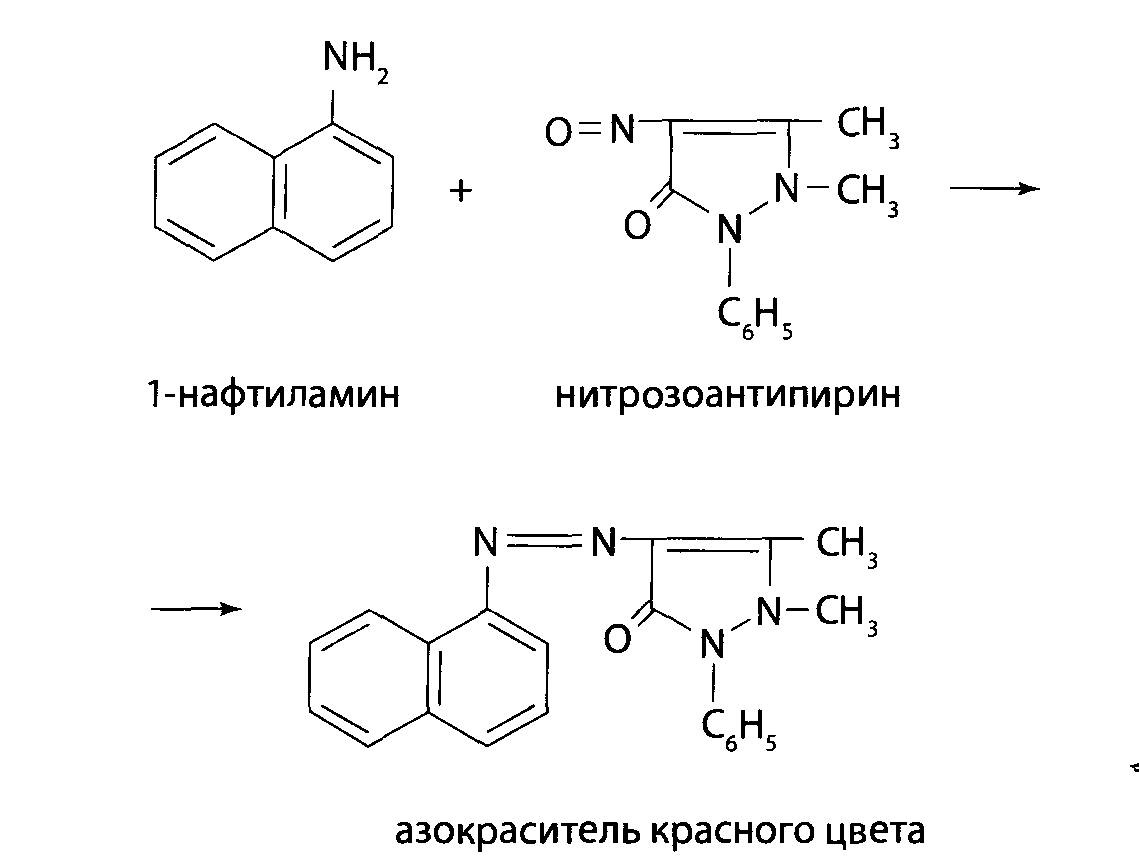
-
С нитратом серебра- фиолетовая окраска
токсическая доза 10-15 г
А
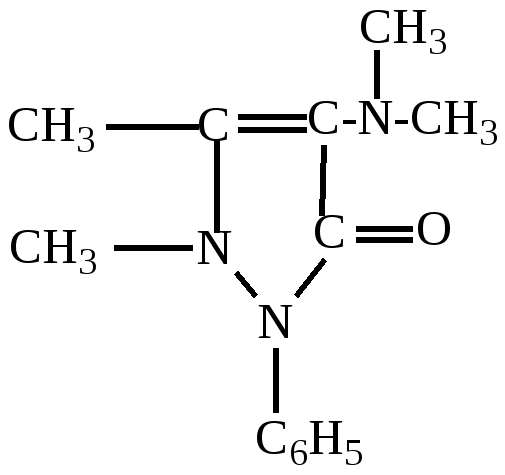 мидопирин
мидопирин^ Физико-химические свойства: Амидопирин (пирамидон, аминофеназон, аминопирин). Это мелкие бесцветные кристаллы, едва горьковатые на вкус. Амидопирин растворяется в хлороформе (1:1), этиловом спирте (1:2), диэтиловом эфире (1:13), воде (1:20).
При действии окислителей на амидопирин
образуется ряд окрашенных промежуточных продуктов. При дальнейшем окислении этих продуктов образуется бесцветное вещество -диоксиамидопирин:
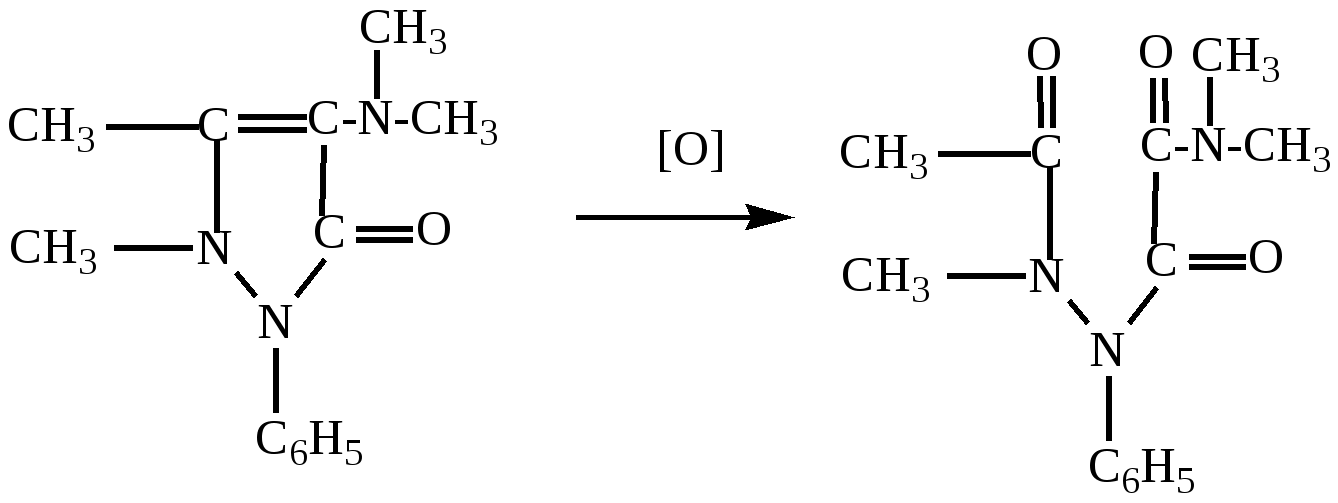
Промежуточные продукты окисления амидопирина синего или сине-фиолетового цвета. Цвет возникает при взаимодействии амидопирина с растворами ферум (III) хлорида, нитратной и нитритной кислот, аргентум нитрата, плюмбум (IV) оксидом и другими окислителями.
Амидопирин экстрагируется органическими растворителями из кислых и щелочных водных растворов.
Реакция с реактивами группового осаждения алкалоидов. Амидопирин с реактивами группового осаждения алкалоидов (таннин, пикриновая кислота, реактив Майера и др.) дает осадки.
Реакция с хлоридом железа (III). Появление фиолетовой окраски указывает на наличие амидопирина в растворе.
При больших количествах амидопирина может выпадать черный осадок металлического серебра. Реакция с азотистой кислотой. При наличии амидопирина появляется фиолетовая окраска, исчезающая от избытка реактива.
Метаболизм. Амидопирин метаболизирует путем деметилирования и ацетилирования. Метаболитами амидопирина являются 4-аминоантипирин, метиламиноантипирин, рубазоновая и метилрубазоновая кислоты.
Эти кислоты имеют красноватый цвет. Поэтому у людей, которые принимают большие дозы амидопирина, моча может приобретать красно-бурый цвет.
Обнаружение амидопирина и антипирина при их совместном присутствии. Для этой цели применяют описанную выше реакцию с азотистой кислотой. Вначале появляется фиолетовая окраска, которую дает амидопирин. Затем под влиянием избытка реактива эта окраска исчезает, а появляется зеленая (нитрозоантипирин)
токсическая доза 10-15 г
13. Производные пиразолона: анальгинин и амидопирин в химико-токсикологическом, отношении.
Случаи острого отравления производными пиразола редки и встречаются, как правило, среди детей младшего возраста. При отравлении наиболее характерно поражение ЦНС. Через 5-10 мин после приема наблюдают потерю сознания, цианоз кожных покровов и слизистых оболочек, клоникотонические судороги. Смерть наступает через 1-3 часа после приема вещества вследствие остановки дыхания. Патологоморфологическая картина неспецифична. В диагностике острого отравления иногда отмечают красноватый цвет мочи из-за наличия в ней рубеановой кислоты.
А
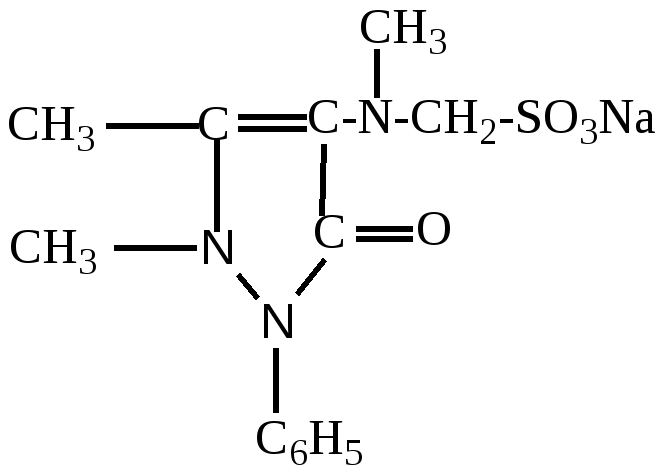 НАЛЬГИН
НАЛЬГИН^ Физико-химические свойства: анальгин (метамизол натрий) или фенил-1-N-2-Метансульфонат натрия. Белый или белый с едва заметным желтоватым оттенком кристаллический порошок. В присутствии влаги быстро разлагается. Растворяется в воде, незначительно в спирте, нерастворимый в эфире, хлороформе, ацетоне.
Применение. В медицине применяют при болевом синдроме разнообразного ґенеза (головная боль, невралгия, радикулит), грипп, ревматизм и др. Входит в состав многих препаратов: спазган, спазмалгон, анальгин-хинин и др.
^ Действие на организм. Анальгин имеет анальгезирующее и жаропонижающее действие. Усиливает действие этанола. При передозировке наблюдается тошнота, рвота, одышка, сонливость, понижение артериального давления, паралич дыхательных мышц.
Метаболизм.
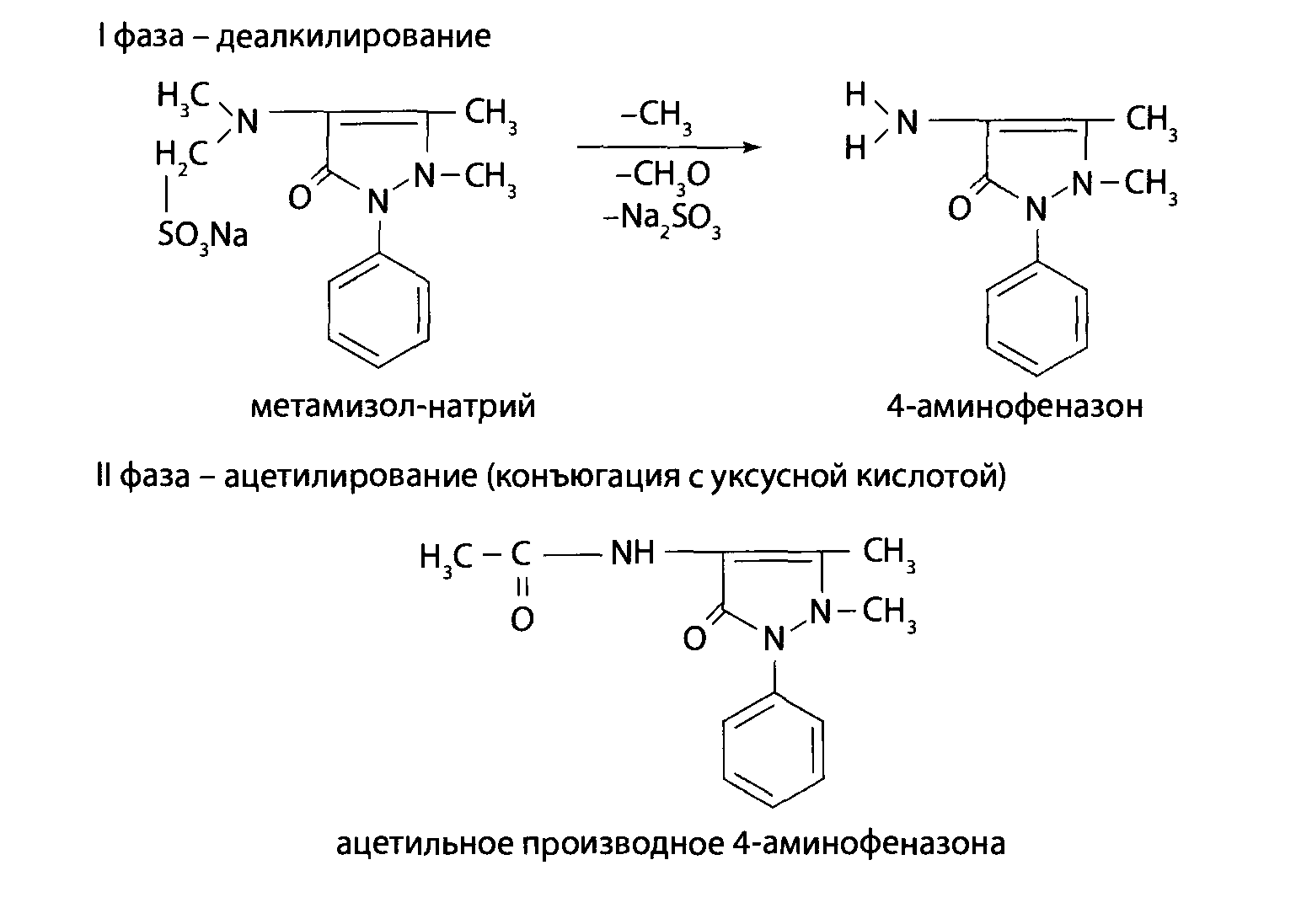
Общие методы обнаружения. Анализ на производные пиразола проводится с остат-ками, полученными после испарения хлороформных экстрактов из водных вытяжек при значениях рН=2 и рН=8-10. При проведении ТСХ-скрининга в общей системе растворителей производные пи-разола обнаруживаются в виде окрашенных пятен при обработке пластинки хлоридом железа(II1) или реактивом Драгендорфа (см. раздел 7.1.2). Производные пиразола дают осадки с общими осадительнымиреактивами. Для обнаружения индивидуальных веществ используют реакции окрашивания, УФ-спектрофотометрию, ИК-спектроскопию и ВЭЖХ.
Обнаружение метамизола. Метамизол обладает выраженными восстановительными свойствами.
Для него характерны реакции окисления. В качестве окислителей могут быть использованы йодат калия, хлорид железа(1I1), нитрат серебра, нитрит натрия и др. Характерное окрашивание появляется в первые минуты после добавления реактива. При стоянии окраска изменяется или исчезает.
Реакции окисления сопровождаются гидролитическим расщеплением молекулы метамизола, особенно при нагревании. Образующиеся продукты (оксид серы (IV), формальдегид) обнаруживаются по запаху или соответствую-щими реакциями. Реакция обнаружения диоксида серы с йодатом калия. Сухой остаток переносят в пробирку, добавляют 1,5 мл воды очищенной, 1,5 мл 10°/о раствора хлороводородной кислоты. Над горлышком пробирки располагают фильтровальную бумагу, пропитанную раствором йодата калия и крахмалом (20 мг в 2 мл раствора крахмала). При нагревании пробирки наблюдают посинение бумаги.