Файл: Общая характеристика группы веществ, изолируемых из биологического материала настаиванием с полярными растворителями.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 08.11.2023
Просмотров: 282
Скачиваний: 5
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
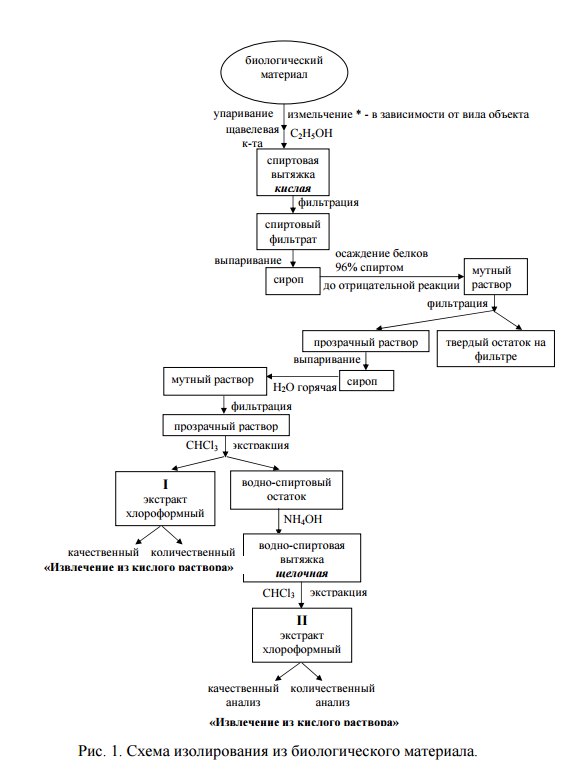
ский материал заливают новой порцией этилового спирта, подкисляют10%-м спиртовым раствором щавелевой или винной кислот до рН=2-3 и оставляют на сутки. Настаивание биологического материала с новыми порциями подкисленного спирта производят 3-4 раза.
Спиртовые вытяжки соединяют, а оставшийся биологический материал промывают спиртом, который приливают к соединенным спиртовым вытяжкам.Эти вытяжки фильтруют через небольшой бумажный фильтр. Фильтрат переносят в фарфоровую чашку и выпаривают на водяной бане (35-40°С) догустоты сиропа. Для экономии спирта фильтрат можно перенести в колбу ипод вакуумом отогнать спирт до получения сиропообразной жидкости. К
жидкости, перемешиваемой стеклянной палочкой, по каплям прибавляют 96-градусный или абсолютный спирт до прекращения осаждения белковых веществ. Если одновременно прибавить большое количество спирта, то выпадет осадок белковых веществ в виде сгустков. Этот осадок может увлекать израстворов исследуемые вещества. После отстаивания жидкости с осадком ее
фильтруют, осадок на фильтре промывают спиртом. Фильтрат снова выпаривают до густоты сиропа, а затем по каплям добавляют спирт и фильтруют.Упаривание спиртовой жидкости до густоты сиропа и обработку ее спиртомпроизводят до тех пор, пока не прикатится выпадение осадка. После этого жидкость фильтруют и прибавляют 20-25 мл воды.
• Кислую водно-спиртовую жидкость, очищенную от белковых веществ и других примесей, переносят в делительную воронку и 3-4 раза взбалтывают схлороформом (порциями по 10-15 мл). Полученные при этом хлороформныевытяжки соединяют и исследуют на наличие токсикологически важных веществ.
При исследовании биологических жидкостей (кровь, моча, плазма, слюна, промывные воды желудка) используют жидкость-жидкостную экстракцию.
• Пробу подкисляют соляной кислотой до рН=2-3 и экстрагируют эфиром(фракция А, «кислое» извлечение), водную фракцию отделяют, затем подщелачивают до рН=9-10 и экстрагируют хлороформом (фракция Б, «щелочное»извлечение).
Для некоторых соединений, присутствующих в биологической жидкости (моче) преимущественно в виде конъюгатов, в частности с глюкуроновой кислотой, проводится предварительный гидролиз в присутствии соляной кислоты. Современным методом изолирования токсикантов из биологических жидкостей является сорбция на синтетических смолах модифицированных силикагелях и активированном угле. Сорбент упакован в специальный патрон и удобен для использования в экспресс-анализе малых объемов пробы. Сорбция на твердом носителе с последующим фракционным элюированием позволяет провести очистку и сконцентрировать вещество. Однако существует опасность потерь токсичных веществ с неизученными характеристиками удерживания
Схема исслед мочи на барбитураты.
17. производные 1,4-бензодиазенина. Общая характеристика группы. Токсичность, пути метаболизма.
Свойства производных 1,4-бензодиазепина.
Оксазепам, диазепам, хлордиазепоксид -белые кристаллические вещества. Допускается желтоватый, зеленовато-желтый или кре-мовый оггенок.
Нитразепам имеет светло-желтую с зеленым оггенком окраску за счет наличия в молекуле нитрогруппы.
Производные бензодиазепина практически нерастворимы в воде, мало растворимы в этаноле и эфире, но хорошо растворимы в хлороформе. Они обладают слабоосновными свойствами за счет гетероатома азота в положении 4 и слабокислотными свойствами за счет имидоимидольной таутомерии в положении 1-2. В электронных спектрах производных 1,4-бензодиазепина наблюдаются 3 полосы поглощения с характерными максимумами в области 200-215, 220-260, 280-360 нм.
Бензодиазепины обладают выраженными токсическими свойствами. Описаны случаи отравлений в отечественной и зарубежной литературе в результате несчастных случаев (чаще всего с маленькими детьми) или с целью самоубийства.
Смертельная доза для взрослого человека 0,1-0,15 г на 1 кг массы тела (68-120 таблеток хлозепида), для де-тей - 0,02-0,15 г на 1 кг массы тела (29 таблеток хлозепида для детей 7-14 лет).
Препараты хорошо всасываются из пищеварительного тракта. Клиническая картина отравления зависит от принятой дозы. При легкой степени отравления хлозепидом проявляется вялость, сонливость, заторможенность, расширение зрачков, снижение мышечного тонуса. При отравлениях средней тяжести признаки отравления, указанные выше, выражены более четко. Добавляется гиперемия лица, сухость кожных покровов, тахикардия, тремор конечностей, отсутствие многих рефлексов.
При тяжелой форме отравления сознание спутано, наблюдается психомоторное возбуждение, клонические судороги или галлюцинаторный синдром, развивается дыхательная и сердечная недостаточность.
Диазепам по действию на организм сходен с хлозепидом, но его токсическое действие проявляется в меньших дозах. Оксазепам (тазепам) менее токсичен, чем хлозепид. Нитразепам оказывает более выраженное успокаивающее и снотворное действие.
Картина отравления сходна с хлозепидом. При патологоанатомическом исследовании трупа отмечают кровоизлияния в слизи-стую оболочку желудка и тонкого кишечника, острую эмфизему легких, полнокровие внутренних органов, расширение зрачков.
Пути метаболизма
Производные бензодиазепинов в организме быстро подвергаются метаболизму. Через несколько минут после приема в крови обнаруживаются метаболиты хлозепида.
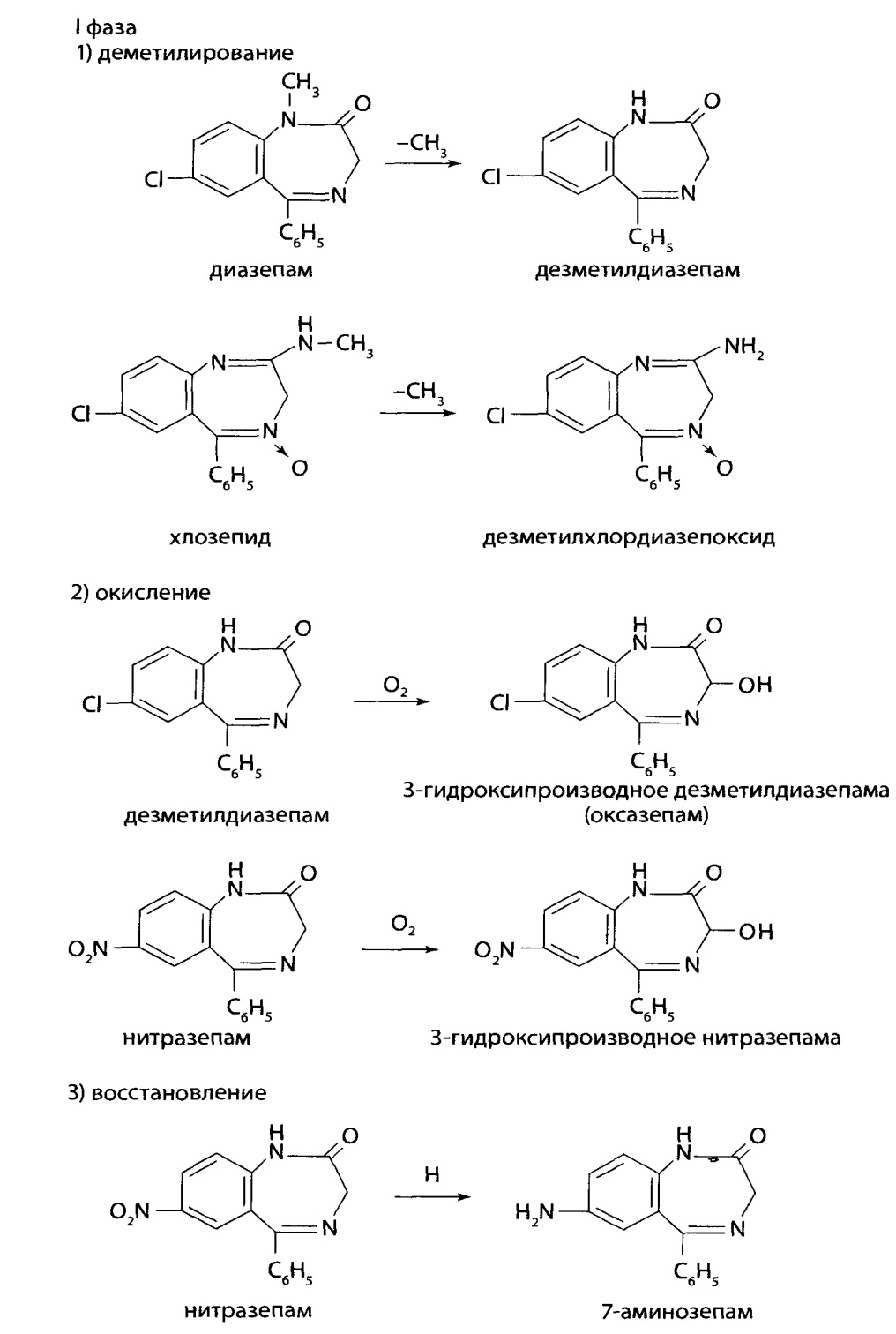
В I фазе метаболизма характерны процессы деметилирования (диазепам, хлозепид) в положении 1 и 2, окисления в положении 3 с образованием гидроксильной группы, восстановления нитрогруппы в положении 7 (нитразепам).
Во II фазе метаболизма происходит конъюгация с глюкуроновой или серной кислота-ми самих препаратов, имеющих гидроксил в 3 положении, и продуктов их метаболизма. Метаболит нитразепама (аминозепам) образует конъюгат с уксусной кислотой. Метаболиты, конъюгаты с кислотами и нативные соединения производных бензодиазе-пина выводятся из организма почками.
18. Схема исследования внутренних органов трупа на наличие производных 1.4-бензодиазепина по нативным веществам.
100,0 б.о. пробоподготовка метод Васильевой ( 10% р-р щавельевой кислоты рН=2-3) Стаса-отто экстрагирование( хлороформ, рН2-3. 9-10 хлороформное извлечение выпаривание до суха( 6н НCl 140градусов, 30-60 мин)1. предварительные исследования - гидролизат(до появление желто коричнев окраски ТСХ в общей скрининг 2. подтверждающие реакции 3. количественное определение( СФМ, ФЭК, ВЭЖХ) 235, 390 нм для щелочи, 265 нм- для кислой среды
1. Проведение гидролиза.
I мл хлороформного раствора исследуемого вещества или экстракта помещают в пробирку и выпаривают досуха на кипящей водяной бане. К сухому остатку добавляют 5 мл 6 н. соляной кислоты и содержимое нагревают с обратным холодильником на кипящей водяной бане в течение 60 минут. Образование жёлто-коричневого окрашивания гидролизата позволяет предположить наличие производных 1,4-бензодиазепина в исследуемом экстракте.
2. ТСХ-скрининг.
Общая система растворителей: хлороформ - диоксан - ацетон-25% - аммиак (45:47,5: 5: 2,5).
Способ детекции: реактив Драгендорфа.
3. Подтверждающие реакции. Могут быть любые в зависимости от группы.
3.1.Реакция образования азокрасителя.
Охлажденный гидролизат, нейтрализуют кристаллическим гидроксидом натрия до рН=7-9, охлаждая пробирку под струей холодной воды.
К 1 мл нейтрализованного гидролизата прибавляют 0,5 мл 1 н. раствора соляной кислоты, 0,5 мл 10% раствора нитрита натрия и оставляют на 3 минуты. Затем прибавляют 0,5 мл 0,1% раствора N-нафтилэтилендиамина гидрохлорида (реакция Браттона-Маршала) или щелочной раствор Р-нафтола. При наличии аминобензофенонов появляется вишневая (оранжево-красная) окраска.
3.2. Реакция с реактивом Марки.
0,5 мл хлороформного раствора исследуемого вещества или экстракта помещают в выпарительную чашку и прибавляют несколько капель реактива Марки. Наблюдают появление жёлто-оранжевого окрашивания.
3.3. Реакция с реактивом Драгендорфа.
0,5 мл хлороформного раствора исследуемого вещества или экстракта помещают в выпарительную чашку и прибавляют несколько капель 2 н. раствора уксусной кислоты и реактива Драгендорфа. Появляется жёлто-оранжевое окрашивание.
3.4. Реакция с нингидрином.
0,5 мл хлороформного раствора исследуемого вещества или экстракта помещают в выпарительную чашку и прибавляют 0,5 мл этилового спирта, 1 мл раствора нингидрина и нагревают 2 минуты на водяной бане. После прибавления этилового спирта раствор приобретает синюю окраску, которая от 2 капель 1% раствора сульфата меди (II) переходит в красную (диазепам), жёлтую (нит-разепам), коричневую (оксазепам).