Файл: Лабораторная работа 3 Изучение кинетики химических реакций 313080120009 Аликберов М. Н. Дата сдачи 23. 05. 23.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 22.11.2023
Просмотров: 151
Скачиваний: 14
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
САНКТ-ПЕТЕРБУРГСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ ПЕТРА ВЕЛИКОГО
ЛАБОРАТОРНАЯ РАБОТА №3
«Изучение кинетики химических реакций»
3130801/20009
Аликберов М.Н.
Дата сдачи: 23.05.23
Опыт 1. «Влияние концентрации реагирующих веществ на скорость гомогенной химической реакции»
Цель: доказательство справедливости закона действующих масс для реакции, протекающей в водном растворе
Na2S2O3 + H2SO4 = Na2SO4 + S + SO2 + H2O
Ход работы:
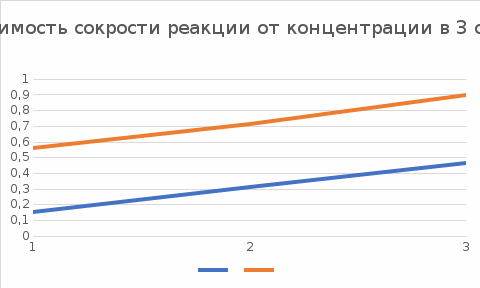
Приготовили 3 раствора тиосульфата натрия Na2S2O3 различной концентрации (количество капель раствора соли и воды указано в таблице 1). Во все пробирки добавили по 1 капле серной кислоты H2SO4. Отмечали время с момента касания капли кислоты поверхности раствора соли до появления опалесценции (помутнения раствора, в частности, побеление). Данные занесли в таблицу 1. По полученным данным на миллиметровой бумаге построен график зависимости условной скорости реакции от начальной концентрации тиосульфата натрия, рассчитана константа скорости для произвольно взятой точки на графики.
| Таблица 1. Зависимость скорости реакции от концентрации реагирующих веществ | ||||||||
| номер пробирки (наблюдения) | число капель Na2S2O3 | число капель H2O | число капель H2SO4 | C(Na2S2O3), моль/л | C(H2SO4), моль/л | время течения реакции ∆τ, с | условная скорость реакции v = 1/∆τ, с-1 | константа скорости реакции, k |
| 1 | 4 | 8 | 1 | 0,154 | 0,077 | 16 | 0,0625 | 0,405844 |
| 2 | 8 | 4 | 1 | 0,308 | 0,077 | 8 | 0,125 | 0,405844 |
| 3 | 12 | 0 | 1 | 0,462 | 0,077 | 5 | 0,2 | 0,4329 |
k (среднее) = 0,415 (округл.)
Вывод:
В результате проведения опыта 1 была установлена прямая зависимость скорости гомогенной реакции химических веществ от начальной концентрации реагирующих веществ. На основании полученных данных был построен график, подтверждающий эту зависимость. Таким образом, чем больше концентрация исходных веществ – тем скорость гомогенной реакции больше, т.е. реакция протекает быстрее (и наоборот). Для каждого из 3-х случаев была посчитана константа скорости, полученные значения приблизительно совпадали – значит, мы экспериментально доказали, что константа скорости не зависит от концентрации реагирующих веществ.