ВУЗ: Национальный исследовательский томский политехнический университет
Категория: Учебное пособие
Дисциплина: Химия
Добавлен: 09.02.2019
Просмотров: 10350
Скачиваний: 59
106
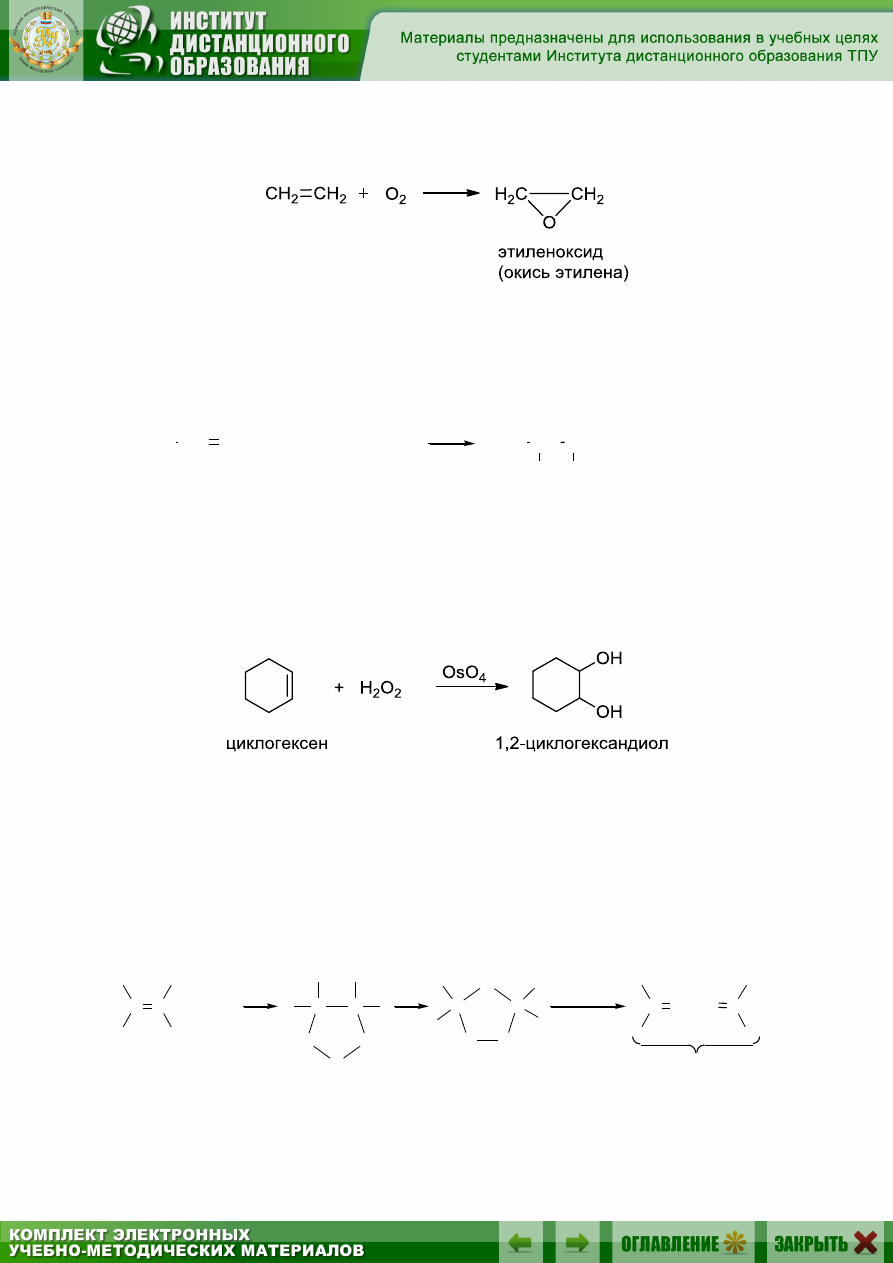
Эпоксиды образуются при окислении олефинов кислородом возду-
ха в присутствии серебряного катализатора:
6.6.10.2. Гидроксилирование. Образование диолов
При взаимодействии алкена с холодным водным раствором пер-
манганата калия образуются диолы (гликоли). Эта реакция имеет назва-
ние – реакция Вагнера (проба Байера):
CH
3
CH CH
2
+ KMnO
4
+ H
2
O
CH
3
CH CH
2
OH OH
+ MnO
2
+ KOH
розовый
бесцветный
Гидроксилирование проводят при комнатной температуре в ней-
тральной или слабощелочной среде. Гидроксилирование алкенов – наи-
более важный метод получения гликолей.
Тот же самый результат достигается при использовании оксида ос-
мия OsO
4
или оксида осмия и пероксида водорода:
6.6.10.3. Озонолиз. Определение структуры алкенов
методом озонирования
Алкены реагируют с озоном О
3
. Реакция протекает в две стадии:
первая – присоединение озона по двойной связи с образованием неус-
тойчивого озонида, вторая – гидролиз озонида с образованием карбо-
нильных соединений как продуктов расщепления:
C C
+
O
3
O
O
O
C
C
O
O
C
O
C
H
2
O, Zn
C
O
C
O
+
- H
2
O
2
альдегиды
и кетоны
мольозонид
озонид
107
Озониды – неустойчивые взрывчатые соединения. Их обрабатыва-
ют водой в присутствии восстановителя, чтобы избежать превращения
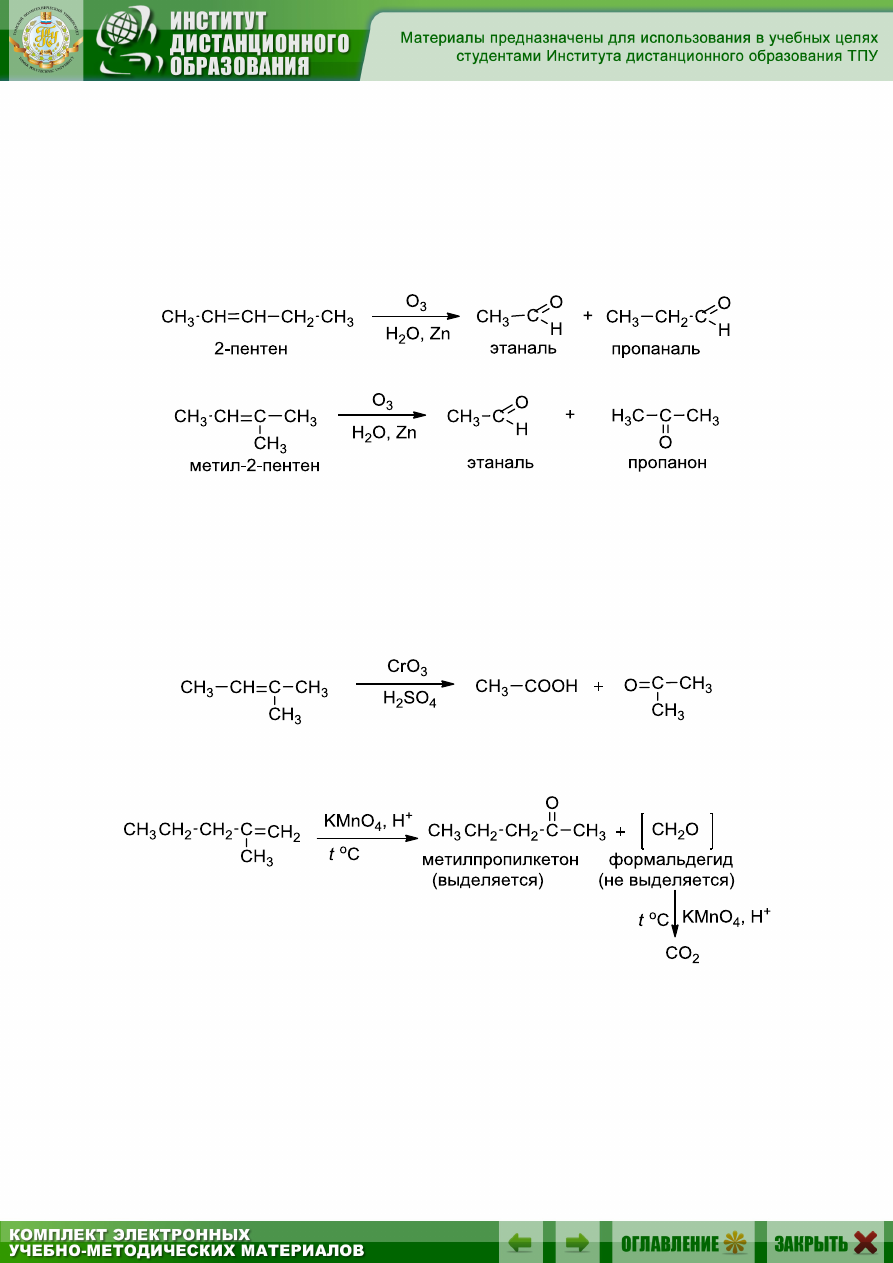
альдегидов в кислоты. Идентифицируя продукты озонолиза, можно ус-
тановить структуру исходного алкена, т.к. кислород оказывается при-
соединенным к атомам углерода, ранее связанным двойной связью. На-
пример, для изомерных пентенов продукты озонолиза различны:
6.6.10.4. Окисление с деструкцией в жестких условиях
При действии концентрированных растворов окислителей (перман-
ганат калия, хромовый ангидрид, хромовая кислота, азотная кислота)
молекула алкена разрывается по месту двойной связи, образуя кетоны
или кислоты:
Концевая группа (═СН
2
) окисляется до СО
2
, например:
Этот метод, как и озонирование, может использоваться для уста-
новления строения алкенов. Однако он менее надежен, поскольку при-
менение концентрированных окислителей, таких как хромовая кислота,
может привести к нежелательным побочным продуктам.

108
6.6.11. Химические тесты на алкены (качественные реакции)
Несмотря на широкое развитие спектральных методов определения
структуры органических соединений, химики до сих пор используют
качественные реакции, позволяющие быстро идентифицировать то или
иное соединение.
В качестве характерной пробы выбирают реакцию, которая
протекает быстро, которую удобно проводить и которая вызывает
легко наблюдаемые изменения – появление или исчезновение окраски,
выделение газа, образование или исчезновение осадка.
Как правило, для проведения качественной реакции требуется не-
сколько минут времени и очень малое количество испытуемого вещества.
Алкены лучше всего идентифицировать по обесцвечиванию рас-
твора брома в четыреххлористом углероде:
или холодного разбавленного раствора перманганата калия (проба Байера):
CH
3
CH CH
2
+ KMnO
4
+ H
2
O
CH
3
CH CH
2
OH OH
+ MnO
2
+ KOH
розовый
бесцветный
Обе реакции легко выполнимы; в первом случае – исчезает красно-
коричневое окрашивание брома, а во втором – исчезает розовое окра-
шивание и появляется бурый осадок двуокиси марганца.
Однако эти пробы не являются абсолютными для алкенов. Обес-
цвечивание раствора брома – тест на любое вещество, способное реаги-
ровать с бромом. Такую реакцию, помимо алкенов, дают алкины
(
С
С
) и альдегиды (
СНО).
Аналогично проба Байера – это проба на любое вещество, реаги-
рующее с MnO
4
-
c образованием MnO
2
. Положительную пробу Байера
дают следующие функциональные группы:
СН=СН
,
СН
СН
,
СНО,
СООН.
Реакция с бромом или перманганатом калия достаточна для того,
чтобы отличить алкен от алкана, алкилгалогенида и спирта. Во всех
других случаях необходимы дополнительные исследования.

109
6.7. Применение алкенов
Алкены применяются в качестве исходных продуктов в производ-
стве полимерных материалов (пластмасс, каучуков, пленок), раствори-
телей, а также многих других важнейших органических веществ.
Этилен в больших количествах выделяют из газов крекинга и кок-
сования и используют ля получения полимеров (полиэтилена, поливи-
нилхлорида, политетрафторэтилена – тефлона), этилового спирта, ук-
сусного альдегида, уксусной кислоты, галогенопроизводных (дихлорэ-
тана, хлороформа и др.), антифриза – этандиола, Применяется как сред-
ство для ускоренного созревания фруктов.
Пропилен также выделяют из промышленных газов и применяют,
в основном, для получения полипропилена (62 % всего выпускаемого
объема). Также из него получают кумол, оксид пропилена, акрилонит-
рил, изопропанол, глицерин и масляный альдегид.
Бутилены применяют для производства бутадиена, изопрена, поли-
изобутилена, бутилкаучука, метилэтилкетона и пр.
Изобутилен является сырьем для получения бутилкаучука, изопре-
на, изооктана и трет-бутанола; используется для алкилирования фено-
лов при синтезе поверхностно-активных веществ (ПАВ). Его сополиме-
ры с бутенами применяют как присадки к маслам и герметики.
Амилены с нормальным строением изомеризуют в изоамилены.
Высшие алкены, содержащие от десяти до восемнадцати атомов
углерода, применяют при синтезе ПАВ, а также для получения высших
спиртов.
110
Глава 7
АЛКАДИЕНЫ
Алкадиены – это углеводороды состава С
n
H
2n-2
, содержащие две
связи С=С. В зависимости от взаимного расположения двойных связей
алкадиены делят на три типа: изолированные, сопряженные и кумули-
рованные.
Если двойные связи разделены в углеродной цепи двумя или более
одинарными связями, то такие двойные связи называются изолирован-
ными, например:
1,4-
пентадиен
Химические свойства алкадиенов с изолированными двойными
связями не отличаются от свойств алкенов с той лишь разницей, что
в реакции могут вступать не одна, а две двойные связи независимо друг
от друга.
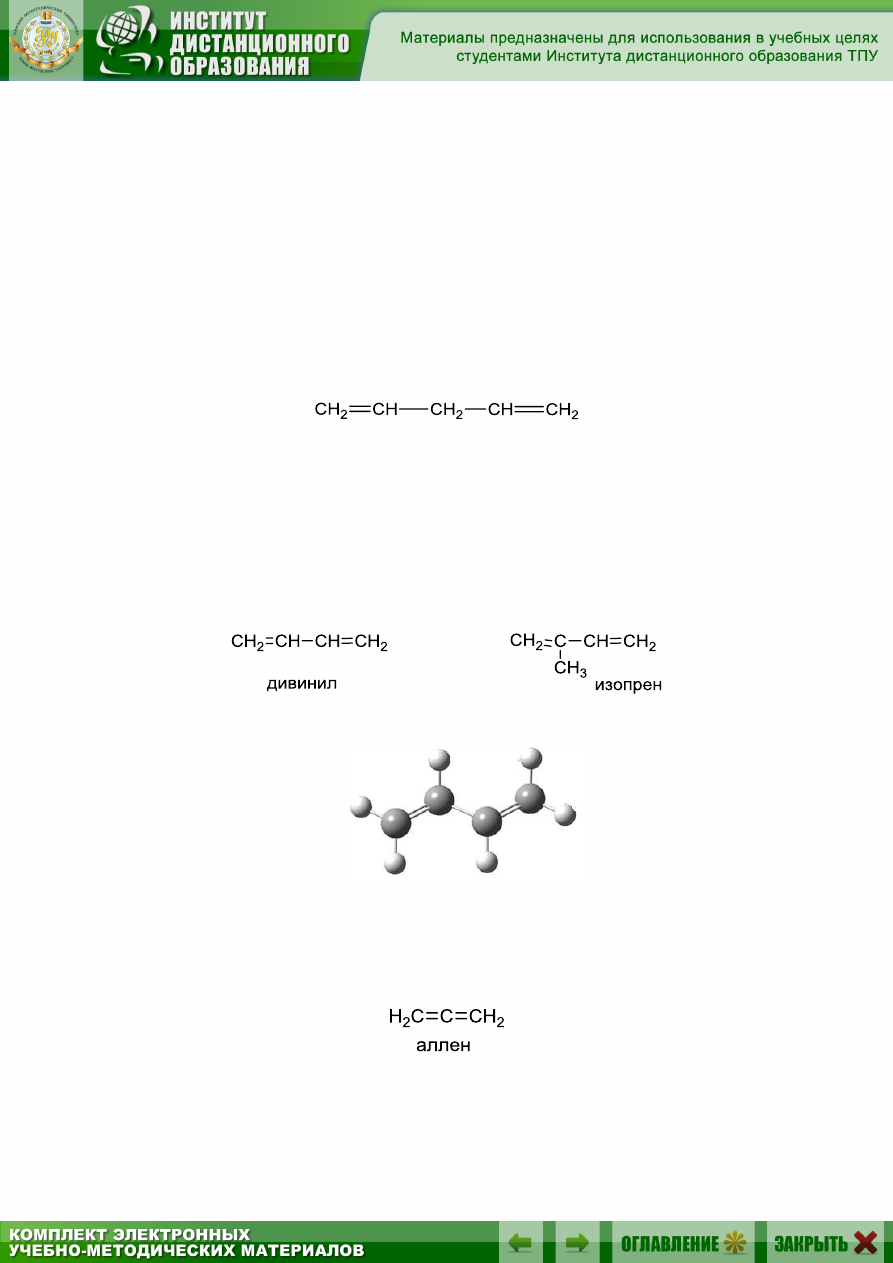
Если двойные связи разделены в цепи только одной
-связью, то их
называют сопряженными. Важнейшие представители сопряженных
диенов:
Модель сопряженного диена – изопрена приведена на рис. 7.1.
Рис. 7.1. Модель молекулы дивинила
(1,3-бутадиена)
Существуют также диены с кумулированными связями (примы-
кающими к одному атому углероду), называемые алленами, например:
Далее рассмотрим только сопряженные диены, имеющие большое
практическое значение.