ВУЗ: Национальный исследовательский томский политехнический университет
Категория: Учебное пособие
Дисциплина: Химия
Добавлен: 09.02.2019
Просмотров: 10351
Скачиваний: 59
111
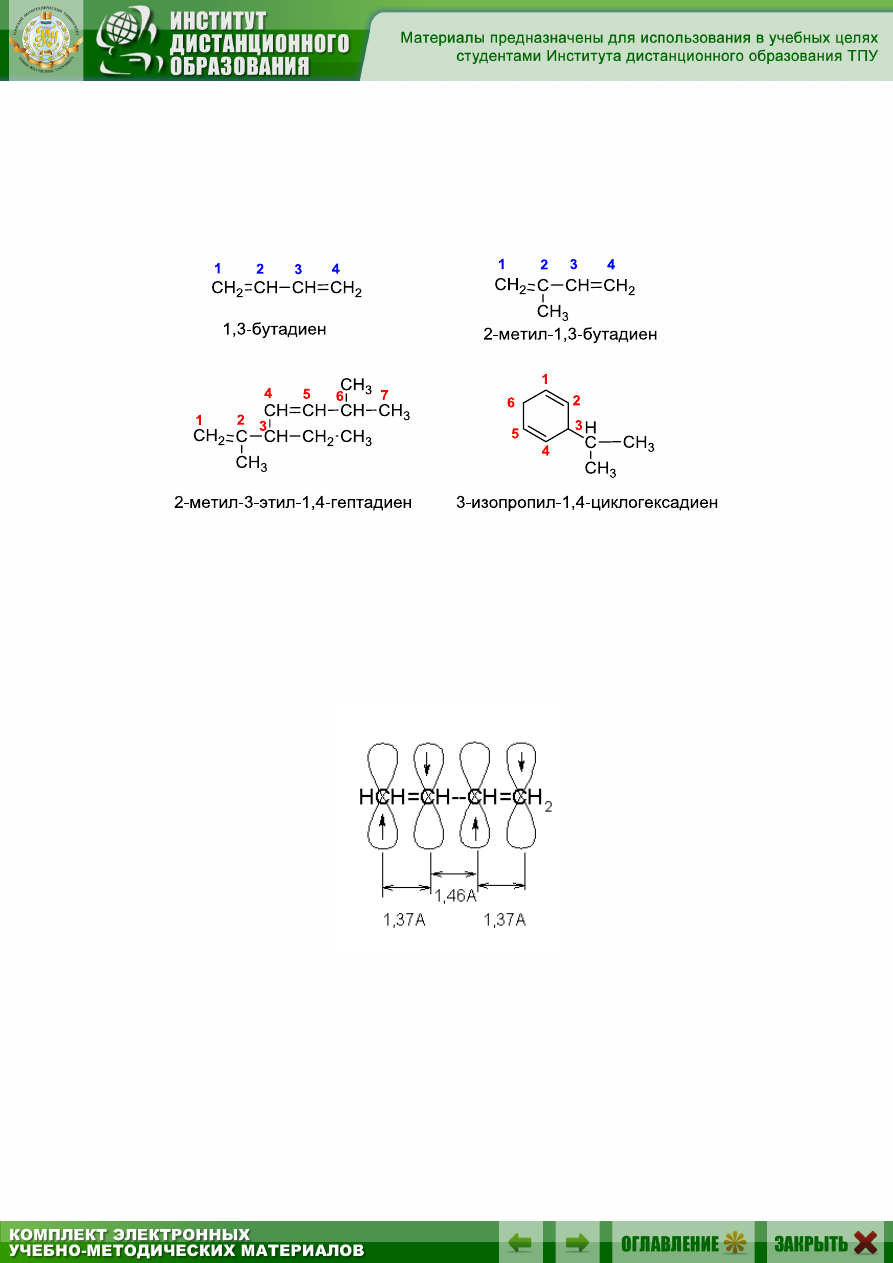
7.1. Номенклатура
Главную цепь в алкадиенах выбирают так, чтобы она содержала
обе двойные связи, и нумеруют с того конца, при котором сумма номе-
ров положений двойных связей минимальна. В названии соответствую-
щего алкана окончание -ан заменяется на -диен.
7.2. Строение сопряженных диенов
В сопряженных диенах
-электронные облака двойных связей пе-
рекрываются между собой и образуют единое
-электронное облако.
В сопряженной системе
-электроны уже не принадлежат определенным
связям, они делокализованы по всем атомам, поэтому структуру диенов
можно изобразить на примере 1,3-бутадиена следующим образом:
Рис. 7.2. Строение 1,3-бутадиена
Установлено, что двойные связи в молекуле 1,3-бутадиена (C
1
–C
2
и С
3
–С
4
) (рис. 7.2) несколько длиннее (0,136 нм), чем двойная связь
в этилене (0,134 нм). Простая же связь (С
2
–С
3
), расположенная между дву-
мя двойными связями, короче обычной s-связи (0,146 нм в 1,3-бутадиене
112
и 0,154 нм в этане). Причина такого «выравнивания» длин углерод-
углеродных связей в дивиниле состоит в том, что 2р-орбитали всех четы-
рех углеродных атомов перекрываются между собой (правда, это пере-
крывание между C
2
и С
3
несколько меньше) с образованием единой мо-
лекулярной орбитали с равномерным по своей молекуле p-электронным
облаком.
Взаимодействие двух соседних p-связей способствует процессу
взаимного влияния атомов в такой системе (эффект сопряжения). Это
приводит к снижению общей энергии молекулы, и в результате повы-
шается ее устойчивость. В то же время, молекула дивинила при химиче-
ских реакциях ведет себя намного активнее, чем обычный алкен. Осо-
бенно это проявляется в реакциях присоединения.
7.3. Физические свойства
1,3-Бутадиен – легко сжижающийся газ с неприятным запахом.
Изопрен – жидкость с Т
кип
34 °С. Аллен (1,2-пропадиен) – газ. По срав-
нению с алканами и алкенами диены имеют большие значения показа-
теля преломления.
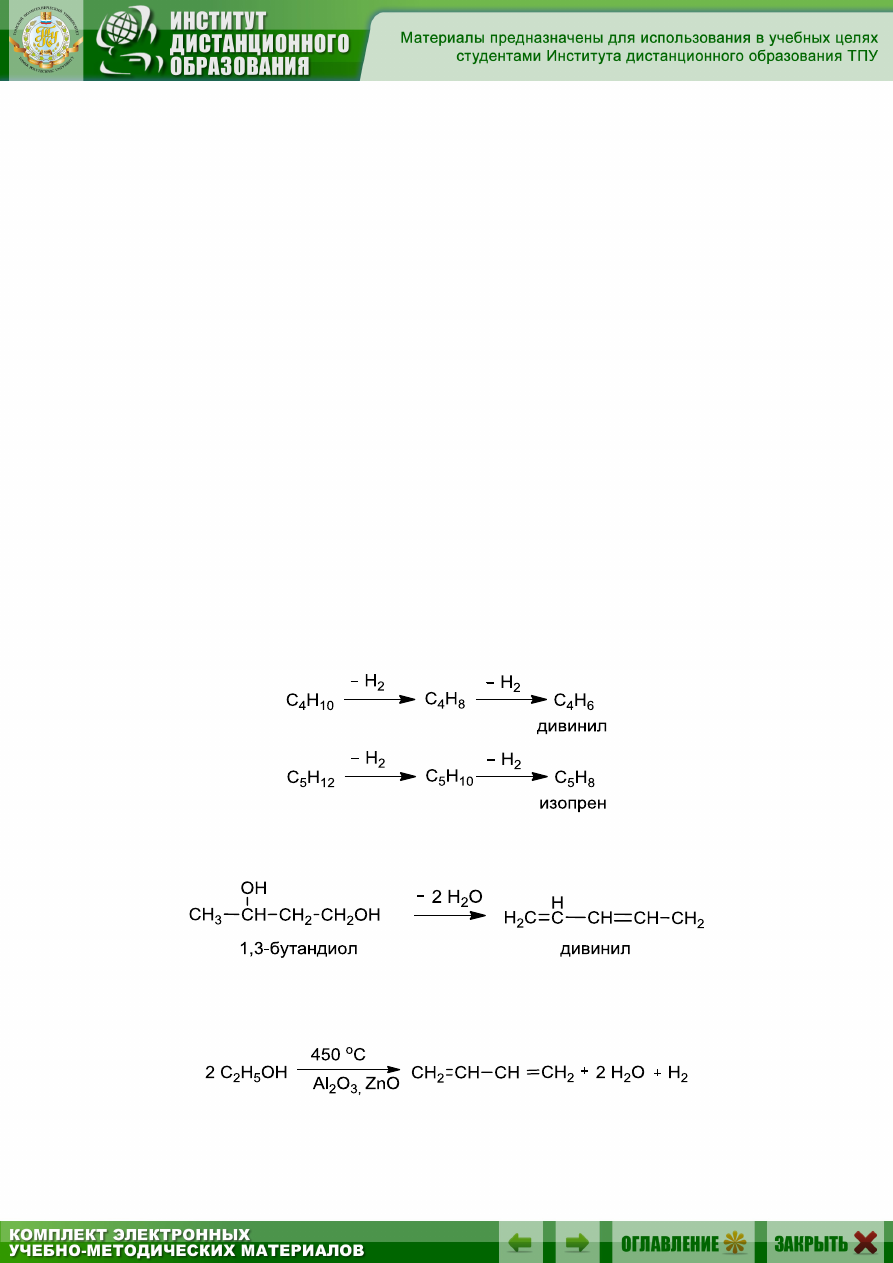
7.4. Способы получения сопряженных диенов
1. Дегидрирование алканов и алкенов (разд. 7.4.1):
2. Дегидратация двухатомных спиртов (гликолей или пинаконов)
(разд. 7.4.2):
3. Дегидратация и дегидрирование этанола (метод С.В. Лебедева)
(разд. 7.4.3):
113
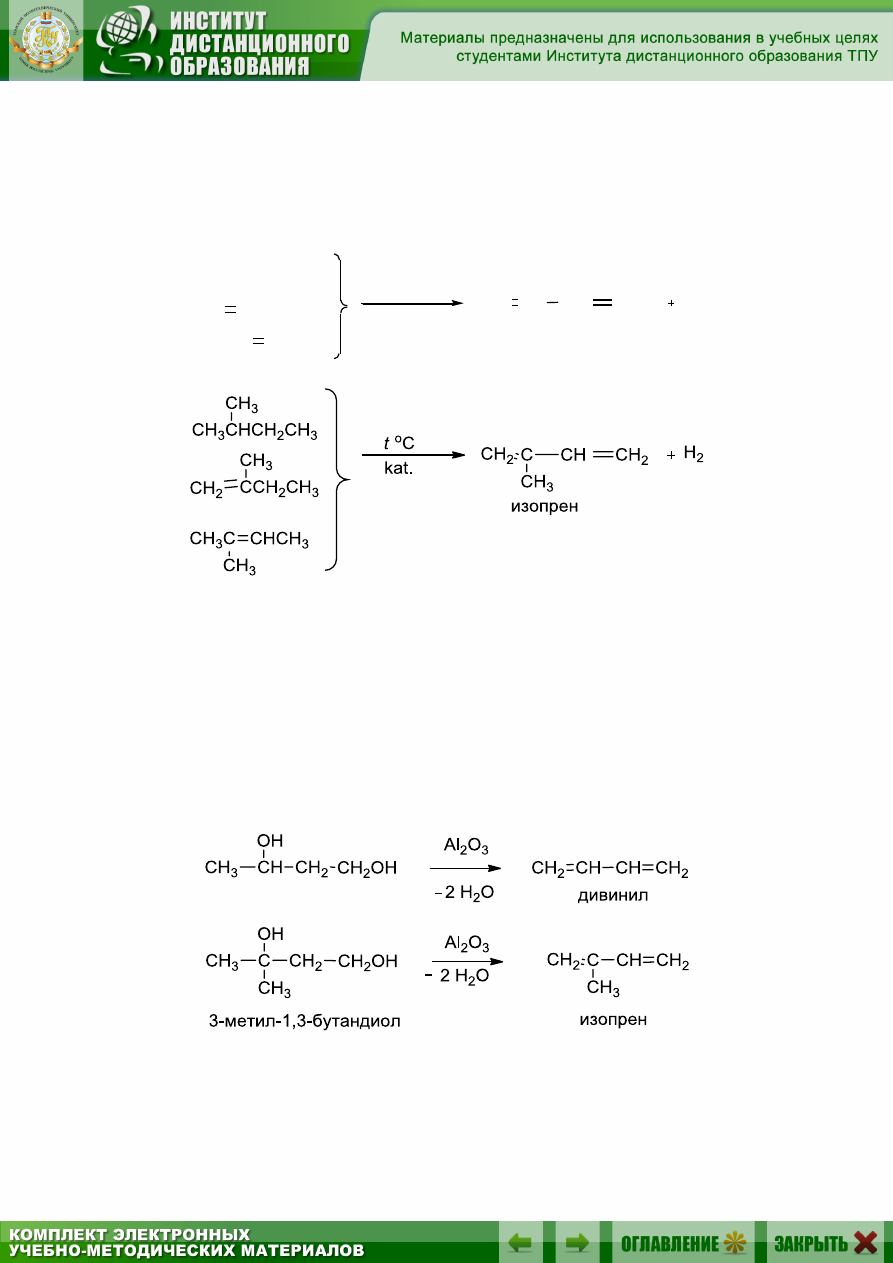
7.4.1. Дегидрирование алканов и алкенов
Основным промышленным способом получения дивинила и изо-
прена является дегидрирование соответствующих бутан-бутиленовых
или изопентан-амиленовых смесей над катализатором (Сr
2
O
3
):
CH
2
CH CH
CH
2
CH
3
CH
2
CH
2
CH
3
CH
2
CHCH
2
CH
3
CH
3
CH CHCH
3
Cr
2
O
3
H
2
650
o
C
Исходные вещества выделяют из нефти путем фракционной пере-
гонки или из попутных газов.
7.4.2. Дегидратация двухатомных спиртов
(гликолей или пинаконов)
Дивинил, изопрен в промышленных масштабах получают дегидра-
тацией гликолей:
114
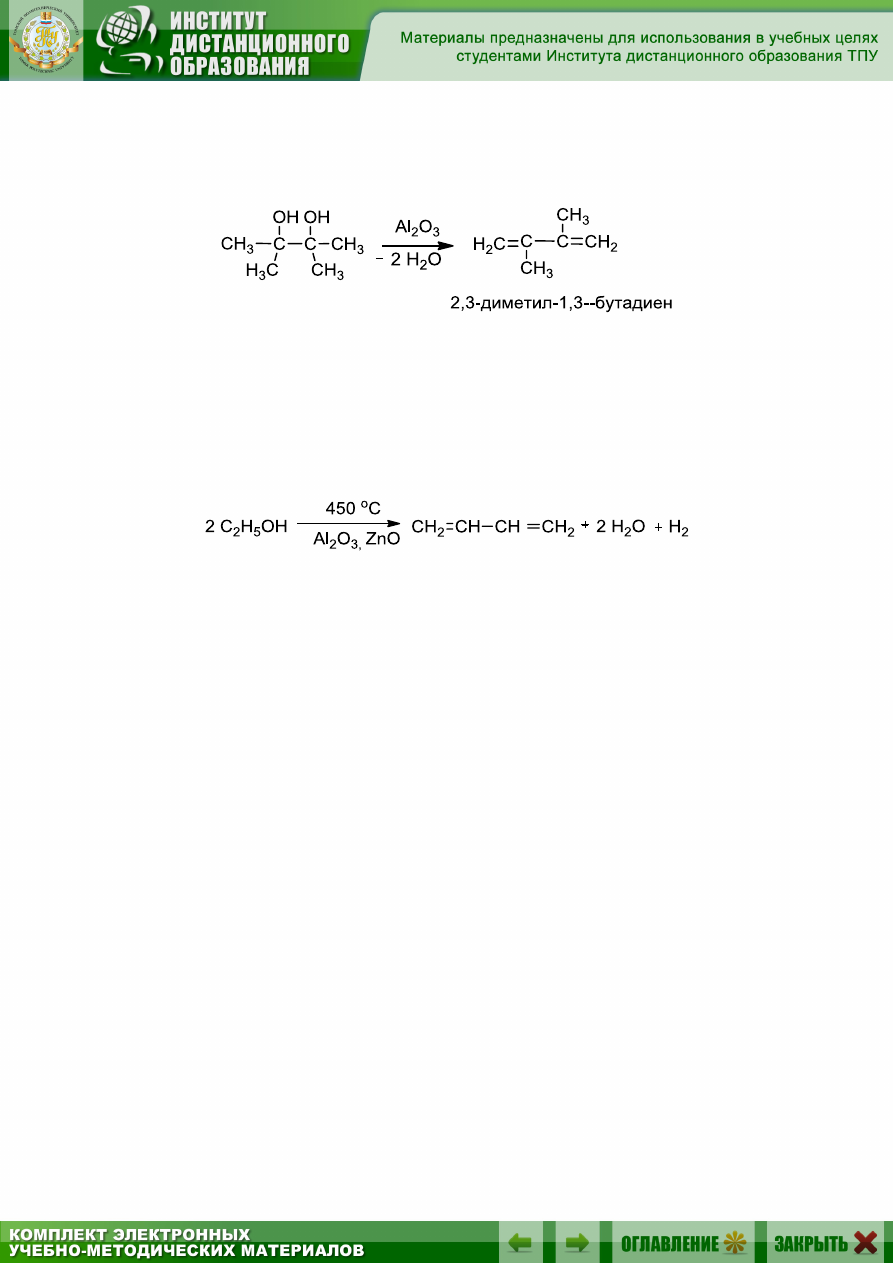
При дегидратации пинаконов (дитретичные гликоли) в присутст-
вии оксида алюминия образуются замещенные сопряженные диеновые
углеводороды:
7.4.3. Дегидратация и дегидрирование этанола
Этот одностадийный способ получения дивинила разработал совет-
ский химик, академик Лебедев Сергей Васильевич в 1926–1928 гг.
Реакция Лебедева протекает при повышенной температуре в присутст-
вии цинк-алюминиевого катализатора:
Реакция включает следующие стадии: дегидрирование спирта до
альдегида, альдольную конденсацию альдегида, восстановление альдо-
ля до диола и его дегидратацию.
С 1932 г. благодаря реакции Лебедева и его работам по получению
каучуков и резины в СССР начали получать синтетический каучук
в промышленном масштабе.
7.5. Химические свойства сопряженных диенов
Для сопряженных диенов известны все реакции, характерные для
алкенов. Однако их поведение отличает ряд особенностей. Особенность
сопряженных диенов состоит в том, что две двойные связи в их молеку-
лах функционируют как единое целое, поэтому реакции присоединения
могут протекать в двух направлениях: а) к одной из двойных связей
(1,2-присоединение) или б) в крайние положения сопряженной системы
с образованием новой двойной связи в центре системы (1,4-присоединение).
В реакциях электрофильного присоединения А
E
сопряженные дие-
ны более активны, чем алкены, т.к. реакции присоединения к ним элек-
трофилов протекают через образование термодинамически стабильных
карбокатионов аллильного типа:
115
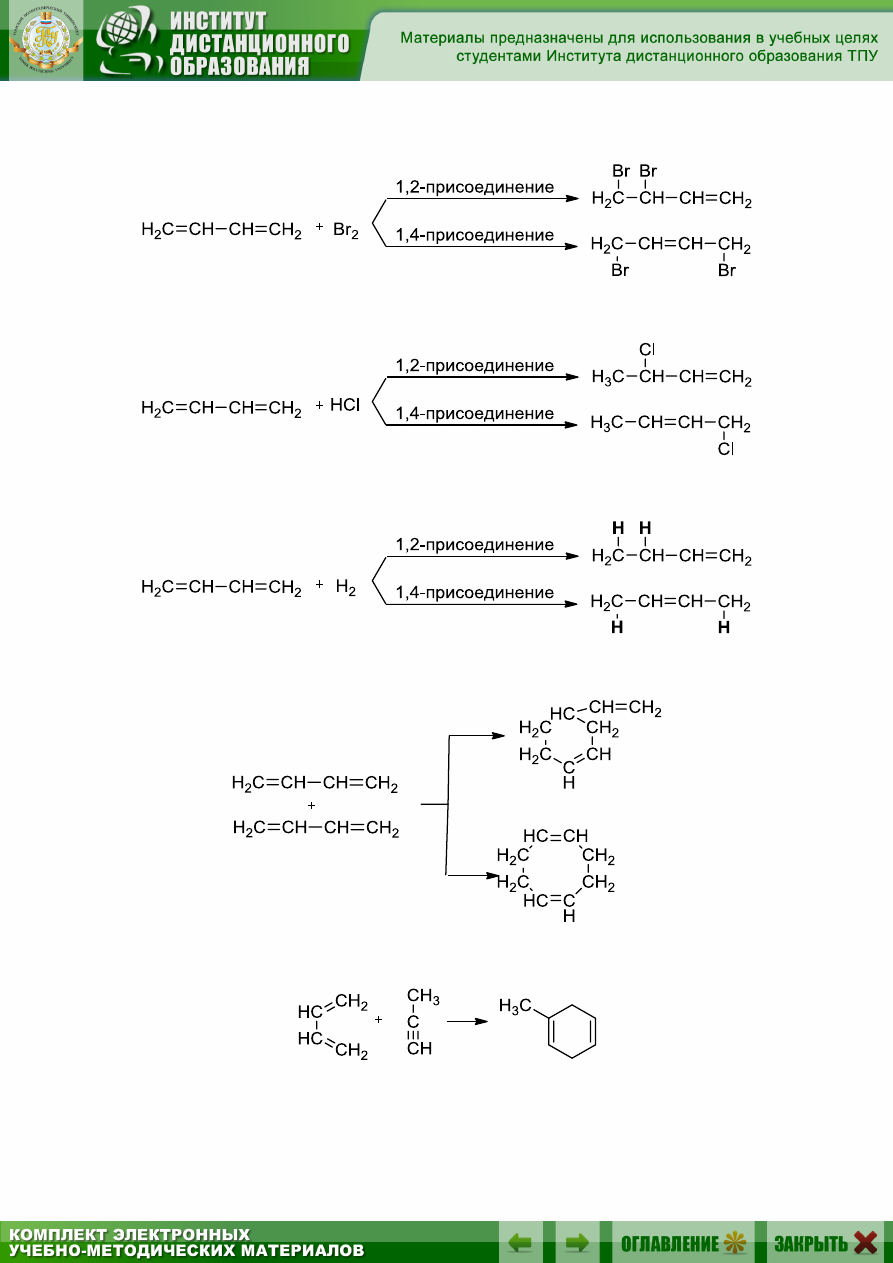
1. Галогенирование (разд. 7.5.1):
2. Гидрогалогенирование (разд. 7.5.2):
3. Гидрирование (разд. 7.5.3):
4. Димеризация (разд. 7.5.4):
4. Диеновый синтез (реакция Дильса – Альдера) (разд. 7.5.5):