Файл: Учебное пособие по химии для учащихся 10 классов, обучающихся в лицеях фдп рниму под редакцией проф. Теплова В. В.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.01.2024
Просмотров: 1205
Скачиваний: 9
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
262. При обработке одноатомного спирта металлическим натрием образовался алкоголят, в котором массовая доля натрия равна 23,96%. Назовите спирт.
263. При обработке 83г смеси пропанола и этанола металлическим натрием выделилось 16,8л(н.у.) водорода. Рассчитайте массовую долю спиртов в исходной смеси.
264. При сжигании 31,4г смеси этанола и бутанола образовалось 35,84л(н.у.) углекислого газа. Рассчитайте массовую долю спиртов в исходной смеси.
265. 18г одноатомного спирта обработали избытком натрия, при этом выделился водород в количестве, достаточном для полного гидрирования 1,68л(н.у.) бутадиена-1,3. Назовите исходный спирт.
266. В 200мл этанола (плотность равна 0,8г/мл) растворили такое количество натрия, что массовая доля алкоголята стала равна 17,7%. Рассчитайте массу растворённого натрия.
267. 250 мл этанола(плотность 0,8г/мл), в котором массовая доля воды равна 4,5%, прореагировало с избытком натрия. Рассчитайте объём выделившегося водорода.
268. 4,6г натрия растворили в 200мл этанола (плотность равна 0,8г/мл).Рассчитайте массовую долю алкоголята натрия в спиртовом растворе.
269. При дегидратации предельного одноатомного спирта и последующим взаимодействии с бромом образовавшегося алкена было получено 20,2г дибромида. При действии избытка натрия на такое же количество спирта выделяется 1,12л(н.у.) водорода. Назовите исходный спирт.
270. При дегидратации 9,25г предельного одноатомного спирта образовался алкен, объём которого в 4 раза меньше объёма углекислого газа, образующегося при сжигании такого же количества спирта. Назовите исходный спирт.
271. При дегидратации предельного одноатомного первичного спирта с разветвлённым углеродным скелетом образовался алкен, который смешали с равным объёмом азота. Плотность полученной газовой смеси стала равна плотности пропена при тех же условиях. Установите строение спирта.
272. При взаимодействии предельного одноатомного спирта с бромоводородом образовалось соединение, в котором массовая доля брома равна 73,4%. Назовите спирт.
273. Дегидратацией некоторого количества одноатомного предельного спирта получен алкен. Половина образовавшегося газа может обесцветить 120г 20% раствора брома в CCl4 , а при сожжении второй половины газа образуется 10,08л(н.у.) углекислого газа. Какой спирт и в каком количестве был подвергнут дегидратации?
274. При нагревании 23г этанола с небольшим количеством концентрированной серной кислоты образовался газ и легкокипящая жидкость. Газ может обесцветить 40г 40% раствора брома в CCl
4. Какие соединения и в каком количестве образовались?
275. При дегидратации предельного одноатомного спирта и последующем взаимодействии с хлором было получено 59,4г дихлорида. При действии на такое же количество спирта избытком натрия выделяется 6,72л(н.у.) водорода. Каково строение исходного спирта?
276. В 50 мл метанола(плотность равна 0,79г/мл) растворили столько лития, что массовая доля алкоголята стала равна 36,28%. К этому раствору добавили 20мл воды и пропустили 6,72л(н.у.) углекислого газа. Рассчитайте массовые доли веществ в конечной смеси.
277. Какой одноатомный спирт взят для реакции, если при взаимодействии 72г этого спирта с избытком натрия выделился водород в количестве, достаточном для полного гидрирования 6,72л(н.у.) пропина.
278. Какое- то количество алкена присоединило 8,96л(н.у.) бромоводорода. При гидролизе полученного продукта водным раствором гидроксида натрия образовалось 29,6г одноатомного спирта с положением гидроксильной группы у третичного атома. Каково строение алкена и спирта?
279. При межмолекулярной дегидратации некоторого количества одноатомного спирта образовалось 55,5г простого эфира, а при внутримолекулярной дегидратации такого количества спирта образовалось 33,6л(н.у.) алкена. Определите формулу исходного спирта.
280. Предельный одноатомный спирт дегидратировали, в результате образовался алкен, объём которого в три раза меньше объёма углекислого газа, образующегося при сгорании такого же количества спирта. Полученный алкен обесцвечивает 120г 20% раствора брома в CCl4 . Определите спирт.
281. При дегидратации предельного одноатомного спирта и последующей обработке алкена бромоводородом получили 12,3г бромпроизводного, при обработке которого водным раствором гидроксида натрия получили 6г изомера исходного спирта. Определите структурную формулу исходного спирта.
282. Некоторое количество алкена присоединило 58,24л(н.у.) бромоводорода. При обработке полученного продукта водным раствором гидроксида натрия образовалось 156г предельного одноатомного спирта. Определите строение исходного углеводорода и полученного спирта.
283. При обработке смеси стирола и этанола избытком натрия выделилось 2,24л(н.у.) газа. Такая же масса смеси полностью прореагировала со 100г 4% раствора брома в CCl4. Определите массу исходной смеси.
284. При дегидратации одноатомного спирта и последующим взаимодействии с бромом образовавшегося алкена получили 101г дибромида. При действии на такое же количество спирта избытком натрия выделилось 5,6л(н.у.) газа. Рассчитайте массу исходного спирта.
285. При обработке 14,4г двухатомного спирта избытком калия выделилось 3,584л(н.у).газа. Назовите спирт.
286. При обработке некоторого количества двухатомного спирта избытком натрия выделилось 2,24л(н.у.) газа, а при сжигании такого же количества спирта выделилось 6,72л(н.у.) углекислого газа. Назовите спирт.
287. При сжигании 16,6г смеси пропандиола-1,2 и бутандиола-1,2 выделилось 15,68л(н.у.) углекислого газа. Рассчитайте массовые доли спиртов в исходной смеси.
288. 15,4г смеси этанола и этандиола-1,2.обработали избытком натрия, при этом выделилось 4,48л(н.у.) водорода. Рассчитайте состав исходной смеси в %% по массе.
289. При действии на смесь метанола и пропандиола-1,2 избытком натрия выделилось 12,32л(н.у.) газа, а при сжигании такого же количества смеси образовалось 33,6л(н.у.) углекислого газа. Рассчитайте состав смеси в %% по массе.
290. При реакции избытка натрия с 23,8г смеси бутанола-2 и насыщенного двухатомного спирта выделилось 4,48л(н.у.) газа. При сжигании такой же массы смеси в избытке кислорода образовалось 27г воды. Назовите спирт.
291. Двухатомный спирт массой 7,44г обработали равномолекулярным количеством хлороводорода, при этом образовалось соединение массой 9,66г, в молекуле которого содержится по одному атому кислорода и хлора. Назовите спирт.
292. Два двухатомных спирта являются ближайшими гомологами. При сжигании 16,6г равномолекулярной смеси этих спиртов выделилось 15,68л(н.у.) углекислого газа. Определите формулы спиртов и рассчитайте их количества.
293. При обработке 56,4г смеси этанола и пропандиола-1,2 избытком натрия выделился водород, в количестве достаточном для полного гидрирования 0,5 моль смеси этена и этина с плотностью по водороду 13,6. Определите состав исходной смеси в %% по массе.
Глава 9. ФЕНОЛЫ
Фенол – соединение, содержащее гидроксильную группу, которая непосредственно связана с атомом углерода ароматического кольца.
Фенол, а также о-, м- и п- метилфенолы(крезолы) содержатся в каменноуголной смоле.
3-метил-6-изопропилфенол(тимол) и изомерный ему
2-метил-5-изопропилфенол (корвалол) входят в состав душистых масел чабреца и тмина.
Фенолы и многоатомные фенолы в виде различных производных применяются в медицине парфюмерии ( таннин, ванилин, антиоксиданты, дезинфицирующие средства).
Фенолы представляют собой твёрдые кристаллические вещества с резким характерным запахом. Они плохо растворимы в воде, хорошо-
в спирте и эфире.
9.1. Получение фенола
1. Кумольный способ
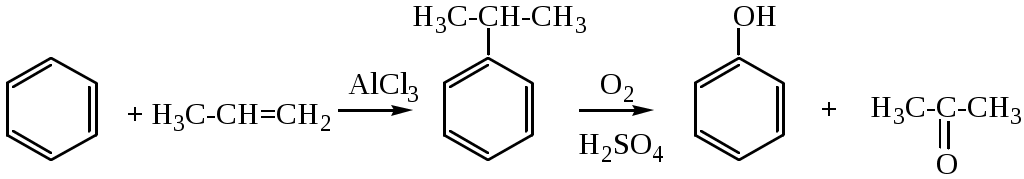
2. Из ароматических галоидных соединений
а) Действие едких щелочей при нагревании в присутствии тонкого порошка меди
C6H5Cl + NaOH
б) Парофазный каталитический гидролиз хлорбензола.
3. Из каменноугольной смолы
Каменноугольную смолу обрабатываю раствором щелочи и выделяют фенолы из полученных продуктов кислотой:
C6H5OH + NaOH
2C6H5ONa + H2SO4
4. Из ароматических сульфокислот
C6H6 + HO-SO3H
бензолсульфокислота
Далее бензолсульфокислоту сплавляют с гидроксидом натрия
C6H5-SO3H + 3NaOH
Далее: C6H5ONa + HCl
9.2. Химические свойства фенолов
Химическое поведение фенолов связано с наличием в их молекуле гидроксильной группы и ароматического ядра. Они вступают практически во все реакции, характерные для них.
.В то же время имеется ряд особенностей связанных с взаимным влиянием гидроксильной группы и бензольного ядра.
1. Кислотные свойства
В связи с тем, что неподелённая электронная пара атома кислорода гидроксильной группы вступает во взаимодействие с π – электронами бензольного ядра, электронная плотность смещается в сторону бензольного ядра(+М-эффект), на последнем возникает дефицит электронной плотности и атом водорода приобретает большую подвижность.
По этой причине фенол является слабой кислотой
а) В водных растворах диссоциируют по кислотному типу:
C6H5OH = C6H5O- + H+
б) Реакция с активными металлами.
2C6H5OH + 2Na
2C6H5ONa + H2
в) В отличие от спиртов растворяется (как и другие фенолы ) в водных растворах щелочи, образуя феноляты

C6H5OH + NaOH = C6H5ONa + H2O
Феноляты, будучи солями слабых кислот, частично гидролизованы в водном растворе, который поэтому обладает щелочной реакцией.
Фенолы можно выделить из фенолятов подкислением даже такими слабыми кислотами как угольная: C6H5ONa + H2O + CO2 = C6H5OH + NaHCO3
2. Реакции электрофильного замещения в бензольном кольце
а) При взаимодействии с бромной водой образуется 2, 4, 6, - трибромфенол, так как кислород гидроксигруппы сопрягается с двойной связью бензольного кольца и в орто- и пара- положениях увеличивается электроотрицательность. Наблюдается обесцвечивание бромной воды и выпадение белого творожистого осадка( качественная реакция).
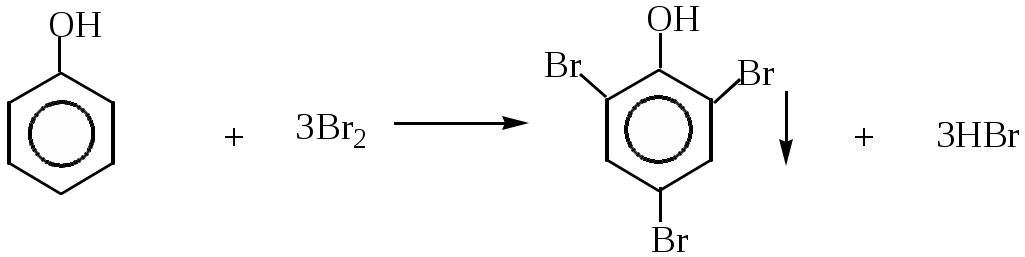
б) При нитровании фенола концентрированной азотной кислотой образуется 2,4,6-тринитрофенол(пикриновая кислота). Благодаря наличию
трёх групп –NO2 связь О-Н ещё больше поляризуется и кислотные свойства усиливаются.
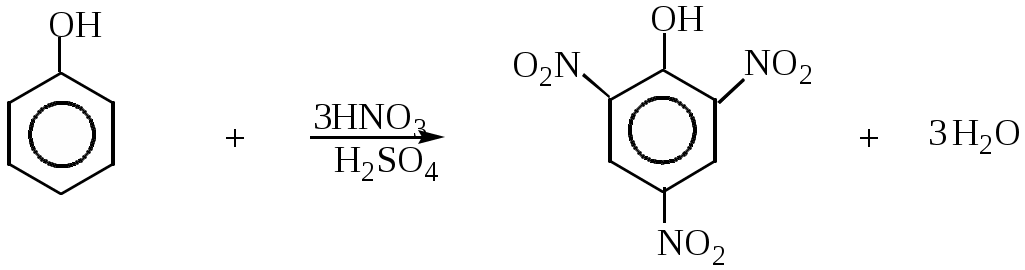
2,4,6-тринитрофенол
При нитровании фенола разбавленной азотной кислотой образуется смесь ортонитрофенола и паранитрофенола.
3. Окислительно-восстановительные реакции
а) Окисление
Фенолы( особеннои многоатомные фенолы) легко окисляются, давая многообразные продукты окисления. Лёгкая окисляемость позволяет использовать их в качестве антиоксидантов.
Антиокислительные свойства фенолов связаны с их способностью реагировать с пероксидными радикалами RO2• , ведущими цепь окисления, с образованием в результате этого малоактивных радикалов, не способных продолжать окисление:
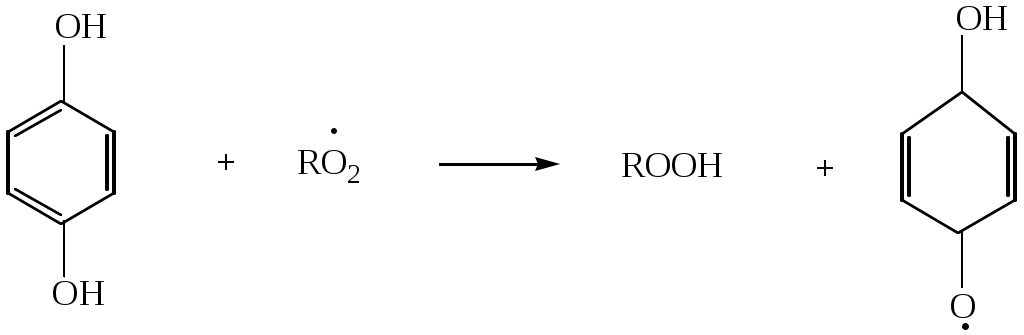 гидрохинон пероксидный радикал
гидрохинон пероксидный радикал 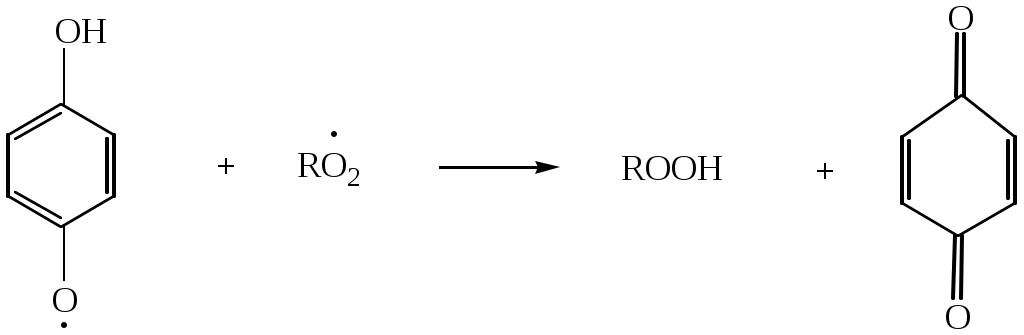
хинон
б) Восстановление
Ni, 150oC
C6H5OH + 3H2
При действии Li[AlH4] при 350оС фенол восстанавливается в бензол