Файл: Учебное пособие по химии для учащихся 10 классов, обучающихся в лицеях фдп рниму под редакцией проф. Теплова В. В.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.01.2024
Просмотров: 1188
Скачиваний: 9
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Было: 10л 10л
2СО + О2 = 2СО2 + [ O2 ]
Прореагировало: 10л 5л стало 10л 5л
Запишем эти данные для удобства в виде таблицы:
| Вещества | Было V(л) | Прореаг. V(л) | Стало V (л) |
| СО | 10 | 10 | - |
| О2 | 10 | 5 | 5 |
| СО2 | - | - | 10 |
| ∑ (V) | 20 | 15 | 15 |
3) Определим состав полученной газовой смеси:
V(CO2) V(CO2) 10
φ (CO2) = ─────── = ────────── = ──── = 0,6667
V(газ.смеси) V(CO2) + V(O2) 10 + 5
V(O2) 5 1
φ(O2) = ──────── = ─── = ── = 0,3333
V(газ.смеси) 15 3
4) Найдем массу образовавшегося СО2:
V(CO2) 10
m(CO2) = n(CO2) ∙ M(CO2) = ─────── ∙ M(CO2) = ─── ∙ 44 = 19,64(г)
Vm 22,4
Ответ: m(СО2) = 19,64 г ; φ(СО2) = 0,6667; φ(О2) = 0,3333.
1.2.Задачи и упражнения для самостоятельного решения
1. Вычислите массу следующих количеств вещества:а) 1 моль атомов азота;б) 3 моль атомов кислорода;в) 0,2 кмоль атомов меди ;г) 0,3 кмоль воды ; д)0,1 моль аммиака;ж) 0,01 кмоль этана.
2. Сколько моль атомов содержится в :а) 4 г кислорода; б)10 г водорода; в)1,2 кг углерода ;г) 18 г воды;д) 4 г гидроксида натрия; ж)16 мг метана; з)4,4 г пропана;и) 8,8 кг углекислого газа?
3. В какой массе серной кислоты содержится столько же вещества, сколько содержится :а) в 4 мг гидроксида натрия;б) в 4.4 кг углекислого газа;в) в 2,12 г карбоната натрия;г) в 12 г этана?
4. Какой объем при н.у. займут:а) 0,5 моль водорода; б) 0,5 моль гелия; в)0,5моль воды;г) 0,5кмоль атомов хлора;д) 100 ммоль атомов кислорода?
5. Рассчитайте объем, который при н.у. займет газовая смесь, состоящая из 2,73 моль азота, 3,82 моль водорода, 0,45 моль оксида углерода (II) и 3,00 моль оксида углерода (IV).
6. Рассчитайте массу (при н.у.): а)1,12 л азота;б) 7,84 мл пропана;
в) 0,336 м3 кислорода.
7. Рассчитайте массу газовой смеси, состоящей из 8,96л (н.у.) оксида углерода (II) и 4,48л (н.у.) оксида углерода (IV).
8. Рассчитайте массу 22,4 л (н.у.) смеси газов, содержащей ( в %% по объему): 40% азота, 10% оксида углерода (II) и 50% этена.
9. Определите объем, который при н.у. занимают:а) 1кг водорода;
б) 11 г углекислого газа;в) 16 т метана.
10. Определите объем, который при н.у. занимает:а) 12,04 ∙ 1024 молекул водорода;б) 3,01∙1023 молекул метана.
11. Сравните число молекул:а) в 1г водорода и 1г кислорода;
б)в 1л водорода и 1л кислорода;в) в 1моль водорода и 1моль кислорода.
12. Вычислите молярную массу газа , а)если масса 1л газа (н.у.) равна 1,25г;б)если масса 300 мл газа (н.у.) равна 0,857 г. Предложите возможные формулы газов.
13. Определите массу этана, в которой содержится 12,04∙1023 молекул.
14. В каком соотношении по объему следует смешать метан и этан, чтобы масса 1л газовой смеси была равна 1,0 г?
15. Сколько электронов содержится в 0,2 моль метана?
16. В каком объеме метана (н.у.) содержится столько электронов, сколько содержится в 5,6 г железа?
17. Определите относительную плотность по водороду и по воздуху: а)азота; б)хлора;в) метана.
18. Вычислите плотность при н.у.: а)этана;б) бутана.
19. Вычислите плотность и относительную плотность по воздуху газовой смеси, состоящей (в %% по объему) из водорода(20%), метана (50%), пропана (30%).
20. Вычислите среднюю молярную массу и относительную плотность по водороду газовой смеси, состоящей (в %% по объему) из углекислого газа (20%), метана (40%) и водорода (40%).
21. Определите состав газовой смеси (в %% по объему), содержащей метан и этан, если ее относительная плотность по водороду равна 9,4.
22. Определите состав газовой смеси, состоящей из метана и этана, если массовая доля водорода как элемента в ней равна 22%.
23. Определите относительную плотность по воздуху газовой смеси, состоящей из (в %% по массе): 20% водорода, 10% углекислого газа, 40% азота, 20% метана и 10% этана . Какой объем воздуха необходим для сжигания 1л такой смеси?
24. Газовая смесь, состоящая из воздуха и метана, имеет плотность по кислороду 0,82. Определите состав этой смеси в массовых долях, считая что в воздухе содержится 20% кислорода(по объёму).
25. В каком соотношении по объёму следует смешать углекислый газ и пропан, чтобы плотность газовой смеси была равна 1,964 г/л ?
26. В каком соотношении по массе следует смешать азот и этен, чтобы плотность по гелию газовой смеси была равна 7?
27. Рассчитайте массовую долю пропана в смеси с этаном, если её плотность по водороду равна 20. Какой объем воздуха необходим для сжигания 10 л такой смеси, считая, что в воздухе содержится 20% кислорода по объему?
28. Как изменится давление газовой смеси, находящейся с замкнутом сосуде и состоящей из равных объёмов кислорода и СО, если: а) весь оксид углерода (II) превратится в углекислый газ; б) половина оксида углерода (II) превратится в углекислый газ?
29. После сжигания 120 мл(н.у.) смеси водорода с кислородом объём газовой смеси, измеренной при нормальных условиях, уменьшился в два раза. Определите содержание водорода в исходной газовой смеси(в %%) по объёму, если водород сгорел полностью.
30. Рассчитайте массу воды, которая может образоваться при сжигании смесей, состоящих из: а) 10г Н2 и 10г О2; б) 10л(н.у.) Н2 и 10л(н.у.) О2; в) 10г Н2 и 10л(н.у.)О2; г) 10л(н.у) Н2 и 10г О2
.
31. Какой объём воздуха (при нормальных условиях)) необходим для полного сжигания 100г газовой смеси, состоящей (в %% по объёму): 20% СО2 ,10% СО, 30% N2 и 40%H2? Содержание кислорода в воздухе принять равным 21% по объему.
32. Определите молекулярную формулу вещества содержащего углерод (ω = 84,21%) и водород (ω =15,79%). Плотность паров этого вещества по воздуху равна 3,93.
33. Определите формулу вещества, состоящего из углерода, водорода и кислорода, если при сжигании 2,9 г его получено 6,6 г углекислого газа и 2,7г воды. Плотность паров этого вещества при (н.у.) равна 2,59г/л.
Глава 2. АЛКАНЫ
Общая формула гомологического ряда алканов CnH2n+2 .Метан, этан, пропан и бутан в обычных условиях (25 0С и 101 кПа) - газы. Углеводороды с содержанием атомов углерода от 5 до15- жидкости, остальные алканы - твердые вещества. Газообразные алканы не имеют запаха и цвета. Алканы хорошо растворяются в неполярных органических растворителях и не растворяются в воде.
2.1.Получение алканов
1. Основной источник углеводородов - природные газы и нефть. В промышленности углеводороды получают перегонкой нефтепродуктов.
2. Каталитическое гидрирование (Ni, Pd, Pt) ненасыщенных углеводородов при нагревании:
СН2=СН2 + Н2
3. По реакции Вюрца, действуя натрием на галогеналканы при нагревании
CH3−CH2Cl + ClCH2−CH3 + 2 Na
бутан
2 CH3− CH−CH3 + 2 Na
| |
Br CH3−CH−CH3
2,3-диметилбутан
Cl CH3
| |
CH3−Cl + CH3− CH−CH3 + 2 Na
изобутан
4. Гидролиз карбидов
Al4C3 + 12 H2 O
Be2C + 4 H2 O
5. Декарбоксилирование солей низших карбоновых кислот
(для газообразных углеводородов)
t0
CH3COONa + NaOH
тв тв
t0
CH3 CH 2COOK + KOH
тв тв
2.2 Химические свойства алканов
1. Галогенирование – реакция радикального замещения (SR)атомов
водорода на галогены.
а) Инициирование– образование свободных радикалов
Молекулы хлора поглощают свет и диссоциируют на атомы:
б) Рост цепи
Атом хлора может отнимать атом водорода у молекулы алкана с
образованием хлороводорода и алкильного радикала:
Алкильный радикал атакует молекулу хлора,образуя молекулу
алкилгалогенида и атом хлоа, который способен начать следующую
стадию этой цепной реакции
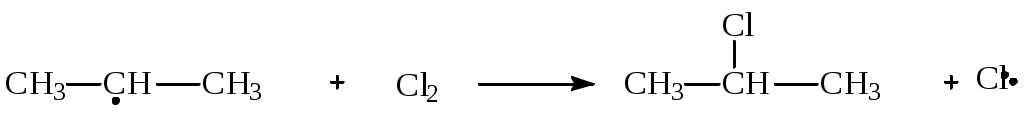
в) Обрыв цепи
Обрыв цепи происходит при взаимодействии каких-либо двух
имеющихся в смеси радикалов:
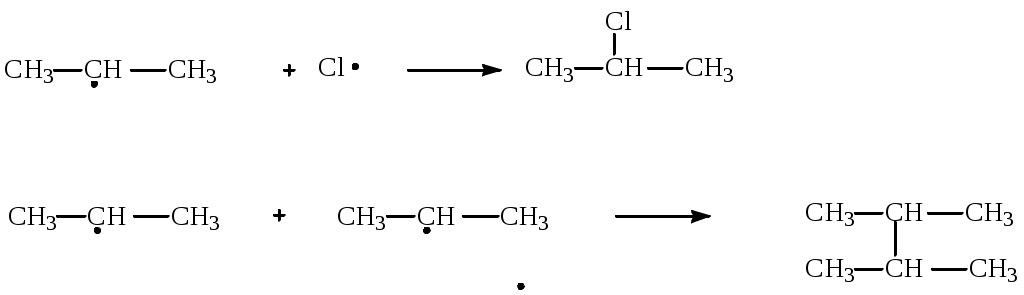
Вообще получить по этому методу монозамещённые продукты
практически невозможно, так как образующиеся алкилгалогениды
взаимодействуют дальше с атомами хлора. На ярком свету реакция
протекает очень бурно(со взрывом).
Устойчивость свободных радикалов уменьшается в следующем ряду:
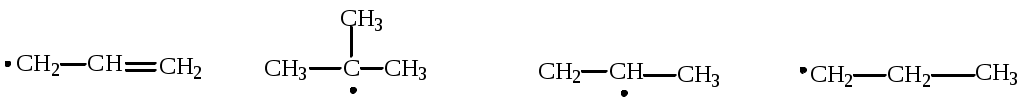 аллил третбутил изопропил пропил
аллил третбутил изопропил пропил Поэтому основным продуктом радикального замещения в реакциях галогенирования алканов являются соединения, в которых атом галогена связан с аллильным или третичным атомом углерода. Гораздо меньше продуктов замещения по вторичному и первичному атомам углерода.