Файл: Учебное пособие по химии для учащихся 10 классов, обучающихся в лицеях фдп рниму под редакцией проф. Теплова В. В.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.01.2024
Просмотров: 1187
Скачиваний: 9
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
470. Смесь диметилэтиламина, втор-бутиламина и метилпропиламина общей массой 29,2 г сожгли в двухкратном, по сравнению с необходимым, объеме воздуха. Определить объемную долю кислорода в конечной смеси до и после конденсации паров воды.
471. К 21 г смеси этана и этиламина добавили 672 мл (н.у.) хлороводорода. Плотность по водороду образовавшейся смеси газов оказалась равна 18,75. Определите объемные доли газов в исходной смеси.
472. Смесь диметиламина, этиламина и метана общей массой 18,6 г с плотностью по неону 1,1625 смешали с 6,72 л (н.у.) бромоводорода. Определите, во сколько раз изменится плотность газовой смеси после реакции.
473. Смесь бензола и анилина массой 1 г сожгли в избытке кислорода. При пропускании продуктов сгорания через избыток раствора гидроксида бария образовалось 14,08 г осадка. Определите состав исходной смеси в массовых долях.
474. 65,4 г смеси хлорида фениламмония и этилового эфира одноосновной кислоты прореагировали с 240 г 10% водного раствора гидроксида натрия. Такое же количество хлорида фениламмония, что и в смеси, может быть получено восстановлением 18,45 г нитробензола в соляной кислоте. Определитее состав исходной смеси в массовых долях и структуру сложного эфира.
475. Для нейтрализации 50 г спиртового раствора смеси анилина и фенола потребовалось 103,7 мл 5% раствора КОН с плотностью 1,07 г/мл, а при добавлении к такой же порции исходного раствора избытка бромной воды получили 38,8 г осадка. Определите массовые доли анилина и фенола в исходном растворе.
476. Рассчитайте массу триметиламина, которую следует растворить в 20 г 17,1% раствора сульфата алюминия для полного осаждения ионов алюминия.
477. Некоторое количество диметиламина сожгли в избытке кислорода,а продукты сгорания растворили в 106,2 мл раствора КОН с массовой долей 14% и плотностью 1,134 г/мл. Определите объем сожженного амина, если в результате реакции образовалось две соли, а массовая доля гидрокарбоната калия в полученном растворе равна 7,4%.
478. К 500 г раствора серина с массовой долей 4,2% добавили 25 г раствора NaOH с массовой долей 48%. Вычислите массовые доли веществ в полученном растворе.
479. К 80 г раствора аланина добавили 5,04 г гидрокарбоната натрия, при этом выделилось 896 мл (н.у.) газа. Определите массовые доли веществ в полученном растворе
480. К 100 г водного раствора глицина прибавили 40,43 мл водного раствора этанола с массовой долей спирта 96% и плотностью 0,8 г/мл. Найдите массовую долю кислоты в исходном растворе, если оба вещества прореагировали полностью. Укажите условия данной реакции.
481. К 80 г раствора, содержащего смесь равных масс хлорида метиламмония и гидросульфата глицина, добавили 200 мл раствора КОН с молярной концентрацией 4 моль/л и плотностью 1,18 г/мл и затем нагрели до полного удаления газообразного продукта. Вычислите массовые доли веществ в полученном растворе, если суммарное количество вещества в исходной смеси было равно 0,2 моль.
482. Образец аминокислоты, входящей в состав белков, массой 4,68 г сожгли в избытке кислорода, при этом выделилось 3,96 г воды и 5,376 л (н.у.) газовой смеси, объем которой уменьшился в 6 раз после пропускания через избыток раствора щелочи. Оставшаяся смесь газов имела плотность по водороду 15. Определите формулу аминокислоты.
483. Продукты сгорания 6 г аминокислоты в избытке кислорода пропустили через трубку с Р2О5, а затем через избыток раствора гидроксида кальция. Масса трубки с Р2О5 увеличилась на 3,6 г, а масса выпавшего осадка равнялась 16 г. Объем газа, оставшегося после поглощения кислорода составил 896 мл (н.у.). Определите формулу аминокислоты. (См. решение).
484. При гидролизе сложного эфира были получены вторичный спирт и природная аминокислота с одной аминогруппой. Продукты сгорания, образовавшиеся при сжигании кислоты, пропустили через избыток раствора гидроксида бария – выпал осадок массой 23,64 г, при этом объем непоглощенного газа составил 448 мл (н.у.). Продукты сгорания, образовавшиеся при сжигании спирта, пропустили через избыток известковой воды – выпал осадок массой 12 г. Установите строение сложного эфира.
485. При кислотном гидролизе дипептида образовалась смесь хлороводородных солей лизина и фенилаланина общей массой 6,31 г. Вычислите массы веществ, которые образовались бы при проведении гидролиза такого же образца дипептида в присутствии избытка КОН.
486. При полном гидролизе дипептида 12% раствором NaOH с плотностью 1,02 г/мл из раствора выделили 22,2 г соли, в которой массовая доля натрия равна 20,72%. Определите формулу и массу дипептида и объем израсходованного раствора щелочи.
ПРИЛОЖЕНИЕ
Таблица 1. Электроотрицательность некоторых атомов по Полингу
| IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| H 2,1 | | | | | | |
| Li 1,0 | Be 1,5 | B 2,0 | C 2,5 | N 3,0 | O 3,5 | F 4,0 |
| Na 0,9 | Mg 1,2 | Al 1,5 | Si 1,8 | P 2,1 | S 2,5 | Cl 3,0 |
| K 0,8 | Ca 1,0 | Ga 1,6 | Ge 1,8 | As 2,0 | Se 2,4 | Br 2,8 |
| Rb 0,8 | Sr 1,0 | In 1,7 | Sn 1,8 | Sb 1,9 | Te 2,1 | I 2,5 |
Таблица 2. Свойства некоторых растворителей
| Растворитель | М г/моль | ρ г/мл(200C) | tпл0С | tкип0С |
| Анилин | 93,13 | 1,022 | -6,0 | 184,25 |
| Ацетон | 58,080 | 0,79 | -94,9 | 56,1 |
| Бензол | 78,14 | 0,88 | +5,5 | 80,8 |
| Бутанол | 74,12 | 0,81 | -79,9 | 117,7 |
| Вода | 18,0 | 1,0 | 9,0 | 100,0 |
| Гексан | 86,18 | 0,66 | -94,0 | 68,8 |
| Глицерин | 92,1 | 1,26 | +18,2 | 290,0 |
| Дихлорэтан | 98,97 | 1,26 | -35,3 | 83,5 |
| Диэтиловый эфир | 74,12 | 0,71 | -117,6 | 34,6 |
| Нитробензол | 123,1 | 1,2 | +5,7 | 210,0 |
| Пропанол-1 | 60,1 | 0,8 | -127,0 | |
| Сероуглерод | 76,14 | 1,26 | -112,8 | 46,25 |
| Толуол | 92,14 | 0,87 | -95,0 | 110,8 |
| Углерод четырёххлористый | 153,8 | 1,6 | -22,9 | 76,7 |
| Уксусная кислота | 60,05 | 1,05 | +16,6 | 118,1 |
| Хлорбензол | 112,6 | 1,11 | -45 | 132,0 |
| Хлороформ | 119,4 | 1,49 | -63,5 | 62,2 |
| Циклогексан | 84,16 | 0,77 | 6,5 | 81,0 |
| Этанол | 46,07 | 0,79 | -11,8 | 78,32 |
| Этаноламин | 61,09 | 1,02 | +10,5 | 172,2 |
| Этилацетат | 88,1 | 0.9 | -83,6 | 77,15 |
| Этиленгликоль | 62,07 | 1,11 | -17,4 | 197,4 |
| Метанол | 32,04 | 0,79 | -94,9 | 64,65 |
Некоторые важные аминокислоты

глицин аланин

серин валин
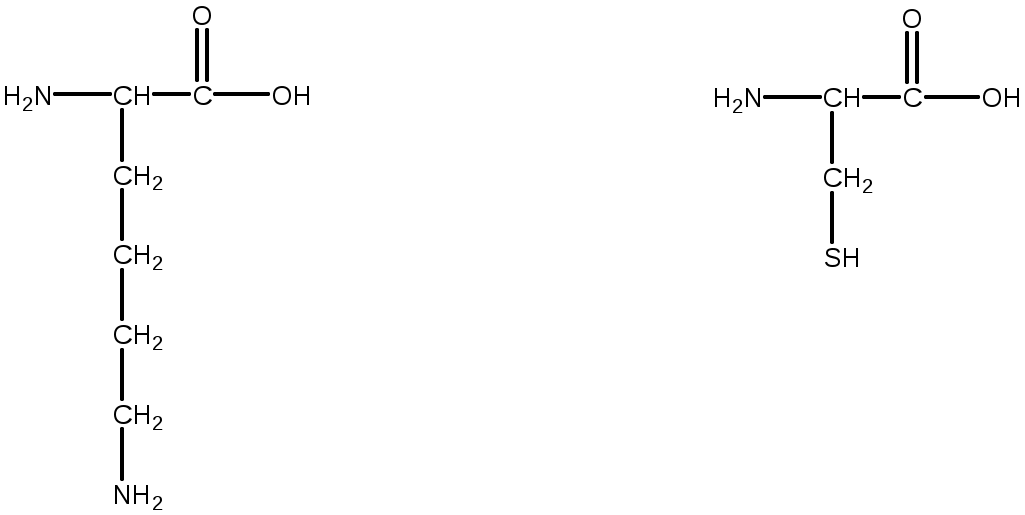
лизин цистеин

глутаминовая кислота фенилаланин
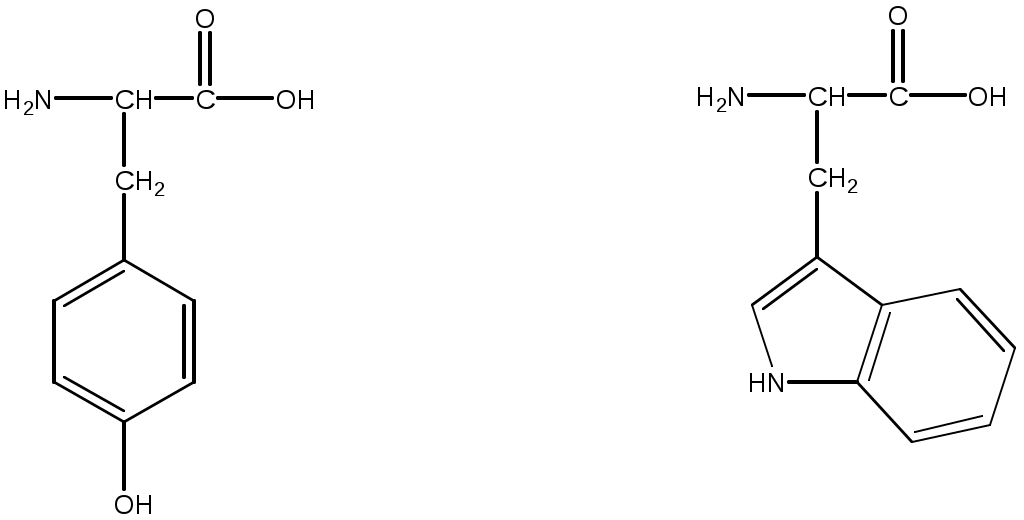
тирозин триптофан
ОТВЕТЫ
1 а)14г; б)48г; в)12,8∙103г; г)5,4∙103г; д) 1,7г; ж)300г)
2. а) 0,25моль; б)10моль; в)100моль; г)3моль; д)0,3моль; ж)5∙10-3 моль;
з)4,4 моль; и)600 моль)
3 а)0,0098г; б) 9800г; в) 1,96г; г) 39,2г
4 а)11,2л; б) 11,2л; в) 9мл; г)11200л; д) 2,24л
5 224 л; 6 а)1,4г;б) 0,0154г;в) 480г
7 26,4г; 8 28г; 9 а)11200л; б) 5,6л; в) 22,4∙103 м3
1 0 а)448л; б) 11,2л; 11 а)16:1; б) равное; в)равное
12 а)28 г/моль, СО; б) 64 г/моль,SO2 ; 13 60г; 14 1,19 : 1
15 1,204∙1024 ; 16 5,824л; 17 а)14 и 0,9655; б) 35,5 и 2,448;
в) 8 и 0,5517
18 а)1,3393 г/л; б) 2,5893 г/л; 19 0,9643 г/л и 0,7448; 20 16г/моль; 8
21 φ(CH4 ) =80%; φ(C2H6)=20% 22 φ(CH4)=55,56%; φ(C2H6)=44,44%
23 0,2605; V(возд.)=73,328л
24 ω(N2)=68,29%; ω(O2)=19,51% ; ω(CH4)=12,20%.
25 в любом соотношении; 26 в любом соотношении
27 ω(С3Н8)=78,57%; 228,57л воздуха
28 а)уменьшится в 1,33 раза; б)уменьшится в 1,143 раза
29 φ(Н2)=33,33%; 30 а)11,25 г; 8,0357г;б) 16,056г; в)8,0357г
31 128,21л; 32 С8Н18; 33 С3Н6О; 39 С4Н10
43 СН4; 44 35,8 г/моль, n(Н)=3,49 моль
45 φ(СН4)=43%, φ(С4Н10)=57% ; 46 Мср =30,0 г/моль, n(С)=1,79 моль
47 СО2 или С3Н8; 48 13,15; 49 ω(СН4) = 41,4%
50 7,2 г; 51 17,92 л; 52 833,5 кг; 53 2 моль
54 ω(СНСI3)=32,89%; ω (ССI4)=67,11%; 55 74,67 л; 56 69,3 г
57 61,6 л; 58 16,625 л; 59 φ(С2Н6)=20%, φ(С3Н8)=80%
60 57,5л; 61 а) 80 л; б) 373 л; 62 81,07%; 63 С2Н4Br2
64. φ(Н2)=φ(С5Н10)=11,97%, φ(С5Н12)=76,06%, η=13,6%
65 С7Н16; 66 14,56 л; 67 44,8 л
68 φ(СО2)=9,84%; φ(О2 )=2,28% ; φ(N2)=87,87%
69 φ(СО2)=4,63%; φ(О2 )=12,59% ; φ(N2)=82,78%
70 0,5 моль; 71 η=79,01%; 72 n(С4Н9Br):n(С4Н9Br2)=1:2
82 С4
Н8; 83 С2Н4; 84 20,8 л; 85 φ(С3Н6) = φ(С3Н8) = 50%
86 φ(Н2)=65,02%; φ(С2Н4 )=15,21% ; φ(С2Н6)=19,76%
87 φ(Н2)=φ(С5Н10 )=11,94%; φ(С5Н12)=76,12%; η=11,94%
88 η=46,03%; φ(Н2)= 20,5%; φ(С5Н10 )=62,0%; φ(С5Н12)=17,5%
89 φ( С4Н10)= 25%; φ(С4Н8 )=6,25%; φ(Н2)=68,75%
90 60,81%; 91 φ( С4Н10)= 50%; φ(С4Н8 )=20%; φ(С2Н4)=30%
92 φ( С2Н6)= φ(С2Н4 )=50%; 93 φ( С3Н6)= φ(С3Н8 )=50%
95 С6Н12; 96 С5Н12; 97 300г; 98 С3Н6
99 φ( С4Н10)= 26,67%; φ(С3Н8 )=33,33%; φ(С3Н6)=40%; 100 0,84 л
101 V(см)= 17,92 л, φ( С4Н10)= 56,3%, φ(С3Н6 )=18,7%, φ(С4Н8)=25%
102 φ( С2Н6)= 50%; φ(С2Н4 )=30%; φ(С4Н8)=20%; ω(С2Н6)=43,3%;
ω (С2Н4)=24,2%, ω(С4Н8)=32,5%
103 ω (С2Н4)=76,04%; ω(С3Н8)=23,96%; 106 3-метилгексадиен-2,4
107 2-метилбутадиен-1,3; 108 2; 112 б; 113 б; 114 2
118 С4Н6; 119 φ(С4Н6)=0,0835; 120 С5Н8; 121 V(Н2)=68,34л
122. изопрен; 123 С6Н10; 124 С5Н8; 125 25% С4Н6; 75% С3Н6
126 C6H10; 127 С4Н6; 128 12 связей; 129 3 изомера
130 5 изомеров; 135 4-метилпентин-1; 4-метилпентин-2; 136 2
137 4; 138 4; 147 С6Н10
148 φ(С2Н6)= φ(С2Н2)=0,5; ω (С2Н6)=0,5357, ω(С2Н2)=0,4643
149 88,88% С, 11,12%Н; бутин-1, бутин-2; 150 127,75 г
151 φ(С3Н4)= φ(С3Н6) =0,2; φ(С2Н6)=0,6
152 φ(C2H6)=20%; φ(C2H4)= 20% и φ(C2H2)=60%
153 φ(C2H2)=22,07% ; φ(C2H4)=22,76%; С2Н6) φ(C2H6)=55,17%
154 в 4 раза; 155 бутин-2; 156 50%С2Н6 и 50% Н2 ; 157 С6Н10
158. 6,286 л; 159 11,2 л ; 160 13,44л; 161 22,4 л
162 4,4-диметилпентин-2; 163 41,65% пропина и 58,35% пропена
164 2,2-диметилпентин-1; 165 бутин-2; 166 6,52г смеси КВr и КОН
167 60% метана, 40% этина; 168. 83,33% этина, 16,67% бутина-1
169 ω(С6Н14)= 0,8695 ; 170 20л
179 φ( СН4)= 25%; φ(С2Н4 )=50%; φ(С3Н6)=25%
180 71,4 г; 181 С4Н8; 182 8,8г; 183 ω(С6Н10)=26,2%