Файл: Дрі Химиялы жне фармацевтикалы технологияны негізгі процестерін жіктеу. Химиялы ндірісті отайландыру.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.01.2024
Просмотров: 765
Скачиваний: 1
СОДЕРЖАНИЕ
Сорғыштың негізгі параметрлері:
Ас тұзы бар ерітіндіден тұзды бөлу үшін, суды қыздырады. Су буланады да, тұз түбінде қалады:
Арал теңізінің жағалауында бұндай тұз көп мөлшерде кездеседі:
Бұл тұз теңіз суының құрамында еді. Кейін су буланып, тұз қайта кристалданып жерде қалды.
Суды қыздырып, буға айналдырып, басқа жерде су буын суытып қайтадан суға айналдыруға болады:
Бұны айдау әдіс деп атайды. Бұл әдістің тағы бір аты - дистилдеу әдісі.
Қоспалардың құрамына және қасиетіне қарай әр түрлі бөлу әдістері қолданылады.
Магнитпен қоспдадан бөлу әдісі.
Суспензияны құр -қатты заттарды сұйық көлемге теп тегіс таратуды қамтамасыз ету;
Қыздыру мен салқындатудың интенсификациясы;
Салмақ ауысу интенсификациясы араластыру жүйесінде (еріту, сілтілеу).
Механикалық- бұлғылауышпен араластыру, аппаратта араласатын оратмен айналады.
Үрдістің тиімділік көрсеткіші- Қоспадағы алынатын заттың концентрациясы.
Механикалық араластыру үрдісінің теориялық маңызы
Критерий Рейнольдса Reм (19.2)
мұнда dм - бұлғылаушының диаметрі, м;
n - бұлғылаушының айналу жылдамдығы, айн /с;
r - сұйықтық тығыздығы, кг/м^3;
Nм -бұлғылаумен жұмыс істеуге кететін қуаттылық, вт;
m - динамикалық тұтқырлық Па*с;
Механикалық араластыру үрдісінің технологиялық –құрылымыдық шамасын есептеу әдісі
1. Бұлғылау түрін таңдау оның диаметрі dм, аппарат өлшемі Daпп и Hапп.
2. Аппаратың түрі мен өлшеміне байланысты коэффициент Сt анықтаймыз.
3. Бұлғылаудың айналу санын анықтайды:
5. Сызба бойынша KN= f(Reм) тауып алады KN.
6. т Nм 2 теңдеуден тауып алады:
7. Құрылғыны айналдыратын өткізгішттің қуаттылығын есептейді Nдв:
Мұнда К- құрылғыны араластыратын және аппаратың құрылымын есептейтін түзету коэффициенті;
Бастапқы компонент бойынша материалдық баланс
Барлық заттар бойынша материалдық баланс
(19.8) және (19.9) алатынымыз:
Басқарылатын айнымалылар – Ссм және hсм.
Сұйық орталарды араластырудың негізгі үш тәсілі болады:
1) механикалық - әртүрлі құрылысты араластырғыштар жәрдемімен;
2) пневматикалық - сығылған ауа немесе инертті газдар жәрдемімен;
3) циркуляциялық - насостар немесе соплалар жәрдемімен.
1) салыстырмалы түрде көп энергия шығыны;
1) механикалық - әртүрлі құрылысты араластырғыштар жәрдемімен;
2) пневматикалық - сығылған ауа немесе инертті газдар жәрдемімен;
3) циркуляциялық - насостар немесе соплалар жәрдемімен.
1) салыстырмалы түрде көп энергия шығыны;
Центрифугалау дегеніміз - центрифугалық күш әсерінен суспензиялар мен эмульсияларды бөлу процесі.
Электрлік тазарту - электр күштерінің әсерінен газды тазарту.
2.Бөлу процесстерінің түрлері?
Жылуөткізгіштік -əртүрлі температурадағы қатты денелер бір-бірімен жанасқанда бірінен-біріне көшетін жылу. Бұл үдерістегі жылудың бір бөлшектен бір бөлшекке берілуі олардың тəртіпсіз қозғалысының нəтижесі деп қараған жөн. Мұндағы бөлшектердің жалпы бір бағыттағы қозғалысы (су сияқты) болмайды. Жылуөткізгіштік таза түрінде тек қатты заттарда ғана байқалады, ал тамшылы сұйықтар мен газдарда конвекция құбылысы жоқ кезінде ғана болады.
Конвекция -тек сұйықтар мен газдарда, олардың молекулаларының өзара алмасуы нəтижесінде болатын жылу таралуы.
Конвекция -еркін жəне еріксіз деп екіге бөлінеді. Газ немесе сұйық көлемінің əртүрлі нүктелеріндегі температуралар айырмашылығы салдарынан, осы нүктелердегі тығыздықтар айырмасының нəтижесінде болатын жылуалмасуды еркін конвекция деп атайды. Газ немесе сұйық көлемінің еріксіз қозғалысы (мысалы, насоспен айдағанда) салдарынан болатын жылуалмасуы еріксіз конвекция деп аталады.
Жылулық сəуле шығару -жылу энергиясының электромагнитті (инфрақызыл) толқындар арқылы таралуы. Бұл ретте жылу сəулесін таратын денеде жылу, сəуле энергиясына айналып кеңістікке таралады да, жолында кездескен денелерге соғылғанда, бұл сəулелі энергия жартылай жылуға айналады, жартылай шағылысады, жартылай сол денеден ары өтіп кетеді.
Техникада жоғарыдағы жылуалмасу үдерістері жеке түрінде өте сирек өтеді. Олар əрқашан екі үдеріс, кейде үш үдеріс түрінде бірлесе өтеді. Мысалы, қатты қабырға мен газ арасындағы жылуалмасуда осы үш үдеріс те болады. Осыған байланысты жалпы жылуалмасу үдерісін екі түрлі ішкі үдерістерге бөлуге болады.
Жылу беру -қатты заттар мен сұйықтардың (газдардың) арасындағы тікелей жылуалмасу үдерістері.
Жылуөту -сұйық пен сұйықтың, газ бен газдың, газ бен сұйықтың, қатты қабырға арқылы жылуалмасу үдерістері.
Кез-келген жылу үдерісінің негізгі сипаттамасы алмасатын жылу мөлшеріне байланысты. Жылуалмасу қондырғыларының өлшемдері осы шамаға байланысты болып келеді. Жылуалмасу қондырғыларының негізгі өлшемі жылу беретін бет немесе жылуалмасу беті болып табылады.
Қондырғыдағы берілетін жылу шамасы мен жылуалмасу бетінің арасындағы байланыс жылу таралудың кинетикалық теңдеуінен анықталады:
d2Q=KЛ∆tdFd τ (2.1)
мұндағы d2Q -берілген жылу мөлшері; Kл -орталар арасындағы жылуалмасудың локальды коэффициенті; ∆t -орталар арасындағы температуралар айырмасы; dF -жылуалмасу бетінің қарапайым бөлігі; dτ -жылуалмасу үдерісінің ұзақтығы.
Жылуөткізгіштік. Фурье теңдеуі. Жылуөткізгіштік коэффициенті. Жылуөткізгіштің негізгі теңдеуін Фурье заңынан жазады. Бұл заң бойынша жылуөткізгіштік арқылы берілген жылу мөлшері dQ, температура градиентіне dt/dn, уақытқа dτ жəне жылу ағынына перпендикуляр жатқан қима беттің ауданына dF тура пропорционал.
dQ=- λdtdF τ/dn, Вт/K
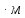 (2.2)
(2.2)Теңдеудегі λ -коэффициенті жылуөткізгіштік коэффициенті деп аталады.
λ -бір уақыт ішінде 1м2 жылуалмасу бетіндегі температуралар айырмасы 1 градус болып, изотермиялық бетке нормаль жатқан қабырға қалыңдығының бірлігінен (1м), жылуөткізгіштік арқылы өткен жылу мөлшерін көрсетеді, яғни ол дененің жылуөткізгіштік қабілетін сипаттайды. Жылуөткізгіштіктің дифференциалдық теңдеуі.
Жылуөткізгіштік арқылы жылу таралуы үдерісін дифференциалдық теңдеу арқылы өрнектеуге болады.
Температураөткізгіштік коэффициенті а дененің жылу инерциялық қасиетін сипаттайды, яғни жылуөткізгіштігі көп дене тезірек қызады немесе тезірек суынады.
Жылуалмасу қондырғыларындағы жылуберу беті негізінен жазық, цилиндрлік немесе сфералық түрде болып келеді. Сондықтан жылуөткізгіштікпен жылудың таралуын осы геометриялық беттер арқылы есептеудің үлкен тəжірибелік мəні бар.
Конвективтік жылуалмасу үдерісі
Сұйықтар ағысы қаншалықты қарқынды, яғни турбулентті болса, соғұрлым конвекция арқылы жылуалмасу күшті болады. Ағындағы жылуалмасу жылуөткізгіштік пен конвекция арқылы болса, конвективтік жылуалмасу деп аталады.
Жылуберу. Ньютон заңы. Сұйықтан қатты денеге, немесе керсінше қатты денеден сұйыққа жылуалмасу беті арқылы берілетін жылу мөлшері, қабырға бетіне tқаб–to=∆t жəне уақытқа тура пропорционал болады.
Бұл теңдеудегі негізгі есептелінетін шама жылуберу коэффиценті α-ның физикалық мəні: ол қабырға мен тамшылы сұйықтың (газдың) арасындағы жылуалмасудың қаншалықты қарқынды өтетіндігін сипаттайды.
Жылуберу коэффиценті өте көп факторларға байланысты өзгеріп отырады. Яғни, α=f(w, ρ ,λ, c, µ, β, d, h, l, e), осыған байланысты α-ны есептеу үшін ұқсастықтар теориясы пайдаланылады.Конвективтік жылуалмасудың дифференциалдық теңдеуі. Конвективтік жылуалмасу жылуөткізгіштік жəне конвекция арқылы өтеді.
Қатты денелер үшін wx=wy=wz=0 болғандықтан, теңдеу жылуөткізгіштіктің дифференциалдық теңдеуіне айналады.
Жылуалмасу үдерістерінің ұқсастықтар теңдеулері. Жылуберу коэффиценті α-ны анықтау үшін Навье-Стокс жəне үздіксіздік теңдеулерін интегралдап шешу керек.
Нуссельт саны қалыптасқан ағындағы қабырға мен ағын ядросы арасындағы жылуалмасу үдерісінің ұқсастығын сипаттайды.
Прандтль саны -конвективтік жылуалмасудағы жылутасымалдағыштардың физикалық қасиеттерінің ұқсастығын сипаттайды.
Грасгоф критерийі -сұйықтар ағынының табиғи конвекция жағдайындағы гидродинамикалық кезеңін сипаттайды.
Осы алынған ұқсастық сандар жылуды конвекциямен берудің ұқсастықтар теңдеуін алуға мүмкіндік береді.
f(Re, Gr, Pr, Fo)=0
Мұндағы Nu біркелкі жағдайлардан құралмағандықтан ұқсастықтың анықталатын саны болады, сонда
Nu=f(Re, Gr, Pr, Fo)
Есептеуді жеңілдету үшін, егер жылуалмасу қалыптасқан болса
Nu= f(Re, Gr, Pr)
Еріксіз конвекция кезіндегі критерийлік теңдеуде Gr критерийі алынып тасталынады
Nu =f(Re, Pr), немесе Nu =A Ren Prm
Ерікті конвекция кезіндегі критерийлік теңдеуде Re критерийі алынып тасталынады.
Сұйықтардың еркін ағуындағы жылуберу. Сұйықтардың еркін ағуы (еркін конвекция) ыстық жəне суық бөлшектердің қысымының салдарынан болады. Мұндағы жылуберудің ұқсастық теңдеуі бойынша жазылады:
Nu =c(GrPr)m (2.11)
Мұндағы с, m -тұрақтылар, олар сұйықтардың қандай кезеңде ағуына байланысты болады: ламинарлық кезеңде Gr·Pr<5·102, мұндағы c=1,18 n=0,125; өтпелі кезеңде Gr·Pr=5·102÷2·107, мұндағы c=0,54 n=0,25; турбулентті кезеңде Gr·Pr>2·107, мұндағы c=0,135 n=0,33. Грасгоф критерийін есептегенде (2.28) бойынша анықтаушы геометриялық өлшем ретінде цилиндрлік жəне сфералық денелер үшін диаметр, ал жазық қабырға үшін олардың биіктігі алынады. Анықтаушы температура ретінде шекаралық қабаттың орташа температурасы t=0,5(tқ+tc) алынады. Осы температура бойынша керекті физикалық мəндердің шамалары анықталады. Сұйықтардың еріксіз ағуындағы жылуберу. Сұйықтардың еріксіз ағуы кезіндегі жылуберудің қарқындылығы бірінші кезекте сұйықтардың ағу кезеңіне байланысты. Ламинарлы кезеңдегі (Re<2300) жылуберу сұйықтардың еркін жəне еріксіз қозғалыстарымен анықталады. Ламинарлы кезеңдегі жылуберуді есептеу үшін мына теңдеу пайдаланылады.
Nu=0.43Re0.33 Pr0.43 Gr0.1 (Pr/Prқаб)0.25. (2.12)
Бұл теңдеу l/d>50 болған кезде дұрыс, мұндағы l -құбыр ұзындығы, м. Анықталмаған шама ретінде каналдың эквивалентті диаметрі dэ алынған. Агрегаттық жағдай өзгергендегі жылуберу. Жылуалмасу үдерісінде көп жағдайда қыздырылатын немесе суытылатын заттар өздерінің агрегаттық жағдайын өзгертеді: буланады, суланады, балқиды немесе кристалданады. Жылуалмасу үдерісінің мұндағы ерекшелігі сол, мұндағы жылу заттарға тұрақты температура кезінде беріледі немесе алынады, ал оның таралуы бір фазада емес, екі фазада өтеді. Жылуберудің осы ерекшелігін ескеруде қосымша ұқсастық сан алады. ∆t=tқаныққан–tқабырға, яғни мұндағы бу өзінің қанығу температурасынан төмен температуралы қабырғамен жанасып конденсацияланудағы температуралар айырымы. К -фазалар шекарасындағы агрегаттық жағдайдың өзгеруі салдарынан болатын ағатын сұйықтың салыстырмалы өзгеру мөлшерін сипаттайды. Басқаша айтқанда, заттың агрегаттық күйінің өзгерісін сипаттайды.
Жылулық сəуле шығару үдерісі
Мына жағдайларда:
Егер A=1, (R=D=0) -денеге түскен сəуленің барлығы сіңіріледі. Абсолюттік қара дене деп аталады.
Егер R=1, (A=D=0) -денеге түскен сəуленің барлығы шағылысады. Абсолюттік ақ дене деп аталады.
Егер D=1, (A=R=0) – денеге түскен сəуленің барлығы өтіп кетеді. Абсолюттік мөлдір дене деп аталады.
Табиғатта мұндай жеке абсолюттік қасиеттері бар денелер жоқ. Олар бірлескен күйде болады. Мысалы қатты денелер үшін D=0, R+A=1. Нақты жағдайларда денеге түскен сəулелік энергияның бір бөлігі шағылысады, бір бөлігі өтіп кетеді, ал бір бөлігі сіңіріледі. Мұндай денелерді сұр денелер деп атайды.
Беті F дененің τ уақытта шығаратын сəулелі энергия мөлшері дененің сəуле шығару қабілеттілігі деп аталады. Жылулық сəуле шығару үдерісін бірнеше заңдар сипаттайды. Стефан-Больцман заңы: абсолюттік қара дененің сəуле шығару қабілеттілігі оның абсолюттік температурасының төртінші дəрежесіне тура пропорционал. Стефан-Больцман заңын сұр денелерге де қолдануға болады. Сұр дененің сəуле шығару коэффициентінің абсолюттік қара дененің сəуле шығару коэффициентіне қатынасы салыстырмалы сəуле шығару қабілеттілігі немесе сұр дененің қаралық дəрежесі деп аталады.
Сұр дененің сəуле шығару жəне сəулені сіңіру қабілеттілігі арасындағы байланысты Кирхгоф заңы бойынша табады. Кирхгоф заңы абсолюттік қара дене мен сұр дененің арасындағы сəуле алмасуынан алынған, яғни бірдей температурадағы кез-келген дененің сəуле шығару қабілеттілігінің сəуле сіңіру қабілеттілігіне қатынасы тұрақты шама болады жəне ол абсолютті қара дененің сəуле шығару қабілеттілігіне тең. Күрделі жылуалмасу. Көптеген жағдайларда жылу үдерістеріндегі жылу таралуы бір мезгілде жылуөткізгіштік, конвекция жəне жылулық сəуле шығару үдерісінің екеуі немесе үшеуінің қатысуымен өтеді. Осындай жылуалмасу үдерістерін күрделі жылуалмасу деп атайды.
Жылуөту үдерісі
Жылу үдерістерінде жылу бір жылутасымалдағыштан екінші жылутасымалдағышқа өтеді жəне ол көптеген жағдайларда, оларды бөлетін қабырға арқылы беріледі. Бұл жағдайда бір жылутасымалдағыштан қабырғаға жəне қабырғадан екінші жылутасымалдағышқа конвекциямен, ал қабырға арқылы жылуөткізгіштікпен беріледі. Осындай жылуалмасуды жылуөту деп атайды. Жылуөту коэффициентінің физикалық мəні: беті 1м2 болған қабырға арқылы температуралар айырмасы 1К жағдайында, температурасы жоғары жылутасымалдағыштан температурасы төмен жылутасымалдағышқа 1с уақыт ішінде өтетін жылу мөлшерін көрсетеді.