Файл: Дрі Химиялы жне фармацевтикалы технологияны негізгі процестерін жіктеу. Химиялы ндірісті отайландыру.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.01.2024
Просмотров: 734
Скачиваний: 1
СОДЕРЖАНИЕ
Сорғыштың негізгі параметрлері:
Ас тұзы бар ерітіндіден тұзды бөлу үшін, суды қыздырады. Су буланады да, тұз түбінде қалады:
Арал теңізінің жағалауында бұндай тұз көп мөлшерде кездеседі:
Бұл тұз теңіз суының құрамында еді. Кейін су буланып, тұз қайта кристалданып жерде қалды.
Суды қыздырып, буға айналдырып, басқа жерде су буын суытып қайтадан суға айналдыруға болады:
Бұны айдау әдіс деп атайды. Бұл әдістің тағы бір аты - дистилдеу әдісі.
Қоспалардың құрамына және қасиетіне қарай әр түрлі бөлу әдістері қолданылады.
Магнитпен қоспдадан бөлу әдісі.
Суспензияны құр -қатты заттарды сұйық көлемге теп тегіс таратуды қамтамасыз ету;
Қыздыру мен салқындатудың интенсификациясы;
Салмақ ауысу интенсификациясы араластыру жүйесінде (еріту, сілтілеу).
Механикалық- бұлғылауышпен араластыру, аппаратта араласатын оратмен айналады.
Үрдістің тиімділік көрсеткіші- Қоспадағы алынатын заттың концентрациясы.
Механикалық араластыру үрдісінің теориялық маңызы
Критерий Рейнольдса Reм (19.2)
мұнда dм - бұлғылаушының диаметрі, м;
n - бұлғылаушының айналу жылдамдығы, айн /с;
r - сұйықтық тығыздығы, кг/м^3;
Nм -бұлғылаумен жұмыс істеуге кететін қуаттылық, вт;
m - динамикалық тұтқырлық Па*с;
Механикалық араластыру үрдісінің технологиялық –құрылымыдық шамасын есептеу әдісі
1. Бұлғылау түрін таңдау оның диаметрі dм, аппарат өлшемі Daпп и Hапп.
2. Аппаратың түрі мен өлшеміне байланысты коэффициент Сt анықтаймыз.
3. Бұлғылаудың айналу санын анықтайды:
5. Сызба бойынша KN= f(Reм) тауып алады KN.
6. т Nм 2 теңдеуден тауып алады:
7. Құрылғыны айналдыратын өткізгішттің қуаттылығын есептейді Nдв:
Мұнда К- құрылғыны араластыратын және аппаратың құрылымын есептейтін түзету коэффициенті;
Бастапқы компонент бойынша материалдық баланс
Барлық заттар бойынша материалдық баланс
(19.8) және (19.9) алатынымыз:
Басқарылатын айнымалылар – Ссм және hсм.
Сұйық орталарды араластырудың негізгі үш тәсілі болады:
1) механикалық - әртүрлі құрылысты араластырғыштар жәрдемімен;
2) пневматикалық - сығылған ауа немесе инертті газдар жәрдемімен;
3) циркуляциялық - насостар немесе соплалар жәрдемімен.
1) салыстырмалы түрде көп энергия шығыны;
1) механикалық - әртүрлі құрылысты араластырғыштар жәрдемімен;
2) пневматикалық - сығылған ауа немесе инертті газдар жәрдемімен;
3) циркуляциялық - насостар немесе соплалар жәрдемімен.
1) салыстырмалы түрде көп энергия шығыны;
Центрифугалау дегеніміз - центрифугалық күш әсерінен суспензиялар мен эмульсияларды бөлу процесі.
Электрлік тазарту - электр күштерінің әсерінен газды тазарту.
2.Бөлу процесстерінің түрлері?
3.Сорбционные процесі және оларды тамақ өндірісінде қолдану түрлері?
4. Абсорбция процесінің қозғаушы күші не?
5 Абсорбциялау аппараттарының жіктелуі және олардың конструкциясы?
6.Адсорбция процесі дегеніміз не?
7. Адсорбция процесінің қозғаушы күші не?
8.Адсорбциялау аппараттарының жіктелуін түсіндір. Адсорбциялық аппаратының конструкциясы қандай?
9.Кептіру процесі дегеніміз не?
10.Кептіру процесінің сипаттамасы қандай?
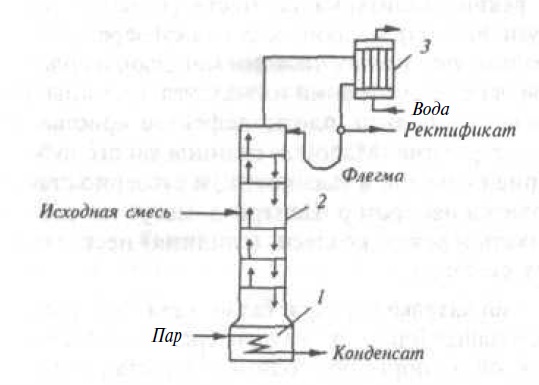
Дәріс 15. Дистилляция және түзету. Дистилляциялық колоннаның материалдық балансы. Ең аз және нақты рефлюк номері
Массаалмасу үдерістері деп бір фазадан екінші фазаға өтетін бөлшектердің (массаның) өту жылдамдығымен анықталатын технологиялық үдерістерді айтады, ал осы үдерістерді өткізуге керекті қондырғылар массаалмасу қондырғылары деп аталады. Массаалмасу қондырғыларында əртүрлі үдерістер өтуі мүмкін. Ондай үдерістерге абсорбция, ректификация, экстракция, кристалдандыру, адсорбция, кептіру, ионалмасу, мембраналық айыру, т.б.үдерістер жатады.
Ректификация -сұйық қоспалардың құрамындағы компоненттерінің əртүрлі температурада ұшқыштығына негізделген, сұйық қоспа мен оның буының қарама-қарсы əрекеттесуінің нəтижесінде, сұйық қоспаның құрамындағы компоненттердің бір-бірінен толық ажыратылу үдерісі. Ректификацияда қыздырылған бастапқы сұйық қоспа, бу жəне сұйық фазаларының бір-бірімен қарама-қарсы əрекеттесулері нəтижесінде дистиллят пен кубтық қалдыққа бөлінеді. Барлық қоспа үшін материалдық баланс былай жазылады:
GF=GD+GW
концентрациялары бойынша
GF xF=GD xD+GW xW
мұндағы GF -ректификацияға түсетін қоспа мөлшері; GD мен GW -алынған дистиллят пен кубтық қалдық мөлшері; xF, xD, xW -жеңіл ұшатын компоненттің бастапқы қоспа, дистиллят жəне кубтық қалдықтағы мөлшері (моль. үлестер).
Теңдеулерді бірлестіре шешіп табамыз
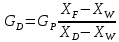
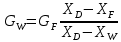
Ректификация үдерісі кезінде бу мен сұйық арасында мөлшерсіз көп əрекеттесулер болады. Соған сəйкес ректификациялық қондырғыдағы бу мен сұйықтың əрекеттесуінде мынандай шарттар қабылданған, яғни: а) компонттердің мольдік булану жылулары бірдей, сондықтан будың əрбір кг/моль шамасы конденсацияланғанда соған сəйкес сұйықтың кг/моль шамасы пайда болады. Сол себепті аппаратта төменнен жоғары көтерілген будың мольдік ағыны, аппараттың кез-келген қимасында бірдей болады. б) аппараттағы дефлегматорға көтерілген бу конденсацияланғанда оның құрамы өзгермейді, сондықтан да аппараттан көтерілген бу мен дистилляттың құрамдары бірдей, яғни убу = уD=хD; в) куб -буландырғыштан көтерілген бу мен кубтық сұйықтың құрамдары бірдей уw=xw; Дефлегматорға көтерілген будан пайда болған конденсат екі бөлікке бөлінеді: бірінші бөлігі массаалмасуды қамтамасыз ету үшін колоннаға қайта жіберіледі, оны
флегма деп атайды, ал екінші бөлігі өнім ретінде алынады, оны дистиллят деп атайды. Флегмаға сəйкес флегмалық сан деген ұғым бар. Ол колоннаға жіберілген флегманың сандық мəнінің, өнім ретінде алынған дистилляттың сандық мəніне қатынасын көрсетеді, яғни R=Ф/D.
Флегмалық санды анықтап, жұмыстық концентрация сызығының теңдеулерін шығарып алу үшін, ректификацияның материалдық балансын төменгі температурада ұшатын компонент үшін қарастырамыз. Ол барлық массаалмасу үдерістері үшін мынадай жалпы теңдікпен жазылады:
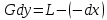
Ректификациялық колоннадағы сұйық қоспа бөлінуі үшін, яғни бу мен сұйық ағындары арасында əрекеттесулер болуы үшін, олардың қатынастары бу мөлшері үшін (R+1), ал сұйық мөлшері үшін (R) болуы керек. (R+1) -булану еселігі, (R) -конденсациялану еселігі деп аталынады. Осыдан əрекеттесетін бу мөлшері G кмоль, ал сұйық L кмоль болса, онда колоннанның жоғары бөлігі үшін G=(R+1)GD мен L=RG теңдеулері, ал колоннанның төменгі жағы үшін L=(R+F)GD теңдеулері сəйкес болады.
Сонда материалдық баланс болады
(R+1)dy=R(–dx),
жəне
(R+1)dy=(R+F)(–dx)
Колоннаның қандай да бір қимасы үшін жұмыстық концентрациялар х пен у болса, ал колоннаның жоғары жағы үшін хD жəне уD болса, теңдеуден аламыз:
(R+1)(уD–у)=(R+1)(хD–y)=R(хD–х),
осыдан колоннаның жоғары жағы үшін жұмыстық сызығының теңдеуі болады
Колоннаның төменгі жағы үшін х–у жəне xW–yW болса, жұмыстық сызығының теңдеуі
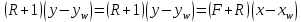
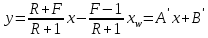
теңдеулер ректификациялық колоннаның жоғары жəне төменгі бөліктері үшін жұмыстық концентрация сызығының теңдеулері болып табылады. (3.66) теңдеуден колоннаның қандай да бір қимасы үшін жұмыстық концентрациялар х пен у, ал колоннаның жоғары жағы үшін хD жəне уD болғанда аламыз:
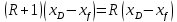
Осыдан
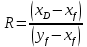
НемесеR=Rmin·σ,
мұндағы Rmin -массаалмасуға қажетті флегманың ең аз мөлшері; σ – флегманың артықшылық коэффициенті. Жұмыстық концентрацияның у–х диаграммаларындағы жағдай бастапқы қоспаның құрамына жəне оның жылулық мəндеріне қатысты болады. Осыған байланысты, бастапқы қоспаны берудің мынадай жолдары болуы ықтимал:1) бастапқы қоспаның қайнау температураcынан төменгі температурада; 2) бастапқы қоспаның қайнау температурасында; 3) сұйық пен қаныққан будың қоспасымен; 4) қаныққан бумен; 5) қатты қыздырылған бумен.
Колоннаның min кіші көлемі жағдайындағы оптималды флегмалық санды табу керек болады. Мұндағы ректификациялық колонна арқылы өтетін бу шамасы GD(R+1)-ге тең болады, сонда оның көлемдік жылдамдығы мына теңдіктен анықталады:
VD=GD(R+1)/(3600ρF)
Алдын-ала берілген VD мен GD кезінде колоннаның қимасы (R+1)-ге, ал аппарат биіктігі mx-ға (ТБС) пропорционал болады. Сəйкес түрде, mx·(R+1) шамасы аппараттың жұмыстық көлеміне пропорционал болады. Осыдан R-дің сандық мəнін Rmіn
Концентрациялары xw ден хр-ге дейін өзгеру шегінде жататын, координаталары ус, хб болатын барлық нүктелердің жинамасы кинетикалық қисық деп аталатын сызықты береді. Кинетикалық қисықты мынадай тəртіппен: у-х диаграммасына тепе-теңдік жəне жұмыстық сызықтарды (оптималдық флегмалық санда) тұрғызады xw -хр аралығында бірнеше х мəндерін таңдап алады
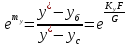
х-тің таңдап алынған əрбір мəніне теңдеуі бойынша у*-ус-ің сəйкес мəндерін есептеп табады. Есептеуге қажетті у*-уб мəндерін у-х диаграммасынан х-тің əрбір мəні үшін тепе-теңдік пен жұмыстық концентрациялардың айырымы ретінде анықтайды. Яғни,
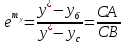
Осыдан
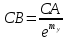
Алынған кесінділерді тепе-теңдік сызығының төменгі жағынан орналастырады. Алынған нүктелерді бір-бірімен жалғап сызық тұрғызады. Алынған сызық кинетикалық сызықты береді. Кинетикалық сызық белгілі болған жағдайда, қондырғыдағы қажетті ажырату дəрежесін қамтамасыз ететін нақты табақшалар санын, жұмыстық жəне кинетикалық сызықтар арасында сатылы түзу сызықтар тұрғызу арқылы анықтайды. Сатылы сызықты концентрациялар бойынша xf -тен xD-ге дейін жəне xf -тен xw-ге дейін тұрғызады. Концентрацияның xfтен xD-ге дейінгі аралығы колоннаның жоғарғы бөлігіндегі нақты табақшалар санына сəйкес келеді, ал xf -тен xw-ге дейінгі аралық колоннаның төменгі бөлігіндегі нақты табақшалар санын береді. Əрбір табақша үшін ТБС-тың сандық мəндерін
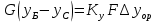 теңдеуін қолдана отырып анықтайды
теңдеуін қолдана отырып анықтайды 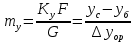 осыдан
осыдан 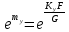
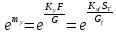
мұндағы ST -табақшаның жұмыстық ауданы, ол табақшаның көлденең қима ауданының 85–90 %-ы болады, м2; Куf -табақшаның жұмыстық ауданына қатысты массаөту коэффициенті, кмоль/(м2·сағ); Gf -бастапқы қоспаның мольдік шығыны, (кмоль/сағ) Табақша үшін массаөту коэффициентін Куf фазалық кедергінің аддивтілігі заңынан анықтайды
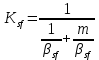
мұндағы βуf -табақшаның жұмыстық ауданына қатысты бу фазасындағы массаберу коэффициенті, (кмоль)/м2сағ; βxf -табақшаның жұмыстық ауданына қатысты сұйық фазасындағы массаберу коэффициенті, (кмоль)/м2сағ; m -тепе-теңдік сызығының бұрыштық коэффициенті.
Ректификация үдерісінің жылу балансы
Жалпы баланс мына түрде жазылады:
Q1+Q2+Q3=Q4+Q5+Q6
мұндағы Q1 -қыздырғыш бумен келетін жылу, немесе басқаша айтқанда үдерісті жүргізуге жұмсалатын жылу, кДж/сағ; Q2 -бастапқы қоспамен келетін жылу; кДж/сағ; Q3 -флегмамен келетін жылу, кДж/сағ; Q4 -бумен кететін жылу, кДж/сағ; Q5 -кубтық қалдықпен кететін жылу, кДж/сағ; Q6 -қоршаған ортаға кететін жылу, кДж/сағ. (3.79) теңдеуді Q1-ге байланысты ашып жазсақ аламыз -
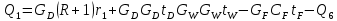
мұндағы RD -дистилляттың булану жылуы, кДж/сағ. Мерзімдік ректификациялық қондырғылар. Өндірісте R=const жағдайындағы ректификациялау үдерісі, əсіресе аз өндірісті орындарда кеңінен қолданылады. Оның себебі бұл үдерісті бір ғана ректификациялық қондырғыда тиімді түрде өткізуге болады. R=const жағдайындағы жұмыстық сызықтардың қисаюы концентрацияға тəуелді болмайды, жұмыстық сызықтар параллельді түрде өзгереді. Жалпы жоғары құрамды дистиллят алу үшін фракциялық ректификация деп аталатын технологиялық əдіс қолданылады. Оның мəні 3.11, асуретте көрініп тұр, яғни мұндағы бастапқы
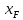 -тан
-тан 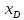 мен
мен 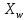 алынады, олар тағы да ректификациялық қондырғыға салынып,
алынады, олар тағы да ректификациялық қондырғыға салынып, 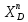 мен
мен 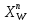 алынады. Осылай қайталай отырып, керекті тазалықтағы
алынады. Осылай қайталай отырып, керекті тазалықтағы 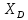 -ны алуға болады.
-ны алуға болады. 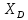 =const жағдайында R шамасы үдерістің басында
=const жағдайында R шамасы үдерістің басында 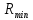 болады, ал соңында
болады, ал соңында 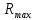 мəнге жетеді. Мұндағы бастапқы қоспа төменгі температурада ұшатын компоненттен ажыраған сайын
мəнге жетеді. Мұндағы бастапқы қоспа төменгі температурада ұшатын компоненттен ажыраған сайын 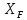 →
→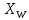 -ға жақындай түседі. Мысалы
-ға жақындай түседі. Мысалы 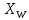
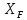 концентрациялары арқылы. Ең соңында
концентрациялары арқылы. Ең соңында 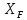 =
=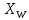 болады. Бірақ мұндай үдерісті жүргізу қиын болады. Өйткені ол үшін колоннаға берілетін бу мен флегма құрамдарын программалық түрде өзгертіп отыруға тура келеді.
болады. Бірақ мұндай үдерісті жүргізу қиын болады. Өйткені ол үшін колоннаға берілетін бу мен флегма құрамдарын программалық түрде өзгертіп отыруға тура келеді.Үздіксіз ректификациялық қондырғылар. Бұл жобада жылу тиімді қолданылмайды, яғни колоннадан шыққан ағындардың жылуы пайдаланылмайды, ал ол жылуды бастапқы қоспаны жылытуға пайдалануға болар еді. Қоспадағы компоненттердің салыстырмалы ұшқыштықтары бір-біріне өте жақын болса, оларды жай ректификациялық əдіспен айырып алу өте қиын. Сондықтан ондай қоспаларды экстрактивтік жəне азеотроптық ректификация көмегімен ажыратады. Экстрактивтік ректификация кезінде бастапқы қоспаға жоғары температурада қайнайтын компонент қосылады. Осы компонентте бастапқы компоненттердің біреуі өте жақсы еруі керек, ал екінші компонент ерімейтін немесе өте аз еритін болуы керек. Осы алынған қоспаны одан кейін жай ректификация арқылы бөліп алады. Азеотропты ректификация кезінде жүйеге азеотропты қоспа құрайтын компонент қосылады. Ол ұшатын компоненттің буындағы қысымды Рmax жасайды немесе екінші компоненттің буында Рmіn жасайды. Осыған байланысты буды жекелей бөліп алуға болады. Көп компонентті қоспалардың ректификациясы. Химиялық өндірісте көп компонентті қоспалармен жиі жұмыс істеуге тура келеді, оларды бөлу үшін арнайы ректификациялық қондырғылар қолданылады. Көп компоненттік қоспалардың жұмыстық сызықтарының теңдеулері екі компоненттік қоспалардың жұмыстық сызықтарына ұқсас, аппараттың жоғары жағы үшін