Файл: Лабораторная работа 1 Определение меди фотоэлектроколориметрически по окраске её аммиачного комплекса.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.01.2024
Просмотров: 280
Скачиваний: 14
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
кисл. по данным потенциометрического титрования определяется из кривой титрования графическим способом. Известно, что до точки эквивалентности в растворе содержится буферная смесь из СН3СООН и её соли СН3СООNa.
Обработка результатов:
Таблица 11. Значения рН при грубом титровании
Таблица 12. Значения рН при точном титровании
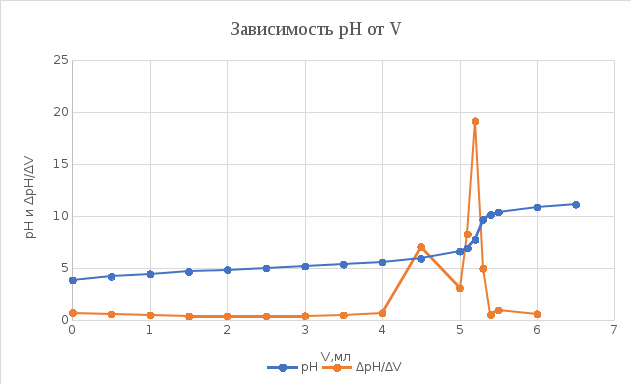
График 10. Определение точки эквивалентности
Расчёт массы уксусной кислоты:
m (CH3COOH) =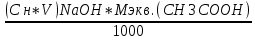
где:
m (CH3COOH) =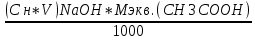 =
= 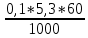 = 0,0318 г
= 0,0318 г
Расчёт константы ионизации:
V (точки эквивалентности) = 5,3 мл
V1/2 =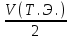 = 2,65 мл
= 2,65 мл
Объёму 2,65 мл соответствует рН = 4,9
рН1/2 = рКкисл.
рН1/2 = 4,9 = Ккисл.
Табличное значение Ккисл. для усусной кислоты = 4,76
Вывод: определено содержание уксусной кислоты в анализируемом растворе – 0,0318 г, а также Ккисл. равную 4,9.
Обработка результатов:
Таблица 11. Значения рН при грубом титровании
| V (NaOH), мл | рН |
| 0,0 | 3,802 |
| 0,5 | 4,115 |
| 1,0 | 4,383 |
| 1,5 | 4,610 |
| 2,0 | 4,782 |
| 2,5 | 4,958 |
| 3,0 | 5,124 |
| 3,5 | 5,298 |
| 4,0 | 5,525 |
| 4,5 | 5,839 |
| 5,0 | 6,442 |
| 5,5 | 10,237 |
| 6,0 | 10,890 |
| 6,5 | 11,140 |
Таблица 12. Значения рН при точном титровании
| V (NaOH), мл | рН | ΔрН/ΔV |
| 0 | 3,806 | |
| 0,5 | 4,142 | 0,672 |
| 1 | 4,406 | 0,528 |
| 1,5 | 4,633 | 0,454 |
| 2 | 4,803 | 0,34 |
| 2,5 | 4,973 | 0,34 |
| 3 | 5,143 | 0,34 |
| 3,5 | 5,326 | 0,366 |
| 4 | 5,548 | 0,444 |
| 4,5 | 5,875 | 0,654 |
| 5 | 6,577 | 7,02 |
| 5,1 | 6,88 | 3,03 |
| 5,2 | 7,703 | 8,23 |
| 5,3 | 9,615 | 19,12 |
| 5,4 | 10,108 | 4,93 |
| 5,5 | 10,35 | 0,484 |
| 6 | 10,812 | 0,924 |
| 6,5 | 11,089 | 0,554 |
График 10. Определение точки эквивалентности

Расчёт массы уксусной кислоты:
m (CH3COOH) =
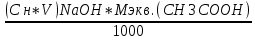
где:
-
Сн, V – молярная концентрация эквивалента и объём тиранта в точке эквивалентности, моль/л;мл; -
Мэкв. (СН3СООН) – молярная масса эквивалента уксусной кислоты.
m (CH3COOH) =
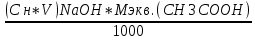 =
= 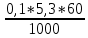 = 0,0318 г
= 0,0318 гРасчёт константы ионизации:
V (точки эквивалентности) = 5,3 мл
V1/2 =
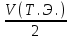 = 2,65 мл
= 2,65 млОбъёму 2,65 мл соответствует рН = 4,9
рН1/2 = рКкисл.
рН1/2 = 4,9 = Ккисл.
Табличное значение Ккисл. для усусной кислоты = 4,76
Вывод: определено содержание уксусной кислоты в анализируемом растворе – 0,0318 г, а также Ккисл. равную 4,9.