Файл: Методические рекомендации по выполнению лабораторных и практических работ по учебной дисциплине ен. 01 Химия.docx
Добавлен: 12.01.2024
Просмотров: 726
Скачиваний: 4
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
, определение кратности пен и устойчивости пен. Приобретение практических навыков работы с химическим оборудованием и реактивами.
Реактивы и материалы: мерный цилиндр с притертой пробкой на 50-100 мл; стакан на 50 мл; кольцо из медной проволоки диаметром 15-20 мм; жидкое мыло, вода, желатина.
Теоретическая часть
Пены — грубодисперсные системы, в которых дисперсная фаза — газ, а дисперсионная среда — жидкость в виде тонких пленок. Чистые жидкости не дают пен. Чтобы получить устойчивые пены, необходимы эффективные стабилизаторы-пенообразователи. К типичным пенообразователям водных пен относятся спирты, мыла, белки.
Пены по своей природе близки к концентрированным эмульсиям, но дисперсной фазой в них является газ, а не жидкость. Пены получают из растворов поверхностно-активных веществ. Для повышения их устойчивости в растворы ПАВ добавляют высокомолекулярные вещества, повышающие вязкость растворов. В качестве характеристик пены используется комплекс свойств, всесторонне характеризующих пену.
Ознакомьтесь с правилами по технике безопасности при работе в химической лаборатории и распишитесь в журнале по ТБ.
Ход работы
Опыт 1. Получение пены
В цилиндр емкостью 50-100 мл наливают 10 мл воды и 1 мл жидкого мыла. Встряхивают эту смесь в течение 15-20 сек. После прекращения встряхивания включают секундомер, одновременно отмечая объем образовавшейся пены. Наблюдают изменение объема во времени.
Затем повторяют этот опыт при разбавлении раствора в 2, 4 раз. Полученные результаты записывают в таблицу 1.
Таблица 1
Опыт 2. Время жизни пены
Готовят растворы, как в опыте 1. Исследуемый раствор наливают в стаканчик на 50 см3 и перемешивают. Затем в него погружают проволочное кольцо. Кольцо осторожно вынимают из жидкости и по секундомеру отмечают время с момента образования пленки до ее разрушения – время жизни элементарной пены.
Для каждого из приготовленных растворов проводят 10 отсчетов времени жизни элементарной пены и вычисляют среднюю величину.
Опыт 3. Получение и разрушение пен
В цилиндр наливают 50 мл раствора пенообразователя (олеата натрия) и встряхивают в течение 30 секунд.
После прекращения встряхивания включают секундомер и немедленно отмечают объем образовавшейся пены. Истинный объем пены получают, вычитая из общего объема системы в цилиндре объем оставшегося раствора.
Отметить время самопроизвольного уменьшения объема пены в 2 раза (устойчивость пены), рассчитать кратность пены (L=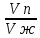 ).
).
Повторным встряхиванием в течение 30 секунд восстановить пену. В пену, стабилизированную олеатом натрия, ввести 1-2 мл соляной кислоты (1 н). Описать наблюдаемые явления.
В цилиндр налить 50 мл раствора пенообразователя (желатины) и встряхнуть в течение 30 секунд.
После прекращения встряхивания включить секундомер и отметить объем образовавшейся пены. Рассчитать истинный объем пены, устойчивость, кратность пены. Результаты непосредственных наблюдений и расчеты оформить в виде таблицы.
Таблица 2
Оформите результаты лабораторной работы в тетради.
Сделайте выводы.
Изучение процессов набухания и студнеобразования крахмала, желатина и различных видов зерен
Цель: Исследование кинетики ограниченного набухания веществ; факторов, влияющих на процессы набухания и студнеобразования.
Реактивы и оборудование: штатив с пробирками, колбы, мерные цилиндры, термометр, линейка, водяная баня, химические весы, желатин, крахмал, зерно, печенье, 0,025 % растворы HCL и NaOH, 0,1 % растворы NaCL, KCL, K2SO4, KCNS.
Теоретическая часть
Полимеры подобно низкомолекулярным веществам обладают избирательной растворимостью. Растворению полимера предшествует набухание. Набухание зависит, как от природы полимера, так и от природы жидкости. Полярные полимеры набухают в полярных жидкостях, а неполярные — в неполярных.
С повышением температуры скорость набухания увеличивается. Тепловой эффект, сопровождающий набухание полимера в жидкости, называется теплотой набухания.
Растворы высокомолекулярных веществ способны терять текучесть и застудневать, образуя при этом студни. Студнеобразное состояние вещества можно рассматривать как промежуточное между жидким и твердым состоянием. Застудневание связано с увеличением вязкости и замедлением броуновского движения и заключается в объединении частиц дисперсной фазы в форме сетки или ячеек и связывании при этом всего растворителя.
С повышением концентрации способность к застудневанию увеличивается, т.к. при этом уменьшается расстояние между частицами. Процесс застудневания даже при низкой температуре не происходит мгновенно и нередко требует продолжительного времени для формирования ячеистой объемной сетки.
Время, необходимое для застудневания, называется периодом созревания.
Продолжительность созревания зависит от природы веществ, концентрации, температуры.
Ознакомьтесь с правилами по технике безопасности при работе в химической лаборатории и распишитесь в журнале по ТБ.
Ход работы
Опыт 1. Кинетика набухания зерна
Зерновые культуры (пшено, рис, лучше дробленый) ограниченно набухают в воде. Зерно насыпают в пробирки (1/3) так, чтобы во всех пробирках было одинаковое количество зерна по высоте. Наливают дистиллированную воду, чтобы вместе с зерном пробирки были заполнены на ¾ объема. Наблюдения за процессом набухания проводят в течение 40-50 минут. Полученные данные заносят в таблицу 1 по образцу:
Таблица № 1
Опыт 2. Влияние кислоты, щелочи и солей на набухание желатины
В семь пробирок одинакового диаметра вносят по 0,3 г. порошка желатины. В каждую пробирку наливают по 5 мл различных растворов (см. табл. № 2). Пробирки осторожно встряхивают, чтобы частицы желатины опустились на дно, определяют высоту осадка желатины до набухания. После этого, встряхнув пробирки несколько раз, оставляют их в покое на 40-50 мин. По истечении этого времени каждую пробирку еще раз встряхивают, дают осадку осесть, измеряют высоту набухшего осадка желатины (с каждой пробиркой измерения повторяют 2 раза). Данные заносят в таблицу 2.
Таблица № 2
Реактивы и материалы: мерный цилиндр с притертой пробкой на 50-100 мл; стакан на 50 мл; кольцо из медной проволоки диаметром 15-20 мм; жидкое мыло, вода, желатина.
Теоретическая часть
Пены — грубодисперсные системы, в которых дисперсная фаза — газ, а дисперсионная среда — жидкость в виде тонких пленок. Чистые жидкости не дают пен. Чтобы получить устойчивые пены, необходимы эффективные стабилизаторы-пенообразователи. К типичным пенообразователям водных пен относятся спирты, мыла, белки.
Пены по своей природе близки к концентрированным эмульсиям, но дисперсной фазой в них является газ, а не жидкость. Пены получают из растворов поверхностно-активных веществ. Для повышения их устойчивости в растворы ПАВ добавляют высокомолекулярные вещества, повышающие вязкость растворов. В качестве характеристик пены используется комплекс свойств, всесторонне характеризующих пену.
-
Пенообразующая способность раствора — количество пены, выражаемое её объёмом (см³) или высотой столба (м), которое образуется из заданного постоянного объёма пенообразующего раствора при соблюдении некоторых стандартных условий пенообразования в течение постоянного времени. -
Кратность пены, которая представляет собой отношение объёма пены к объёму раствора, пошедшего на её образование. -
Стабильность (устойчивость) пены — её способность сохранять общий объём, дисперсность и препятствовать вытеканию жидкости (синерезису). Часто в качестве меры стабильности используют время существования («жизни») выделенного элемента пены (отдельного пузырька или пленки) или определённого объёма пены. -
Дисперсностьпены, которая может быть охарактеризована средним размером пузырьков, распределением их по размерам или поверхностью раздела «раствор-газ» в единице объёма пены.
Экспериментальная часть
Ознакомьтесь с правилами по технике безопасности при работе в химической лаборатории и распишитесь в журнале по ТБ.
Ход работы
Опыт 1. Получение пены
В цилиндр емкостью 50-100 мл наливают 10 мл воды и 1 мл жидкого мыла. Встряхивают эту смесь в течение 15-20 сек. После прекращения встряхивания включают секундомер, одновременно отмечая объем образовавшейся пены. Наблюдают изменение объема во времени.
Затем повторяют этот опыт при разбавлении раствора в 2, 4 раз. Полученные результаты записывают в таблицу 1.
Таблица 1
| Концентрация пенообразователя | |||||
| С1 | С2 = 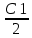 | С3 = 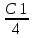 | |||
| Время, сек | Объем пены, V, мл | Время, сек | Объем пены, V, мл | Время, сек | Объем пены, V, мл |
| 0 сек | | 0 сек | | 0 сек | |
| 300 сек (5мин) | | 300 сек (5мин) | | 300 сек (5мин) | |
| 600 сек (10 мин) | | 600 сек (10 мин) | | 600 сек (10 мин) | |
Опыт 2. Время жизни пены
Готовят растворы, как в опыте 1. Исследуемый раствор наливают в стаканчик на 50 см3 и перемешивают. Затем в него погружают проволочное кольцо. Кольцо осторожно вынимают из жидкости и по секундомеру отмечают время с момента образования пленки до ее разрушения – время жизни элементарной пены.
Для каждого из приготовленных растворов проводят 10 отсчетов времени жизни элементарной пены и вычисляют среднюю величину.
Опыт 3. Получение и разрушение пен
В цилиндр наливают 50 мл раствора пенообразователя (олеата натрия) и встряхивают в течение 30 секунд.
После прекращения встряхивания включают секундомер и немедленно отмечают объем образовавшейся пены. Истинный объем пены получают, вычитая из общего объема системы в цилиндре объем оставшегося раствора.
Отметить время самопроизвольного уменьшения объема пены в 2 раза (устойчивость пены), рассчитать кратность пены (L=
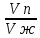 ).
). Повторным встряхиванием в течение 30 секунд восстановить пену. В пену, стабилизированную олеатом натрия, ввести 1-2 мл соляной кислоты (1 н). Описать наблюдаемые явления.
В цилиндр налить 50 мл раствора пенообразователя (желатины) и встряхнуть в течение 30 секунд.
После прекращения встряхивания включить секундомер и отметить объем образовавшейся пены. Рассчитать истинный объем пены, устойчивость, кратность пены. Результаты непосредственных наблюдений и расчеты оформить в виде таблицы.
Таблица 2
| Пенообразователь | Объем, мл | Характеристика пены | |||
| | Пены (Vп) | Жидкости (Vж) | Устойчивость пены, t | Кратность пены, L= 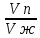 | |
| | | | | | |
Оформите результаты лабораторной работы в тетради.
Сделайте выводы.
Контрольные вопросы
-
Какие системы называются пенами? -
Как классифицируются пены? Что называется кратностью пены? -
В чем заключается седиментационная и агрегативная устойчивость пены? -
Какие вещества используют в качестве пенообразователей? -
Какие вы знаете факторы устойчивости пены? -
Какие существуют методы разрушения пен?
Лабораторная работа № 15
Изучение процессов набухания и студнеобразования крахмала, желатина и различных видов зерен
Цель: Исследование кинетики ограниченного набухания веществ; факторов, влияющих на процессы набухания и студнеобразования.
Реактивы и оборудование: штатив с пробирками, колбы, мерные цилиндры, термометр, линейка, водяная баня, химические весы, желатин, крахмал, зерно, печенье, 0,025 % растворы HCL и NaOH, 0,1 % растворы NaCL, KCL, K2SO4, KCNS.
Теоретическая часть
Полимеры подобно низкомолекулярным веществам обладают избирательной растворимостью. Растворению полимера предшествует набухание. Набухание зависит, как от природы полимера, так и от природы жидкости. Полярные полимеры набухают в полярных жидкостях, а неполярные — в неполярных.
С повышением температуры скорость набухания увеличивается. Тепловой эффект, сопровождающий набухание полимера в жидкости, называется теплотой набухания.
Растворы высокомолекулярных веществ способны терять текучесть и застудневать, образуя при этом студни. Студнеобразное состояние вещества можно рассматривать как промежуточное между жидким и твердым состоянием. Застудневание связано с увеличением вязкости и замедлением броуновского движения и заключается в объединении частиц дисперсной фазы в форме сетки или ячеек и связывании при этом всего растворителя.
С повышением концентрации способность к застудневанию увеличивается, т.к. при этом уменьшается расстояние между частицами. Процесс застудневания даже при низкой температуре не происходит мгновенно и нередко требует продолжительного времени для формирования ячеистой объемной сетки.
Время, необходимое для застудневания, называется периодом созревания.
Продолжительность созревания зависит от природы веществ, концентрации, температуры.
Экспериментальная часть
Ознакомьтесь с правилами по технике безопасности при работе в химической лаборатории и распишитесь в журнале по ТБ.
Ход работы
Опыт 1. Кинетика набухания зерна
Зерновые культуры (пшено, рис, лучше дробленый) ограниченно набухают в воде. Зерно насыпают в пробирки (1/3) так, чтобы во всех пробирках было одинаковое количество зерна по высоте. Наливают дистиллированную воду, чтобы вместе с зерном пробирки были заполнены на ¾ объема. Наблюдения за процессом набухания проводят в течение 40-50 минут. Полученные данные заносят в таблицу 1 по образцу:
Таблица № 1
| Зерно | Условный объем набухающего зерна за время, мин. | |||||
| 0 | 10 | 20 | 30 | 40 | 50 | |
| Пшено | | | | | | |
| Рис | | | | | | |
| Рис дробленый | | | | | | |
Опыт 2. Влияние кислоты, щелочи и солей на набухание желатины
В семь пробирок одинакового диаметра вносят по 0,3 г. порошка желатины. В каждую пробирку наливают по 5 мл различных растворов (см. табл. № 2). Пробирки осторожно встряхивают, чтобы частицы желатины опустились на дно, определяют высоту осадка желатины до набухания. После этого, встряхнув пробирки несколько раз, оставляют их в покое на 40-50 мин. По истечении этого времени каждую пробирку еще раз встряхивают, дают осадку осесть, измеряют высоту набухшего осадка желатины (с каждой пробиркой измерения повторяют 2 раза). Данные заносят в таблицу 2.
Таблица № 2
| № пробирки | Концентрация, моль/л | Приливаемый раствор | Высота осадка, мм | |
| до набухания | после набухания | |||
| 1 | - | Вода | | |
| 2 | 0,025 | HCL | | |
| 3 | 0,025 | NaOH | | |
| 4 | 0,1 | NaCL | | |
| 5 | 0,1 | KCL | | |
| 6 | 0,1 | K2SO4 | | |
| 7 | 0,1 | KCNS | | |