Файл: Практическая работа Расчеты составов газовых смесей Дисциплина Химическая технология нефти и газа.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.01.2024
Просмотров: 110
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
| ФИО | Группа | Дата | Вариант |
| | | | |
Практическая работа № 1. Расчеты составов газовых смесей
Дисциплина «Химическая технология нефти и газа».
Расчеты составов и свойств газовых смесей
Задание 1.1. Смешение газовых потоков
Производится смешение двух газовых потоков: потока № 1 и потока № 2.
Состав потоков известен (см. таблицу).
| Содержание вещества, об. % | CH4 | C2H6 | C3H8 | C4H10 | C5H12 | CO2 | H2S | CH3SH | N2 |
| Поток № 1 | 90,6 | 3,7 | 1,1 | 0,5 | 0,5 | 0,3 | 0,9 | 0,3 | 2,1 |
| Поток № 2 | 77,2 | 5,5 | 1,6 | 1,1 | 2,9 | 1,1 | 2,9 | 0,9 | 6,8 |
Отношение объемных расходов потоков известно (см. таблицу).
| Вариант | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| Отношение объемных расходов потоков № 1 и № 2 | 7:1 | 6:1 | 5:1 | 4:1 | 3:1 | 2:1 | 1:1 | 1:2 | 1:3 | 1:4 | 1:5 | 1:6 | 1:7 | 1:8 | 1:9 |
Для газового потока, получаемого при смешении, определите:
- объемный состав;
- массовый состав;
- плотность газа как идеального газа (при н.у.);
- мольный объем газа как идеального газа (при н.у.);
- молярную массу газа;
- относительную плотность газа по воздуху;
- содержание S (г/нм3);
- содержание H2S (г/нм3);
- парциальное давление газов в смеси.
Дополнительные данные:
Давление газового потока смешения — 1,75 МПа. Молярная масса воздуха — 29 г/моль. Нормальные условия: 101325 Па, 0 °С.
Задание 1.2. Расчет энтальпии газовой смеси
При практических расчетах большое значение имеет расчет изменения энтальпии газов и жидкостей в результате различных процессов. Однако зачастую для определения теплового баланса какого-либо аппарата необходимо знать начальное и конечное значения энтальпии потока, проходящего через аппарат.
Энтальпия идеального газа (
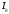 , кДж/кг) при температуре Т и атмосферном давлении рассчитывается по уравнению
, кДж/кг) при температуре Т и атмосферном давлении рассчитывается по уравнению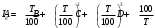 (1)
(1)где А, В, С, D — коэффициенты, значения которых приведены в справочниках (табл. 1).
Энтальпия паров нефтепродуктов и углеводородных газов с повышением давления снижается. Разность энтальпий при атмосферном и повышенном давлении
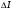 является функцией приведенных температуры и давления:
является функцией приведенных температуры и давления: 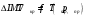 — и определяется по графикам (см. рис. 1). По известной поправке
— и определяется по графикам (см. рис. 1). По известной поправке 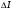 находится энтальпия при повышенном давлении
находится энтальпия при повышенном давлении 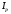 :
: 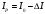 .
.Приведенные температура
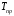 и давление
и давление 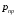 рассчитываются по известным критическим (псевдокритическим) свойствам:
рассчитываются по известным критическим (псевдокритическим) свойствам: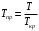
(2)
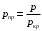 , (3)
, (3)где
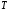 — температура, при которой находится рассматриваемый газ (размерность такая же, как у критической температуры);
— температура, при которой находится рассматриваемый газ (размерность такая же, как у критической температуры); 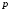 — давление, при котором находится рассматриваемый газ (размерность такая же, как у критического давления).
— давление, при котором находится рассматриваемый газ (размерность такая же, как у критического давления).Энтальпия смеси газов или паров нефтепродуктов, как и теплоемкость, рассчитывается по правилу аддитивности.


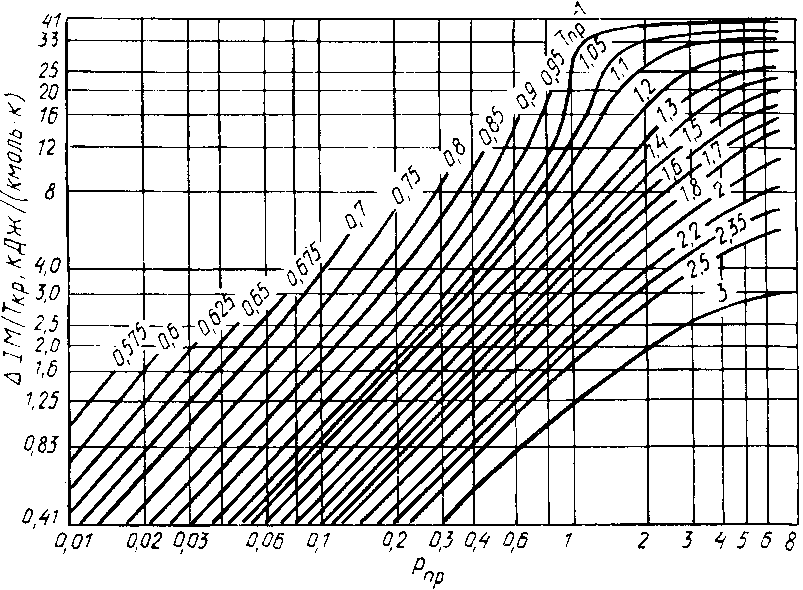
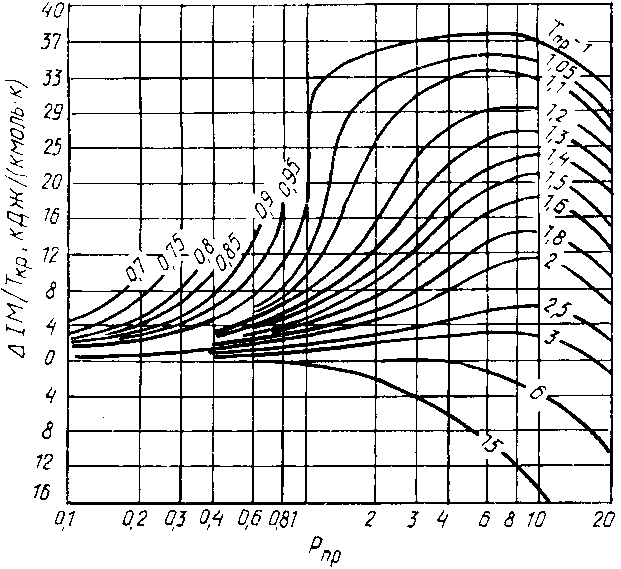
Рисунок 1 — График для определения поправки
 к энтальпии идеальных газов и паров нефтепродуктов (
к энтальпии идеальных газов и паров нефтепродуктов ( , кДж/кг; М, кг/кмоль)
, кДж/кг; М, кг/кмоль)Задание.
В компрессоре производится сжатие ВСГ заданного состава, начальные температура и давление известны (см. таблицу 2). Температура на выходе компрессора — 18 °С, давление на выходе компрессора 3,1 МПа.
Рассчитайте энтальпию ВСГ как идеального газа на входе в компрессор и на выходе из компрессора. Изменением состава ВСГ при прохождении компрессора пренебречь.
Таблица 1 — Справочные данные для расчета
| Газы | Критическая температура, К | Критическое давление, атм | А, кДж/кг | В, кДж/кг | С, кДж/кг | D, кДж/кг |
| Водород | 32,98 | 12,9 | 82,27 | 2,54 | 0,013 | 25,12 |
| Метан | 190,56 | 45,9 | 154,15 | 15,12 | 0,051 | 59,62 |
| Этан | 305,33 | 48,7 | 58,65 | 23,63 | 0,414 | 56,15 |
| Пропан | 369,85 | 42,5 | 33,65 | 26,31 | 0,538 | 35,58 |
Таблица 2 — Исходные данные
| Вариант | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| Состав ВСГ, % мольн. | | | | | | | | | | | | | | | |
| Водород | 92 | 90 | 89 | 95 | 88 | 87 | 85 | 94 | 91 | 88 | 85 | 89 | 90 | 96 | 93 |
| Метан | 5 | 6 | 6 | 3 | 5 | 6 | 7 | 2 | 3 | 5 | 10 | 6 | 5 | 2 | 3 |
| Этан | 2 | 3 | 4 | 1 | 4 | 4 | 4 | 2 | 3 | 4 | 3 | 3 | 4 | 1 | 2 |
| Пропан | 1 | 1 | 1 | 1 | 3 | 3 | 4 | 2 | 3 | 3 | 2 | 2 | 1 | 1 | 2 |
| Температура на входе в компрессор, °С | 35 | 40 | 28 | 20 | 25 | 32 | 40 | 42 | 37 | 32 | 45 | 50 | 40 | 35 | 36 |
| Давление на входе в компрессор, МПа | 1,9 | 1,8 | 0,9 | 1,0 | 2,2 | 1,6 | 1,6 | 1,5 | 1,5 | 1,8 | 1,9 | 2,0 | 2,1 | 2,0 | 1,4 |
Задание 1.3. Расчет теплоемкости газовой смеси
Для газов различают теплоемкость, определяемую при постоянном давлении (изобарная теплоемкость) Ср и при постоянном объеме (изохорная теплоемкость) Сv. Эти теплоемкости идеальных газов связаны между собой соотношением
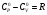 (индекс 0 означает нормальное давление). В технологических расчетах преимущественно используются изобарные теплоемкости газов, значения которых при нормальных условиях приведены в справочниках. Теплоемкость газов слабо зависит от давления, часто этим влиянием в расчетах пренебрегают. При повышении температуры теплоемкость газов увеличивается.
(индекс 0 означает нормальное давление). В технологических расчетах преимущественно используются изобарные теплоемкости газов, значения которых при нормальных условиях приведены в справочниках. Теплоемкость газов слабо зависит от давления, часто этим влиянием в расчетах пренебрегают. При повышении температуры теплоемкость газов увеличивается. Теплоемкость газов (как идеальных) определяется по формуле (Дж/моль К):
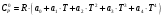 (1)
(1)где a0, a1, a2, a3, a4 — коэффициенты.
Поправка теплоемкости на давление (кДж/кг К) рассчитывается по формуле
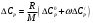 (2)
(2)где
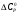 ,
, 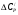 — безразмерные поправки, определяемые по графикам (рис. 1-2) в зависимости от приведенных давления и температуры; M— молярная масса, кг/кмоль; — фактор ацентричности.
— безразмерные поправки, определяемые по графикам (рис. 1-2) в зависимости от приведенных давления и температуры; M— молярная масса, кг/кмоль; — фактор ацентричности.Соответственно, теплоемкость при давлении, отличном от атмосферного:
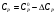
Фактор ацентричности приведен в справочниках. Фактор ацентричности — безразмерная величина. Правило аддитивности действует и при расчете теплоемкости газовой смеси, и при расчете фактора ацентричности газовой смеси.
 | 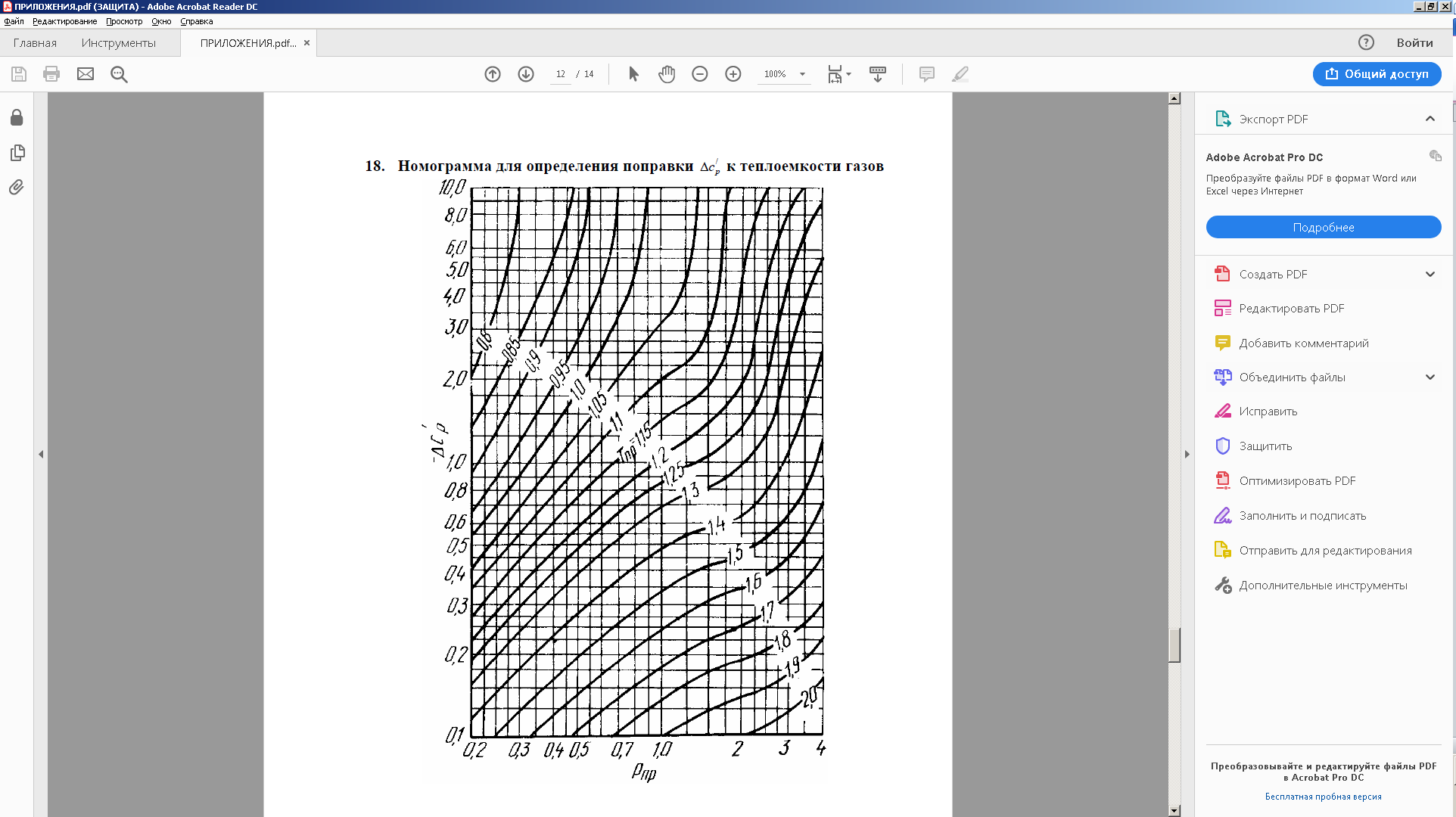 |
| Рисунок 1 — Номограмма для расчета поправки 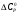 к теплоемкости газов, к теплоемкости газов, | Рисунок 2 — Номограмма для расчета поправки 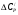 к теплоемкости газов к теплоемкости газов |