Файл: Химия нефти и газа л. 910 Методы исследования состава нефти и газа.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 39
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
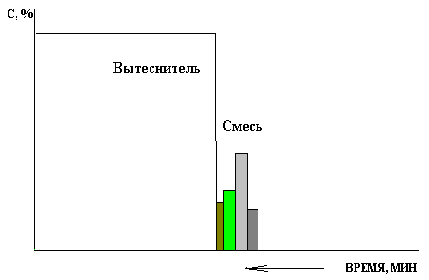
Если мы сумеем отобрать эти узкие зоны, то получим на руки отдельные компоненты смеси. Чтобы узнать концентрации отдельных веществ, достаточно зафиксировать их с помощью специальных детекторов.
Этим методом трудно достичь хорошего разделения смеси из-за взаимной диффузии на границе зон.
-
Фронтальная. Вариант хроматографии при котором смесь веществ непрерывно вводится с подвижной фазой до тех пор пока не выйдет самый слабосорбирующийся компонент.
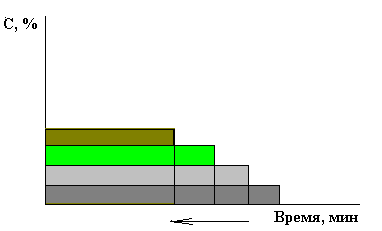
Затем из колонки начинает выходить смесь компонентов, разделяющихся
на примыкающие друг к другу зоны, в которых число компонентов постепенно увеличивается.
Именно этот вариант хроматографического разделения был известен до открытия хроматографии как метода. Цвет модифицировал именно этот метод. Он всего лишь показал, что для полного разделения смеси на компоненты нужно вводить вещество в сорбент не непрерывно, а порциями и элюирование вести чистым растворителем.
В настоящее время метод фронтального анализа практически не применяется, так как он не дает полного разделения смеси: в чистом виде элюируется только слабосорбирующийся компонент.
3. Элюентная (проявительная) – хроматография, при которой исследуемая смесь веществ вводится в поток подвижной фазы однократно или периодически и разделяется в колонке на зоны компонентов, выходящих в порядке увеличения их сорбируемости. В отличие от вытеснительной хроматографии, в элюентном варианте подвижная фаза сорбируется слабее, чем компоненты смеси.

Этот вариант получил наиболее широкое применение; при правильном выборе условий метод позволяет разделить все компоненты и проанализировать смесь.
4. Хромодистилляция. Этот метод находится на стыке хроматографии и ректификации. Смесь веществ перемещается с потоком газа-носителя вдоль колонки со стеклянными или металлическими шариками в условиях отрицательного продольного градиента температур. На заднем фронте смеси происходит испарение веществ, а на переднем – конденсация.
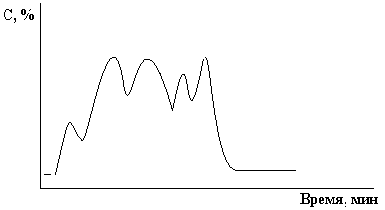
В итоге смесь разделяется на примыкающие друг к другу зоны веществ в порядке повышения их температуры кипения.
По агрегатному состоянию подвижной и неподвижной фаз методы хроматографии делятся на:
- Газовую, где подвижная фаза – газ или пар. Этот вид подразделяется на:
-
Газо-адсорбционную -
Газо-жидкостную -
Газо-мезофазную (на жидких кристаллах)
(сказать какие вещества разделяют)
- Жидкостную, где подвижная фаза – жидкость. Подразделяется:
-
Жидкостно-адсорбционную -
Жидкостно-жидкостную (ж-ж не смешиваются) -
Жидкостная-противоточная
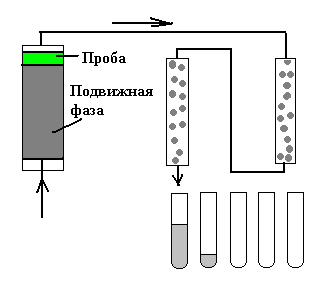
Или капельная противоточная – это жидкостно-жидкостная хроматография, в которой компоненты разделяются в потоке капель, выполняющих роль подвижной жидкой фазы. Капли проходят через колонку, заполненную неподвижной жидкой фазой, не смешивающейся с подвижной фазой.
Сначала систему заполняют неподвижной фазой. Если ее удельная масса больше, чем у подвижной, растворенную пробу вносят на дно колонки, в противном случае – в верхнюю часть колонки. Подвижная фаза поступает в систему через круглое капиллярное отверстие в виде маленьких капель, которыые перемещаются через неподвижную фазу (за счет разности удельных масс), что и приводит к разделению пробы между двумя фазами.
-
Сверхкритическая флюидная…
(сказать какие вещества разделяют)
По характеру взаимодействия сорбата и сорбента хроматография подразделяется на распределительную, ситовую, ионообменную, хемосорбционную.
| Механизм процесса разделения | Схема | Название |
| За счет адсорбции или растворения | 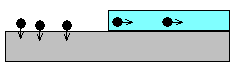 | Распределительная (молекулярная, адсорбционная) |
| По размеру молекул | 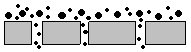 | Ситовая (декстрин-гель получают в результате ферментативного гидролиза крахмала бета-амилазой) |
| За счет ионного обмена | | Ионообменная |
| Водородные связи, Хим. сродство | | Хемосорбционная |
По способу проведения процесса
- колоночная
- капиллярная
- тонкослойная
Различают аналитический (для качественного и количественного анализа смеси) и препаративный (для выделения чистых компонентов или фракций из смеси) варианты хроматографии
При всем разнообразии хроматографии практически всегда реализуется общая схема процесса:
Подвижная фаза ввод образца разделение детектировани обработка результата
В каждом конкретном случае нужно выбирать тот метод, который позволяет решить задачу с нужной точностью и экспрессностью.
Хроматография – на сегодня самый эффективный метод разделения нефтей на группы химически однородных соединений.
С помощью хроматографии из нефти выделить отдельно парафино-нафтеновые и ароматические УВ, а последние разделить по степени цикличности.
Можно в относительно чистом виде выделить кислородные, азотные и сернистые соединения и направить на дальнейшие исследования.
На сегодняшний день хроматографические методы составляют 70-80 % от всех аналитических методов исследования нефтей.
В основе лежат многократно повторяющиеся процессы сорбции и десорбции, которые и приводят к разделению веществ. На разделяемые системы могут накладываться те или иные поля, например электрические, тепловые, гравитационные, что создает большое число возможных вариантов хроматографии.
В процессе хроматографического разделения через зернистый слой или вдоль адсорбционной поверхности постоянно протекает (фильтруется) поток подвижной фазы – жидкости или газа.
Хроматографический пик. Характеристики удерживания анализируемых веществ.
При хроматографическом разделении на выходе из хроматографической колонки фиксируется хроматографическая кривая (хроматограмма), на которой имеются:
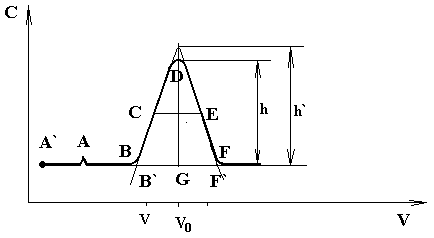
А` – точка ввода анализируемой пробы;
А – появление на выходе несорбирующегося компонента;
В – появление анализируемого вещества
Линия А`BF – нулевая линия;
Кривая BDF – хроматографический пик, характеризующийся высотой, шириной и площадью.
Пик описывает закон нарастания концентрации с от 0 до сmax и спада до 0.
| Если бы не было случайных процессов, которые, наряду с адсорбцией, действуют в хроматографии, то вещества выходили бы из колонки скачком концентрации, очень узкой зоной. Но действие молекулярной диффузии (теплового хаотичного движения молекул- Броуновское) приводит к рассеянию, размыванию пика. В результате хаотичного блуждания и сталкивания молекулы каким-то образом распределяются в пространстве. Получающееся распределение концентраций подчиняется закону распределения случайной величины (вышеуказанный закон Гаусса). |
Вещества, выходящие из хроматографической колонки, кроме формы пика, характеризуются временем удерживания или пропорциональным ему объемом удерживания Vm. На рис. это отрезок A`G. Удерживаемый объем Vm пропорционален времени удерживания tm:
Vm = tmW, (5)
где W – объемная скорость элюента.
На хроматограмме время удерживания определяется как длина отрезка A`G = L, разделенная на скорость записи хроматограммы U:
tm = L/U (6)
Если засечь по секундомеру время выхода максимума пика не от начала хроматограммы, а от максимума пика несорбирующегося компонента, то это будет не абсолютное, а приведенное время удерживания tr:
tr = tm - to (7)
и соответственно можно получить приведенный объем удерживания:
Vr = Vm - Vo (8)
эта величина не зависит от условий разделения, а определяется только природой сорбента, разделяемого вещества и температуры. Если измерить эту величину для разных веществ и занести в справочники, то по ней можно проводить идентификацию веществ на хроматограмме.
Качественный и количественный хроматографический анализ
Основные задачи качественного анализа:
- определение количества индивидуальных веществ на хроматограмме;
- выполнение группового анализа;
- полная идентификация компонентов.
Приемами идентификации веществ являются:
-
Определение характеристик удерживания веществ в колонке (объема удерживания или времени удерживания или относительных индексов удерживания) и сравнение их с приведенными в литературе значениями. Условия опыта не должны отличаться от тех, в которых были получены табличные данные. -
идентификация по эталонным веществам;
в простейшем варианте он реализуется как метод добавки: сравниваются две полученные в одинаковых условиях хроматограммы – исходного образца и образца с добавкой вещества-эталона. Если на второй хроматограмме появился дополнительный пик, это означает, что в анализируемой смеси добавленное эталонное соединение отсутствует. Если один из пиков, имеющийся на первой хроматограмме, увеличился в размере на второй, то, вероятно, добавляемое эталонное соединение присутствует и в анализируемой смеси. Однако следует учитывать, что, если добавляемое эталонное соединение входит в состав исследуемой смеси, на второй хроматограмме увеличится высота соответствующего пика, а ширина пика у основания останется неизменной. Если же одновременно имеет место и изменение ширины пика у основания, то добавляемое эталонное соединение относится к другому классу соединений и имеет место простое совпадение параметров удерживания этих соединений. В этой связи для повышения надежности заключения следует повторить опыты по разделению на нескольких неподвижных фазах, отличающихся по своим характеристикам. Количество добавляемого эталона должно примерно соответствовать количественному содержанию идентифицируемого компонента в анализируемой пробе. При больших добавках пик эталона может наложиться на несколько пиков первоначальной хроматограммы.
-
использование селективных детекторов -
К наиболее трудоемким методам относится сбор веществ, выходящих из колонки и анализ их физико-химическими методами – пример – хромато-масс-спектрометрия.
Задачей количественного хроматографического анализа является определение концентрации анализируемого вещества в пробе.
В основу количественных методов газовой хроматографии положены два допущения:
-
введенная в хроматограф проба имеет тот же состав, что и анализируемый раствор. При этом концентрация вещества выражается уравнением С = qi/qn , где qi - количество определяемого компонента в анализируемой пробе; qn – размер пробы. -
количество i-того компонента в пробе пропорционально параметру пика Хi этого компонента на хроматограмме: qi = ki Xi.
Отсюда следует основное уравнение количественной газовой хроматографии
С = kiXi/qn
Величина ki называется абсолютным калибровочным коэффициентом.
Таким образом задача количественного анализа сводится к определению двух множителей основного уравнения (количество вводимой пробы qn мы обычно знаем).
Нам нужно определить Xi – параметр хроматографического пика – это графическая величина связанная с количеством вещества, соответствующего данному пику.
На практике используют три основных параметра хроматографического пика:
-
1) высота пика h; -
2) произведение высоты пика h на время удерживания t или пропорциональное ему расстояние на хроматограмме от момента ввода пробы до регистрации максимума пика l, т.е. h t или h l; -
3) площадь пика А или величины, приближенно характеризующие ее значение.
Считается, что применение любого из этих параметров для количественных измерений должно давать одинаковые результаты. Метод обсчета выбирают исходя из задач и условий хроматографирования. Главные требования:
-
Должна быть линейность связи измеряемого параметра с концентрацией -
Должна быть обеспечена простота и точность измерения параметра.
Чаще всего применяют метод измерения площади пика. Существуют автоматические методы измерения площади и выполняемые вручную.
Вручную:
-
Вырезания и взвешивания – удобен и точен для определения площади асимметричных пиков и сильно перекрывающихся -
приближенные методы:
-
Произведение высоты пика на ширину пика на половине высоты (hb); -
Произведение высоты пика на среднее значение ширины пика, измеренной на нескольких уровнях; -
Разбивка на простые фигуры (трапеции, прямоугольники, треугольники); -
Измерение площади треугольника, образованного пересечением касательных в точках перегиба кривой. Иногда этот метод называют методом описанного треугольника и др.