Добавлен: 12.01.2024
Просмотров: 127
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Содержание
| Введение | 3 |
| 1 Теоретические основы паровой конверсии метана | 4 |
| 2 Способы паровой конверсии метана | 6 |
| 2.1 Оборудование для проведения процесса паровой конверсии метана | 8 |
| 2.2 Механизм реакций конверсии | 16 |
| 3 Схема трубчатой печи 1 – ой ступени паровой конверсии метана | 18 |
| Заключение | 20 |
| Список используемых источников | 21 |
Введение
Получаемый в промышленности синтез-газ представляет собой смесь водорода, окиси углерода и диоксида углерода. Он может также содержать азот в том виде, в каком он применяется для производства аммиака. Синтез-газ является ключевым промежуточным продуктом в химической промышленности. Он может быть использован в ряде высокоселективных синтезов различных химических веществ и топлива, а также в качестве источника чистого водорода и углерода монооксида. Синтез-газ играет все более важную роль в преобразовании энергии. Синтез-газ может быть получен практически из любого источника углерода, начиная от природного газа и нефтепродуктов и заканчивая углем и биомассой, путем окисления паром и кислородом.
В настоящее время природный газ используется в основном в энергетических целях: тепловые электростанции на природном газе наиболее экологически чистые, пропанобутановая фракция применяется в качестве бытового топлива, а также как горючее для автотранспорта. В небольших количествах метан используют в металлургической промышленности как восстановитель. Однако степень химической переработки природного газа в ценные продукты остается на низком уровне, а значительная часть попутного нефтяного газа сжигается в факелах, что приводит к невосполнимой потере ценного сырья и порождает сложные экологические проблемы в регионах добычи. Столь расточительное отношение к ископаемым источникам сырья недопустимо и требует незамедлительного создания новых технологий переработки легкого углеводородного сырья.[1]
В настоящее время конверсия метана является основным промышленным методом получения водорода и технологических газов для синтеза аммиака, спиртов и других продуктов. Известны различные способы конверсии метана. От метода конверсии зависят как технологическая, так и энергетическая схемы производства аммиака в целом. Для выбора оптимального варианта необходимо знать состав конвертированного газа, его энтальпию и эксэргию.
Расчет равновесных составов конвертированного газа на основе известных методик требует использования ЭВМ и соответствующего программного обеспечения. Для упрощения этой задачи целесообразно построить номограммы для определения содержания отдельных компонентов в конвертированном газе, а также номограммы для нахождения его энтальпии и эксэргии. В литературе приведены номограммы только для паровой конверсии метана, однако, имеется возможность построения подобных номограмм и для других способов конверсии. [1]
Задачей представленной работы является: Изучение существующих промышленных способов получения водорода, в т.ч. процесса парового риформинга природного газа. Рассмотрение основных параметров процесса и применяемого технологического оборудования.
1 Теоретические основы паровой конверсии метана
Паровая конверсия метана – это процесс, в котором метан из природного газа нагревается паром, обычно в присутствии катализатора, для получения смеси монооксида углерода и водорода, используемых в органическом синтезе или в качестве топлива. В энергетике паровой риформинг является наиболее широко используемым процессом для получения водорода.
В описываемом процессе метан реагирует с паром под давлением 3-25 бар в присутствии катализатора с образованием водорода, оксида углерода и относительно небольшого количества углекислого газа. Реакция парового риформинга является эндотермической, т.е. е. для протекания реакции необходимо подавать тепло в процесс. Паровая конверсия метана является наиболее широко используемым процессом для получения водорода. Это в значительной степени связано с его экономической эффективностью при получении водорода высокой степени чистоты. Водород, полученный из природного газа конверсией, может быть использован в промышленных процессах (в частности, производстве аммиака) и топливных элементах [2].
Риформинг обычно осуществляется в многотрубчатых реакторах с неподвижной стационарной фазой, вставляемых в крупные газовые печные установки для обеспечения необходимой энергией. Процесс работает под высоким давлением на поверхности коммерческого катализатора на основе никеля с временем контакта более одной секунды. Паровой риформинг метана состоит из трех обратимых реакций: сильно эндотермических реакций риформинга (1,3) и реакции 2 умеренно экзотермического водо-газового сдвига:
СH4+H2OCO+3H2 (1)
CO+H2OCO2+H2 (2)
СH4+H2O CO2+4H2 (3)
Углекислый газ образуется не только в реакции сдвига 2, но также непосредственно в реакции 3 риформинга с водяным паром. Фактически реакция 3 является результатом сочетания реакций 1 и 2. Из-за эндотермического поведения процесса риформинга природного газа с водяным паром предпочтительной является высокая температура. Кроме того, т.к. происходит увеличение объема, предпочтение отдается низкому давлению. Напротив, экзотермической реакции 2 благоприятна низкая температура, при этом изменение давления не оказывают на нее никакого влияния. Реакции риформинга 1 и реакции конверсии связанного водяного газа 2 обычно проводят на никелевом катализаторе на носителе при повышенных температурах, обычно выше 500 ° С.
Реакции 1 и 3 являются обратимыми и обычно достигают равновесия в присутствии активного катализатора и при высоких температурах. Весь продуктовый газ представляет собой смесь моноксида углерода, диоксида углерода, водорода и непревращенных метана и пара. Температура реактора, рабочее давление, состав подаваемого газа и доля пара, подаваемого в реактор, определяют продукт процесса. Количество оксида углерода, получаемого в результате паровой конверсии метана, достаточно велико; потому что реакция сдвига водяного газа, показанная в уравнении 2, является термодинамически выгодной при более высоких температурах. Количество оксида углерода в конечном продукте парового риформинга метана определяется термодинамикой и кинетикой реакции.
Паровой риформинг является наиболее важным путем для крупномасштабного производства синтез-газа для аммиака, этанола и других продуктов нефтехимии, а также для производства водорода для нефтеперерабатывающих заводов. Как правило, реакции риформинга катализируются металлами группы 8-10, причем никель является предпочтительным металлом для промышленного применения из-за его активности, доступности и низкой стоимости. Метан активируется на поверхности никеля.
2 Способы и катализаторы паровой конверсии метана
Хотя водород можно получить путем риформинга природного газа, нафты, тяжелого мазута или угля, более высокое атомное отношение водород/углерод в метане по сравнению с другими молекулами позволяет предположить, что природный газ, содержащий большое количество метана в своем составе, является лучшим углеводородным сырьем [3].
Природный газ реагирует с паром на никелевом катализаторе при температуре 1200 K и общем давлении 20-30 атмосфер. Учитывая, что природный газ содержит сернистые примеси, во избежание деградации катализатора необходима предварительная очистка. Чистый поток метана затем проходит поступает в реактор, загруженный никелевым катализатором. Образующийся газ отличается высоким содержанием водорода, но содержит часть окиси углерода, которая, в свою очередь, преобразуется во втором или третьем реакторе для получения дополнительного водорода в результате реакции с водяным паром. Получаемый газ в основном состоит из водорода, но содержит также двуокись углерода и небольшое количество неконвертированного метана, а также следы окиси углерода (обычно 1% по объему). Действующие установки производства водорода включают установки компрессии/абсорбции/десорбции, позволяющие получать водород высокой чистоты (99.999% по объему).
Поскольку природный газ содержит небольшую долю других углеводородов, таких как этан, пропан и бутан, которые легко разлагаются для образования углеродных остатков в процессе риформинга метана (метан является основным компонентом), то для преобразования части углеводородов, присутствующих в природном газе, в смесь CO/H2 необходима предварительная стадия риформинга (дореформинга). Этот процесс проводится перед установкой риформинга и позволяет работать с разнообразным сырьем, обеспечивая постоянную подачу сырья. Предварительный риформинг оказывает большое влияние на состав газа, подаваемого на установку парового риформинга. Таким образом, при конверсии фракции метана полностью удаляются длинноцепочечные углеводороды. Учитывая, что эти длинноцепочечные углеводороды имеют тенденцию к образованию углерода, данный процесс предварительного реформирования сводит к минимуму образование кокса при реформировании метана. Это приводит к увеличению срока службы используемых каталитических систем.
Пар, используемый в реакции парового риформинга, может быть заменен углекислым газом, кислородом или их смесью. Также возможно использовать метанол для промышленного производства водорода вместо метана. В этом процессе метанол вступает в реакцию с паром над катализатором для получения H2. Это эндотермическая реакция, поэтому необходимое тепло образуется при сжигании хвостового газа вместе с небольшой фракцией метанола. Поток водорода, как и в случае метанового риформинга, очищается в абсорбционной установке.
В общем, реакции риформинга катализируются металлами 8-10 группы, причем никель является предпочтительным металлом для промышленного применения из-за его доступности и низкой стоимости [4]. Никелевые катализаторы, обладающие достаточно высокой каталитической активностью и дешевой стоимостью, получили широкое распространение используется в метановом риформинге.
Никелевые системы могут использовать в качестве носителей различные оксиды металлов, такие как Al2O3, MgO, CeO2, или La2O3. Как сообщалось, катализаторы на основе Ni в процессе риформинга склонны к спеканию при высокой температуре и под воздействием осаждения углерода, что может привести к их дезактивации во время реакции. Катализаторы риформинга должны отвечать строгим требованиям, таким как высокая активность, разумный срок службы, хорошая теплопередача, низкий перепад давления, высокая термическая стабильность и отличная механическая прочность. Кроме того, необходимо снижать затраты на разработку процессов парового риформинга метана. Разработка новых катализаторов с четко определенными свойствами является фундаментальной для достижения этих целей: на самом деле катализатор должен активировать метан при низкой температуре, он должен приводить доводить его превращение до величин равновесия при коротком времени контакта, и, кроме того, он должен быть устойчив к деактивационным факторам (в том числе образование углерода).
2.1 Оборудование для проведения процесса паровой конверсии метана
Процесс риформинга с водяным паром является хорошо отработанным каталитическим процессом, который превращает природный газ или легкие углеводороды в смесь, содержащую в своем составе водород, монооксид углерода и диоксид углерода (синтез-газ). Процесс риформинга с водяным паром приобретает все большее значение с ростом спроса на различные типы синтез-газов для химической и нефтехимической промышленности.
В промышленности реакции риформинга обычно проводят в нагретой печи над никелевым катализатором. Пример такого трубчатого риформера показан на рисунке 1. Такие риформеры сегодня обеспечивают производительность до 300 000 м3/ч Н2. Печь состоит из радиантной секции коробчатого типа, включающей горелки, и конвекционной секции, для рекуперации тепла отходящих газов, покидающих секцию радианта.
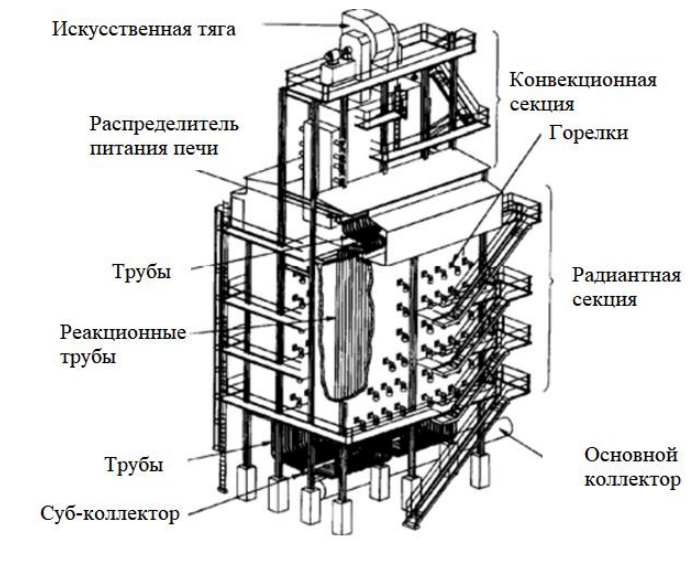
Рисунок 1 – Общий вид печи риформинга