Файл: Курсовая работа по дисциплине Химическая технология органических веществ Исполнитель.docx
Добавлен: 12.01.2024
Просмотров: 85
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Тепловые потери от прихода тепла, - 5,0
Таблица 3 – Термодинамические свойства веществ участников реакции
| Вещество | ΔH, кДж/моль | a | b∙103 | c∙106 | c'∙10-5 |
| C3H6 | 20,41 | 12,44 | 188,38 | -47,60 | --- |
| C3H8 | -103,85 | 1,72 | 270,75 | -94,48 | --- |
| C3H8O | -257,53 | 13,10 | 277,5 | -98,44 | --- |
| H2O | -241,81 | 30,00 | 10,71 | --- | 0,33 |
| C6H14O | -318,52 | 7,49 | 583,95 | -302,2 | --- |
1. Рассчитаем количество тепла поступившего с исходными реагентами.

Gi-количество веществ исходного выражения в [кмоль]
Ti=273+100=373K
Cpi=a+bT+cT2+dT3 (для органических веществ)
Cpi(C3H6)=12.44+188.38∙10
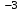 ∙373+(-47.6)∙10-6∙373
∙373+(-47.6)∙10-6∙373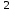 =76.083 Дж/моль к
=76.083 Дж/моль кQi(C3H6)=42,66∙76,083∙373 = 508550,945 кДж/ч
Сpi(C3H8)=1,72+270,75∙10-3∙373-94,48∙10-6/3732=89,565 Дж/моль к
Qi(C3H8)=4,16∙89,565∙373 =17706,105 кДж/ ч
Cpi(H2O)=30+10.71· 10-3 ·373+0.33 ·105 373-2=34,232 Дж/моль к
Qi(H2O)=177,54 · 34,323· 373=686436,495 кДж/ ч
Qi= Qi(C3H6)+ Qi(C3H8) +Qi(H2O)= 508550,945+17706,105+686436,495 =1212693,545 кДж/ч
2. Рассчитать количество тепла уходящая с продуктами реакции.
Qj=Gj∙Cpj∙Tj
Tj=513 К
Cp(C3H6непр)=12,44+188,38∙10-3∙513-47,6∙10-6∙5132=96,552 Дж/моль∙К
Qj(C3H6непр)=1,97∙96,552∙513=97576,417кДж/ч
Cp(H2Oнепр)=30+10,71∙10-3∙513+0,33∙105∙5132=35,619Дж/моль∙К
Qj(H2Oнепр)=39,32∙35,619∙513=718476,548кДж/ч
Cp(C3H8)=1,72+270,75∙10-3∙513-94,48∙10-6 ∙5132=115,751 Дж/моль∙К
Qj(C3H8)=4,16 ∙115,75· 513=31471,539 кДж/ч
Cp(C6H14O)=7,49+583,95∙10-3∙513-302,2∙10-6∙ 5132=227,526 Дж/моль∙К
Qj(C6H14O)=53,01∙227,526∙513=177415,674 кДж/ч
Cp(C3H8O)=13,10+277,5∙10-3∙513-98,44∙106/5132=129,552 Дж/моль∙К
Qj(C3H8O)=42,66∙129,552∙513=858665,474 кДж/ч
∑Qj=Qj(C3H6непр)+Qj(H2Oнепр)+Qj(C3H8)+Qj(C6H14O)+Qj(C3H8O)=97576,417+718476,548+31471,539+177415,674+858665,474=1883605,652 кДж/ч
3. Рассчитаем количество тепла выделенное или поглощенное в ходе химической реакции.
А)Для основной реакции:
Qr=-∆Hr,t∙G
G=0,1525 кмоль/мин
T=753K
∆H0298=∆Hпрод-∆Hисх
∆H0298=-257,53+241,81-20,41=-36,13 103 кДж/моль
∆a= (νапр)- ( νаисх)
∆b= (νbпр)- ( νbисх)
∆c= (νcпр)- ( νcисх)
∆c/ = (νc/ пр)- ( νc/ исх)
∆a=a(C3H8O)-(a(C3H6)+ a(H2O)) =13,10-12,44-30=-29,34
∆b=b(C3H8O)-(b(C3H6)+b(H2O))=(277-10,71-188,38)∙10-3=78,41∙10-3
∆c= c(C3H8O)-(c(C3H6)+c(H2O))=(-98,44+47,6)10-6=-50,84∙10-6
∆c'=-0,33∙105
∆Hr,t=ΔH298+Δa(T-298)+Δb/2(T2-2982)+Δc/3(T3-2983)+Δd/4(T4-2984)+
+Δc'(1/298-1/T)
∆Hr,513=-36130+(-29,34)(513-298)+78,41∙10-3/2(5132-2982)-(50,84∙10-6) /3(5133-2983)-0,33∙105(1/513-1/298)=-37487,895 Дж/моль
Qr=37487,895∙42,44 =484343,6 кДж/ч
Б)Для поболчной реакции
G=1,52
∆H0298 =-318,52-(2· 20,41-241,81)=-117,53 103 Дж/моль
∆a=a(C6H14O)-(2a(C3H6)+a(H2O))=7,49-(2· 12,44+30)=-47,39
∆b=b(C6H14O)-(2b(C3H6)+b(H2O))=(583,95-(2·188,38+10,71))∙10-3=196,48· 10-3
∆c=c(C6H14O)-(2c(C3H6)+c(H2O))=(-302,2-(2(-47,6)+0))∙10-6 =-207· 10-6
∆c'= -c'(H2O)=-0,33 ∙105
∆Hr,513=-177,53·103-47,79 ·215+196,48 ·10-3/2 (174365)-207· 10-6 ·108542105-46,41 =-118211,04 Дж/моль
Qr=118211,04·1,52Дж/моль
Qг= Qrосн+Qrпоб =484343,6+179680,78= 664024,38 кДж/ч
4. Рассчитаем количество тепла идущее на нагрев исходных веществ до температуры химической реакции.
Qiнагр=Gi∙Cpi∙(Tj-Ti)
Cpi- рассчитываем, исходя из средней температуры.
Tср=Tj+Ti/2=(513+373)/2=443K
Cpi(C3H6)=12.44+188.38∙10
 ∙443+(-47.6)∙10-6∙443
∙443+(-47.6)∙10-6∙443 =86,552Дж/моль к
=86,552Дж/моль кQнагр
(C3H6)=17,92∙86,552∙140=217141,658 кДж/ч
Cp(C3H8)=1,72+270,75∙10-3∙443-94,48∙10-6 ∙4432=103,12 Дж/моль к
Qнагр(C3H8)=0,53∙103,12∙140=7651,504 кДж/ч
Cpi(H2O)=30+10.71· 10-3 ·443+0.33 ·105 443-2=34,913 Дж/моль
Qiнагр(H2O)=53,76· 34,913·140=262769,2 кДж/ ч
Qiнагр=217141,658+7651,504+262769,2=487562,362 кДж/ч
5. Рассчитаем количество тепла составляющего потери от прихода.
Qпотери=%потерь∙Qприх
Qприх=Qi+Qr=1212693,545 +664024,38 =1876717,925 кДж/ч
Qпотери=0,05∙1876717,925=93835,896кДж/ч
6. Определим тепловую нагрузку на реактор т.е.рассчитаем количество тепла отводимого или приводимого химической реакции.
Qf=Qрасх-Qприх
Qрасх=∑Qj +∑Qпотер+∑Qiнагр
Qрасх=1883605,652+93835,896+487562,362=2465003,91 кДж/ч
Qf=2465003,91-1876717,925=588285,985 кДж/ч
Qf>0 реакция экзотермическая, надо подводить тепло в этом количестве.
7. Рассчитаем поверхность теплообмена реактора.
F=Qf/Kt∙Δt
Kt- коэффициент теплопередачи.
Δt-разность температур.
Kt=100
Δt=513-373=140 К
F=588285,985∙103∙(1400∙100· 3600)=11,67 м2
Таблица 4 – Тепловой баланс реакции
| Приход | Расход | ||||
| Теплов.потери | кДж/мин | % | Теплов.потери | кДж/мин | % |
| Qi | 1212693,545 | 49,2 | Qj | 1883605,652 | 76,41 |
| Qr | 664024,38 | 26,94 | Qiнагр | 487562,362 | 19,78 |
| Qf>0 | 588285,985 | 23,86 | Qпотер | 93835,896 | 3,81 |
| итого | 2465003,91 | 100 | итого | 2465003,91 | 100 |
Вывод: в ходе проведенных расчетов установлено, что для поддержания заданной температуры реакции необходимо подводить теплоту в количестве 588285,985 кДж/ч процент подводимого тепла невысокий (23,86%) отсюда для данного процесса температура выбрана оптимально.
-
Механический расчет
Заключение
Список использованных источников