ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 08.11.2023
Просмотров: 41
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Все расчеты проводились в программе «Gaussian 09», в двух тестируемых средах: вода и воздух, на базисе PCM/B3LYP/6-31++G**, 298 K
. Реакции гидролиза:

Рисунок 15 Гидролиз нуклеотида (аденин содержащий)

Рисунок 16 Гидролиз нуклеотида (гуанин содержащий)

Рисунок 17 Гидролиз нуклеотида (цитозин содержащий)

Рисунок 18 Гидролиз нуклеотида (тимин содержащий)
В ходе расчетов были установлены энергии гидролиза N – гликозидных связей.
-
Аденин ∆G = -10,1 ккал/моль -
Гуанин ∆G = -11,1 ккал/моль -
Цитозин∆G = -12,4 ккал/моль -
Тимин ∆G = -17,3 ккал/моль
Расчеты проводились в двух тестируемых средах, вода и газ. Расчеты, проводимые в газовой фазе, не показали адекватных результатов, поэтому они не учитывались в анализе данных.
Итоги
-
В ряду связанных с сахарами азотистых оснований наиболее легко может гидролизоваться связи тимин-дезоксирибоза -
Наиболее корректно метод B3LYP отражает процессы гидролиза ДНК при учете воды в качестве растворителя, с использованием модели поляризуемого континуума (PCM)
Дезаминирование аденина и цитозина
Заключающим этапом моего исследования стало изучение процесса дезаминирования азотистых оснований: аденина и цитозина. Изучение термодинамики и механизма данного процесса позволит более точно предсказывать изменения в структуре ДНК, а также позволит уменьшить ошибку в выстраивании комплиментарных пар азотистых оснований.

Цитозин
Урацил
Гипоксантин
Аденин
Рисунок 19 реакции дезаминирования цитозина и аденина
Для выполнения поставленной задачи нами был выполнен поиск сайта в структурах аденина и цитозина, который участвует в процессе дезаминирования. Было установлено, что в процессе участвует лишь малый фрагмент структуры азотистых оснований.
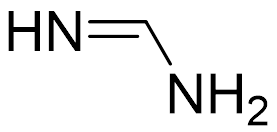
Рисунок 20 Активный центр, участвующий в процессе дезаминирования
Так как реальные модели достаточно сложны, было решено провести первые расчеты на упрощенной модели, т. е. на активном центре, участвующем в дезаминировании цитозина и аденина.
Данный процесс изучался в двух возможных условиях: с участием протонов среды и без их участия.
Также было установлено, что процесс идет под действием двух молекул воды, одна из молекул является катализатором данного процесса, а вторая атакующим реагентом.


Рисунок 21 димер воды
Рисунок 22 протонированный димер воды
Р

∆G = 10,0 ккал/моль
асчеты упрощенной модели дезаминирования проводились в программе «Gaussian 09»,в среде воды, на базисе PCM/B3LYP/6-31++G**, 298 K
∆G = 7,1 ккал/моль
Рисунок 23 Упрощенные модели процесса дезаминирования

∆G =19,3 ккал/моль
∆G = -12,1 ккал/моль
Расчеты упрощенной модели дезаминирования показали, что данный процесс способен протекать только с участием протона среды, а также с образованием комплекса NH4H2O+, так как только в этом случае энергия Гиббса принимает отрицательное значение.
После изучения процесса дезаминирования на упрощенной модели, были проведены расчеты азотистых оснований аденина и цитозина с участием протона среды и димера воды.
Р
 асчеты показали, что данный процесс является одностадийным, экзотермическим.
асчеты показали, что данный процесс является одностадийным, экзотермическим. 
Цитозин
Урацил
Аденин
Гипоксантин
Рисунок 23 схема процесса дезаминирования аденина и цитозина
Также было выяснено, что процесс дезаминирования протекает через шестицентровое переходное состояние, представленное на рисунке 23.
Энергии Гиббса процесса дезаминирвоания для аденина и цитозина:
Цитозин ∆G = -16,1 ккал/моль
Аденин ∆G = - 14,4 ккал/моль
Итоги
-
Механизм дезаминирования с наибольшей вероятностью должен протекать в протон-содержащей среде, с образованием комплекса между аммиаком и катионом гидроксония -
Процесс дезаминирования являются одностадийным, энергетически выгодным. Интермедиаты в данном процессе не образуются.
Выводы
-
В цепях нуклеиновых кислот при старении ДНК наиболее подвержены деструкции участки, содержащие гуанин. -
При деструкции цепей ДНК во время старения самым слабым звеном являются участки Г-Г и Г-Ц, причем фосфатная группа, связанная с 3 атомом углерода. -
В ряду связанных с сахарами азотистых оснований наиболее легко может гидролизоваться связи тимин-дезоксирибоза. -
Механизм дезаминирования с наибольшей вероятностью должен протекать постадийно в протон-содержащей среде. Процесс является одностадийным и термодинамически выгодным в кислых средах.