Добавлен: 25.10.2023
Просмотров: 145
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Рис.1. Условная схема фотосинтеза.
Скорость круговорота кислорода
Если какие-то отдельные процессы, входящие в данный биогеохимический цикл, могут осуществляться достаточно быстро (например, вдох и выдох в течение нескольких секунд), то целиком круговорот кислород, с учётом всех входящих в него процессов, может осуществляться около двух тысяч лет. За этот промежуток времени весь атмосферный кислород проходит через всю биосферу целиком.
Факторы, влияющие на круговорот кислорода в природе
На процессы, входящие в круговорот кислорода, прежде всего влияет сама жизнь на Земле. В основном, кислород потребляется и производится в результате жизнедеятельности живых организмов. И в первую очередь всё связано с растениями. Чем больше растений, тем активнее в результате фотосинтеза выделяется пригодного для дыхания кислорода. И наоборот, чем меньше растений (и цианобактерий, которые также способны осуществлять фотосинтез), тем больше риск превращения тех или иных участков Земли в зоны гипоксии (и такое больше свойственно океану, нежели суше).
Свойства
Физические свойства. При нормальных условиях плотность газа кислорода 1,42897 г/л. Температура кипения жидкого кислорода (жидкость имеет голубой цвет) -182,9 °C. В твердом состоянии кислород существует по крайней мере в трех кристаллических модификациях. При 20°C растворимость газа О2: 3,1 мл на 100 мл воды, 22 мл на 100 мл этанола, 23,1 мл на 100 мл ацетона. Существуют органические фторсодержащие жидкости (например, перфторбутилтетрагидрофуран), в которых растворимость кислорода значительно более высокая.
Химические свойства элемента определяются его электронной конфигурацией: [He]2s22p4 . Высокая прочность химической связи между атомами в молекуле О2 приводит к тому, что при комнатной температуре газообразный кислород химически довольно малоактивен. В природе он медленно вступает в превращения при процессах гниения. Кроме того, кислород при комнатной температуре способен реагировать с гемоглобином крови (точнее с железом (II) гема (гем - производное порфирина, содержащего в центре молекулы атом двухвалентного железа), что обеспечивает перенос кислорода от органов дыхания к другим органам. Со многими веществами кислород вступает во взаимодействие без нагревания, например, с щелочными и щёлочноземельными, вызывает образование ржавчины на поверхности стальных изделий. Без нагревания кислород реагирует с белым фосфором, с некоторыми альдегидами и другими органическими веществами. При нагревании, даже небольшом, химическая активность кислорода резко возрастает.
При поджигании он реагирует со взрывом с водородом, метаном, другими горючими газами, с большим числом простых и сложных веществ. Известно, что при нагревании в атмосфере кислорода или на воздухе многие простые и сложные вещества сгорают, причем образуются различные оксиды, пероксиды и супероксиды, такие как SO2, Fe2O3, Н2О2, ВаО2, КО2. Если смесь кислорода и водорода хранить в стеклянном сосуде при комнатной температуре, то экзотермическая реакция образования воды Н2 + О2 = 2Н2О + 571 кДж протекает крайне медленно; по расчету, первые капельки воды должны появиться в сосуде примерно через миллион лет. Но при внесении в сосуд со смесью этих газов платины или палладия (играющих роль катализатора), а также при поджигании реакция протекает со взрывом. С азотом N2 кислород реагирует или при высокой температуре (около 1500-2000 °C), или при пропускании через смесь азота и кислорода электрического разряда. При этих условиях обратимо образуется оксид азота (II): 2 + O2 = 2NO. Возникший NO затем реагирует с кислородом с образованием бурого газа (диоксида азота): NO + О2 = 2NO2 Из неметаллов кислород напрямую ни при каких условиях не взаимодействует с галогенами, из металлов - с серебром, золотом, платиной и металлами платиновой группы.
С самым активным неметаллом фтором кислород образует соединения в положительных степенях окисления. Так, в соединении O2F2 степень окисления кислорода +1, а в соединении O2F - +2. Эти соединения принадлежат не к оксидам, а к фторидам. Фториды кислорода можно синтезировать только косвенным путем, например, действуя фтором F2 на разбавленные водные растворы КОН. Применение. Применение кислорода очень разнообразно. Основные количества получаемого из воздуха кислорода используются в металлургии. Кислородное (а не воздушное) дутьё в домнах позволяет существенно повышать скорость доменного процесса, экономить кокс и получать чугун лучшего качества. Кислородное дутьё применяют в кислородных конвертерах при переделе чугуна в сталь. Чистый кислород или воздух, обогащённый кислородом, используется при получении и многих других металлов (меди, никеля, свинца и др.). Кислород используют при резке и сварке металлов. При этом применяют сжатый газообразный кислород, хранимый под давлением 15 МПа в специальных стальных баллонах. Баллоны с кислородом окрашены в голубой цвет для отличия от баллонов с другими газами. Жидкий кислород - мощный окислитель, его используют как компонент ракетного топлива. Смесь жидкого кислорода и жидкого озона один из самых мощных окислителей ракетного топлива. Пропитанные жидким кислородом такие легко окисляющиеся материалы, как древесные опилки, вата, угольный порошок и др. (эти смеси называют оксиликвитами), используют как взрывчатые вещества, применяемые, например, при прокладке дорог в горах. круговорот кислород химический элемент
Схема круговорота кислорода в природе
Кислород - основной биогенный элемент, входящий в состав молекул всех важнейших веществ, обеспечивающих структуру и функции клеток - белков, нуклеиновых кислот, углеводов, липидов, а также множества низкомолекулярных соединений. В каждом растении или животном кислорода гораздо больше, чем любого другого элемента (в среднем около 70%). Мышечная ткань человека содержит 16% кислорода, костная ткань - 28,5%; всего в организме среднего человека (масса тела 70 кг) содержится 43 кг кислорода. В организм животных и человека кислород поступает в основном через органы дыхания (свободный кислород) и с водой (связанный кислород). Потребность организма в кислороде определяется уровнем (интенсивностью) обмена веществ, который зависит от массы и поверхности тела, возраста, пола, характера питания, внешних условий и др. В экологии как важную энергетическую характеристику определяют отношение суммарного дыхания (то есть суммарных окислительных процессов) сообщества организмов к его суммарной биомассе. В жизни природы кислород имеет исключительное значение. Кислород и его соединения незаменимы для поддержания жизни. Они играют важнейшую роль в процессах обмена веществ и дыхании. Большинство организмов получают энергию, необходимую для выполнения их жизненных функций, за счет окисления тех или иных веществ с помощью кислорода. Убыль кислорода в атмосфере в результате процессов дыхания, гниения и горения возмещается кислородом, выделяющимся при фотосинтезе. Незначительное количество атмосферного кислорода участвует в цикле образования и разрушения озона при сильном ультрафиолетовом излучении: O2 → O2* O2* + O2 → O3 + O O + O2 → O3 O3 → 3O2 Большая часть кислорода, вырабатываемого в течение геологических эпох, не оставалась в атмосфере, а фиксировалась литосферой в виде карбонатов, сульфатов, оксидов железа и др. Геохимический круговорот кислорода связывает газовую и жидкую оболочки с земной корой. Его основные моменты: выделение свободного кислорода при фотосинтезе, окисление химических элементов, поступление предельно окисленных соединений в глубокие зоны земной коры и их частичное восстановление, в том числе за счет соединений углерода, вынос оксида углерода и воды на поверхность земной коры и вовлечение их в реакцию фотосинтеза. Схема круговорота кислорода в несвязанном виде представлена ниже.
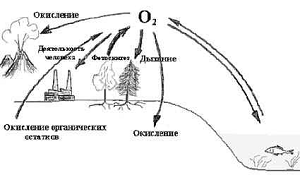
Рис.2. Схема круговорота кислорода в природе
Схема круговорота воды в природе.
Кроме описанного выше круговорота кислорода в несвязанном виде, этот элемент совершает еще и важнейший круговорот, входя в состав воды (рис. 3). В процессе круговорота вода испаряется с поверхности океана, водяные пары перемещаются вместе с воздушными течениями, конденсируются, и вода возвращается в виде атмосферных осадков на поверхность суши и моря. Различают большой круговорот воды, при котором вода, выпавшая в виде осадков на сушу, возвращается в моря путем поверхностного и подземного стоков; и малый круговорот воды, при котором осадки выпадают на поверхность океана. Из приведенных примеров круговоротов и миграции элемента видно, что глобальная система циклической миграции химических элементов обладает высокой способностью к саморегуляции, при этом огромную роль в круговороте химических элементов играет биосфера. В то же время хозяйственная деятельность человека вызывает деформацию природных циклов массообмена и, следовательно, изменение состава окружающей среды. Эти изменения происходят значительно быстрее, чем совершаются процессы генетической адаптации организмов и видообразования. Зачастую хозяйственные действия настолько непродуманны или несовершенны, что создают острую экологическую опасность. Изучение процессов массообмена, связывающих в единое целое все оболочки Земли, должно помочь в создании системы контроля за эколого-геохимическим состоянием окружающей среды и разработке научно обоснованного прогноза экологических последствий хозяйственных действий и новых технологий.
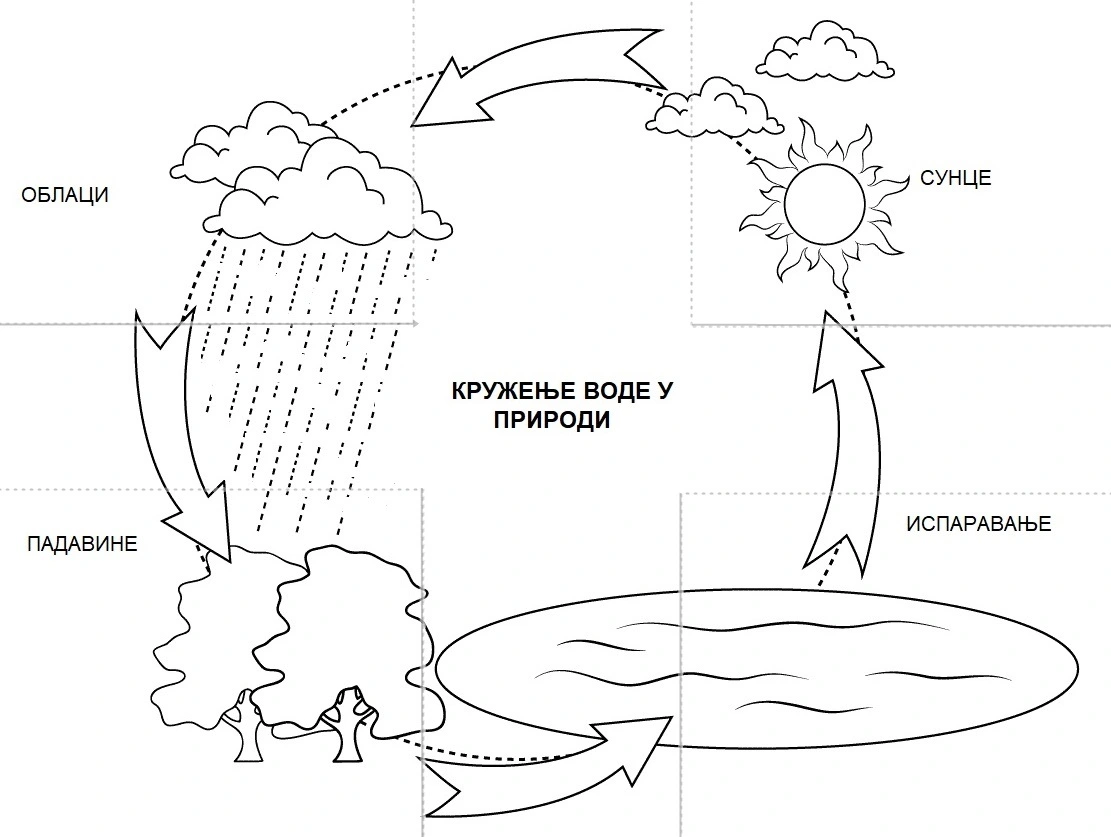
Рис,3.Схема круговорота воды в природе
Заключение
В жизни природы кислород имеет исключительное значение. Кислород и его соединения незаменимы для поддержания жизни. Они играют важнейшую роль в процессах обмена веществ и дыхании. Кислород входит в состав белков, жиров, углеводов, из которых «построены» организмы; в человеческом организме, например, содержится около 65% кислорода. Большинство организмов получают энергию, необходимую для выполнения их жизненных функций, за счет окисления тех или иных веществ с помощью кислорода. Убыль кислорода в атмосфере в результате процессов дыхания, гниения и горения возмещается кислородом, выделяющимся при фотосинтезе. Вырубка лесов, эрозия почв, различные горные выработки на поверхности уменьшают общую массу фотосинтеза и снижают круговорот на значительных территориях. Наряду с этим, мощным источником кислорода является, по-видимому, фотохимическое разложение водяного пара в верхних слоях атмосферы под влиянием ультрафиолетовых лучей солнца. Таким образом, в природе непрерывно совершается круговорот кислорода, поддерживающий постоянство состава атмосферного воздуха.
Список литературы
1. Добровольский В.В. Основы биогеохимии. Учеб. пособие для геогр., биол., геол., с.-х. спец. вузов. М.: Высш. шк., 1998
2. Каменский А.А., Соколова Н.А., Валовая М.А. Основы биологии. Полный курс общеобразовательной средней школы/ А.А. Каменский, Н.А. Соколова, М.А. Валовая. - М.
3. БСЭ, 1953
4. Стадницкий, Родионов. «Экология»
5. М. Фримантл «Химия в действии»
6. Г. Рудзидис, Ф. Фельдман Химия 7-11.