Файл: Бж орындаан Абилдаев Масат Тобы жфи011. абылдаанатпаева .docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 26.10.2023
Просмотров: 50
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
байланыс ионды болады; поляризационды немесе молекулярлы тор; мұндағы молекулалар арасындағы байланыс Ван-дер-Вальс күштері арқылы болады; валентті байланысты атомдық тор және металды байланысты металл торлары болады. Таза бір күш түрімен байланысқан, яғни өзара әсерлесетін атомдарды сирек кездестіретін секілді, құрылым түрлерінде де таза бір типті тордың кездесуі де өте сирек. Көп жағдайда тор өткінші (переходной) болып келеді, яғни тордың өткінші болуы атомдар арасындағы байланыстың түрі екі немесе бірнеше болудың арқасында химиялық элементтердің кристалдық құрылымын жобамен 4 классқа бөлуге болады (1.1-кесте).
1.1.-кесте
Бұл құрылымдарды талдауды IV класстан бастаған ыңғайлы. Бұл классқа инерт газдардың құрылымы жатады. Инерт газдардың сұйық күйге және кристалға айналғанда электрондары симметриялы сфералық қабыршақтары бар атомдар арасындағы байланыс әлсіз Ван-дер-Вальс күштің пайда болуынан болады. Бұл күштің әсерінен симметриялық атомдар тығыз орналасқан жақ центрленген куб торын құрайды (1.2.-сурет).
Тордағы әрбір атомды оған жақын орналасқан 12 атом қоршайды. Атомға жақын орналасқан атомдардың санын тордың координациялық саны деп атайды.
ІІІ класс. Бұл классқа қысқа периодтан кремний және көміртегі IVB топтан германий және қалайы және VB, VІB және VІІB топтарындағы барлық элементтер жатады. Бұл класстағы барлық элементтер 8-N ережесіне сәйкес кристаллизацияланады, яғни тордағы әрбір атом 8-N жақын атомдармен қоршалған, мұндағы N - сол элемент орналасқан топтың нөмірін білдіреді. Мысалы, алмаз, кремний, германий және сұр қалайы N топтың элементтеріне жатады. Сондықтан олардың торының координациялық саны 8-4=4 болады. Шынында да, бұл элементтердің барлығы тэтраэдралық торға ие, мұнда әрбір атом 4 жақын атомдармен қоршалған (1.8. а-сурет).
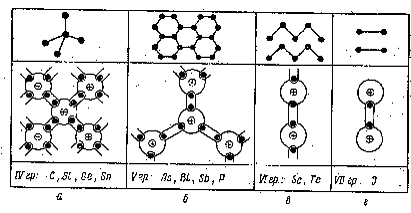
1.8.-сурет
Мышьяк, фосфор, сурьма және висмут периодтық жүйенің V тобында орналасқан, торларының координациялық саны 8-5=3 тең. Бұларда әрбір атом бір жазықта 3 жақын атомдармен қоршалған (1.8. б-сурет).
Торлары жұқа қабыршақтардан тұрады. Атом қабыршақтары бір-бірімен Ван-дер-Вальс күші арқылы байланысқан. Селен және теллур VІ топта орналасқан, торларының координациялық саны 2-ге тең. Олардың атомдары ұзын спираль тізбектерден тұрады. Тізбектегі әрбір атомды жақын екі атом қоршайды (1.8. в-сурет).
Тізбектер өзара Ван-дер-Вальс күштерімен байланысқан. Ал иод VІІ топқа жатады. Иодтың координациялық саны бірге тең. Иодтың торында қос-қос атомдар орналасады (1.8. г-сурет).
Бұл қосақталған атомдар бір-бірімен Ван-дер-Вальс күштерімен байланысқан болады. Сондықтан да иодтың тез буланып ұшып кетуіне алып келеді.
8-N ережесі арқылы химиялық элементтердің кристаллизациялануын оңай түсінуге болады. Мысалы ІV топтағы элемент атомының сыртқы қабыршағында 4 электрон орналасқан. Тұрақты 8 электронды конфигурацияны құрастыру үшін тағы 4 электрон жетіспейді. Бұл кемшілікті толтыру үшін жақын орналасқан 4 атомдардың электрондарымен өзара алмасады (1.8. а-сурет). Сондықтан да кристалл торындағы әрбір атом 4 жақын атомдармен қоршалған. Осы сияқты 8 электронға дейін сыртқы атом қабыршақтары Менделеевтің периодтық кестесіндегі V, VІ, VІІ топтардағы элементтердің атомдары толтырылады.
І класс. Бұл классқа көп элементтер жатады, олар - металдар. Металл торларында атомдар емес, олардың иондары орналасқан. Олар инертті газдар секілді сфералық симметрияға ие. Сондықтан металдар кристаллизация кезінде инертті газдар секілді тығыз орналасқан торға ие деп күтуге болады. Шынында да, металдар 3 түрлі кристалл торларына ие. Координациялық саны 12-ге тең жақ центрленген куб (1.2. в-сурет), координациялық саны 12-ге тең гексагональды тығыз орналасқан тор (1.6.-сурет) және 8 координациялық санға тең көлем центрленген куб (1.2. б-сурет). Бұл ең ұлпа торлы металл (кеңістікті атомдармен толтыру мағынасында). Идеал гексагональды торда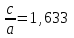 тең.
тең.
ІІ класс. Бұл класстағы химиялық элементтер металл мен ІІІ класстағы 8-N ережемен кристаллизацияланатын элементтер арасындағы аралық кристалдарға жатады. ІІВ топтағы Zn, Cd, Hg металдар, олай болса олар жоғары координациялық санға ие металл торларының біріне жатуы керек. Ал шындығында Zn және Cd кристаллизацияланғанда ерекше гексагональды компакты құрылымға ие болады. с/а=1,633 болмай, бұл қатынас 1,9 тең болады. Бұл кристалдардың координациялық саны 12-ге тең болмай, 6-ға тең, яғни 8-N ережеге сәйкес келеді. Бұл атомдар базис жазықтығында орналасқан болады. Ал сынапқа (Hg) 8-N ереже толығымен орындалады, ол қарапайым ромбоэдрикалық құрылымға ие, мұнда әрбір атом 6 жақын орналасқан атомдармен қоршалған, яғни координациялық сан 6-ға тең. Бор ІІІВ топқа жатады, оның торы деформацияланған, әрбір атомы 5 жақын атомдармен қоршалған тормен сипатталады, яғни тордағы атомдардың орналасуы 8-N ережеге сәйкес келеді.
Ерекше топтарға алюминий, индий, талий және қорғасын элементтердің торларын жатқызуға болады. Олардың барлығы металдың немесе аз шамаға деформацияланған металдың құрылымына ие, бірақ бұл элементтердің атомдары кристалдарда жарым-жартылай ионизацияланған болуы мүмкін. Себебі олардың атом ара қашықтығы ол элементтердің алдындағы элементтер атомдарының ара қашықтығынан үлкен болып келеді. Мысалы, алюминий торының параметрі а=4,04 А болса, оның алдындағы магнийдікі а=3,2 А, индийдікі а=4,87 А болса, оның алдындағы кадмийдікі а=2,97 А, қорғасындікі а=4,94 А болса, оның алдындағы сынаптікі а=3,83 А.
Әр түрлі кристалл құрылымы болуының себебін түсіндіру мақсатында көптеген теориялық зерттеулер болған. Солардың ішінде ең қарапайым таза металдарға кванттық механика арқылы атомдардың әр түрлі орналасуына анықталған атомдар арасындағы әсерлесу энергиясына қарағанда, кристалл құрылымының тұрақтылығына жүйенің (кристалдың) энергиясы минимальды болуы сәйкес келуімен дәлелденген.
Таза металдардың және интерметалды қосындылардың құрылымын түсіндіруде Юм-Розери өзінің ерекше ұсынысын жасаған. Юм-Розеридің гипотезасы электрондық концентрация түсінігіне негізделген. Тордың бір атомына келетін валенттік электрондардың санын электрондық концентрация деп атайды. Металл торының түйінінде орналасқан оң заряды бар иондардың электрон газдармен бірін-бірі тарту күшін тудыратын себебі, электрондық концентрациясы бірдей әр түрлі металдардың және қоспалардың байланыс күштері ұқсас болады және олардың кристалдық құрылымы бір типті болады. Эксперимент нәтижелері бұл Юм-Розери ұсынысының дұрыс екенін дәлелдейді. Менделеевтің периодтық кестесіндегі бір топта орналасқан химиялық элементтердің валенттік электрондары бірдей және олар негізінен бір құрылымға сәйкес кристаллизацияланады (1.1.-кесте). AgZn, Cu3Al, Cu3Sn және басқа көп интерметалды қосындылардың электрондық концентрациясы, жобамен 1,5 тең және олардың кристалдық құрылымы бірдей – көлем центрленген куб. AgCd3, CuZn3 т.б. интерметалды қосындылардың электрондық концентрациясы 1,75 тең, олар гексагоналды тығыз орналасқан құрылымға ие, т.с.с.
Бірақ электрондық концентрация ережесі барлық жағдайда орындала бермейді, кейбір кезде бір топта орналасқан элементтердің кристалдық торы әр түрлі болады. Сонымен қатар электрондық концентрациясы бірдей, бірақ кристалдың құрылымы әр түрлі көптеген қосындыларды көрсетуге болады. Бұл мәліметтерге қарағанда, кристалл құрылымын тек электрондық концентрация анықтай алмайды, сонымен қатар құрылымға тор элементтері арасындағы өріс күші де (оның интенсивтілігі, геометриясы), т.б. факторлар да өзінің әсерін тигізеді.
1.1.-кесте
| | IA | IIA | IIIA | IVA | VA | VIA | VIIA | VIIIA | VIIIB | VIIIC | IB | IIB | IIIB | IVB | VB | VIB | VIIB | 0 | |
| I | | | | | | | | | | | | | | | | | H | He | |
| II | Li | Be | | | | | | | | | | | B | C | N | O | F | Ne | |
| III | Na | Mg | | | | | | | | | | | Al | Si | P | S | Cl | Ar | |
| IV | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |
| V | Rb | Sr | Y | Zr | Nb | Mo | Ma | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | J | Xe | |
| VI | Cs | Ba | P.3. | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | … | Rn | |
| | | | | | | | | | | | | | | | | | | | |
| | І класс | ІІ класс | ІІІ класс | IV класс | |||||||||||||||
Бұл құрылымдарды талдауды IV класстан бастаған ыңғайлы. Бұл классқа инерт газдардың құрылымы жатады. Инерт газдардың сұйық күйге және кристалға айналғанда электрондары симметриялы сфералық қабыршақтары бар атомдар арасындағы байланыс әлсіз Ван-дер-Вальс күштің пайда болуынан болады. Бұл күштің әсерінен симметриялық атомдар тығыз орналасқан жақ центрленген куб торын құрайды (1.2.-сурет).
Тордағы әрбір атомды оған жақын орналасқан 12 атом қоршайды. Атомға жақын орналасқан атомдардың санын тордың координациялық саны деп атайды.
ІІІ класс. Бұл классқа қысқа периодтан кремний және көміртегі IVB топтан германий және қалайы және VB, VІB және VІІB топтарындағы барлық элементтер жатады. Бұл класстағы барлық элементтер 8-N ережесіне сәйкес кристаллизацияланады, яғни тордағы әрбір атом 8-N жақын атомдармен қоршалған, мұндағы N - сол элемент орналасқан топтың нөмірін білдіреді. Мысалы, алмаз, кремний, германий және сұр қалайы N топтың элементтеріне жатады. Сондықтан олардың торының координациялық саны 8-4=4 болады. Шынында да, бұл элементтердің барлығы тэтраэдралық торға ие, мұнда әрбір атом 4 жақын атомдармен қоршалған (1.8. а-сурет).

1.8.-сурет
Мышьяк, фосфор, сурьма және висмут периодтық жүйенің V тобында орналасқан, торларының координациялық саны 8-5=3 тең. Бұларда әрбір атом бір жазықта 3 жақын атомдармен қоршалған (1.8. б-сурет).
Торлары жұқа қабыршақтардан тұрады. Атом қабыршақтары бір-бірімен Ван-дер-Вальс күші арқылы байланысқан. Селен және теллур VІ топта орналасқан, торларының координациялық саны 2-ге тең. Олардың атомдары ұзын спираль тізбектерден тұрады. Тізбектегі әрбір атомды жақын екі атом қоршайды (1.8. в-сурет).
Тізбектер өзара Ван-дер-Вальс күштерімен байланысқан. Ал иод VІІ топқа жатады. Иодтың координациялық саны бірге тең. Иодтың торында қос-қос атомдар орналасады (1.8. г-сурет).
Бұл қосақталған атомдар бір-бірімен Ван-дер-Вальс күштерімен байланысқан болады. Сондықтан да иодтың тез буланып ұшып кетуіне алып келеді.
8-N ережесі арқылы химиялық элементтердің кристаллизациялануын оңай түсінуге болады. Мысалы ІV топтағы элемент атомының сыртқы қабыршағында 4 электрон орналасқан. Тұрақты 8 электронды конфигурацияны құрастыру үшін тағы 4 электрон жетіспейді. Бұл кемшілікті толтыру үшін жақын орналасқан 4 атомдардың электрондарымен өзара алмасады (1.8. а-сурет). Сондықтан да кристалл торындағы әрбір атом 4 жақын атомдармен қоршалған. Осы сияқты 8 электронға дейін сыртқы атом қабыршақтары Менделеевтің периодтық кестесіндегі V, VІ, VІІ топтардағы элементтердің атомдары толтырылады.
І класс. Бұл классқа көп элементтер жатады, олар - металдар. Металл торларында атомдар емес, олардың иондары орналасқан. Олар инертті газдар секілді сфералық симметрияға ие. Сондықтан металдар кристаллизация кезінде инертті газдар секілді тығыз орналасқан торға ие деп күтуге болады. Шынында да, металдар 3 түрлі кристалл торларына ие. Координациялық саны 12-ге тең жақ центрленген куб (1.2. в-сурет), координациялық саны 12-ге тең гексагональды тығыз орналасқан тор (1.6.-сурет) және 8 координациялық санға тең көлем центрленген куб (1.2. б-сурет). Бұл ең ұлпа торлы металл (кеңістікті атомдармен толтыру мағынасында). Идеал гексагональды торда
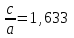 тең.
тең. ІІ класс. Бұл класстағы химиялық элементтер металл мен ІІІ класстағы 8-N ережемен кристаллизацияланатын элементтер арасындағы аралық кристалдарға жатады. ІІВ топтағы Zn, Cd, Hg металдар, олай болса олар жоғары координациялық санға ие металл торларының біріне жатуы керек. Ал шындығында Zn және Cd кристаллизацияланғанда ерекше гексагональды компакты құрылымға ие болады. с/а=1,633 болмай, бұл қатынас 1,9 тең болады. Бұл кристалдардың координациялық саны 12-ге тең болмай, 6-ға тең, яғни 8-N ережеге сәйкес келеді. Бұл атомдар базис жазықтығында орналасқан болады. Ал сынапқа (Hg) 8-N ереже толығымен орындалады, ол қарапайым ромбоэдрикалық құрылымға ие, мұнда әрбір атом 6 жақын орналасқан атомдармен қоршалған, яғни координациялық сан 6-ға тең. Бор ІІІВ топқа жатады, оның торы деформацияланған, әрбір атомы 5 жақын атомдармен қоршалған тормен сипатталады, яғни тордағы атомдардың орналасуы 8-N ережеге сәйкес келеді.
Ерекше топтарға алюминий, индий, талий және қорғасын элементтердің торларын жатқызуға болады. Олардың барлығы металдың немесе аз шамаға деформацияланған металдың құрылымына ие, бірақ бұл элементтердің атомдары кристалдарда жарым-жартылай ионизацияланған болуы мүмкін. Себебі олардың атом ара қашықтығы ол элементтердің алдындағы элементтер атомдарының ара қашықтығынан үлкен болып келеді. Мысалы, алюминий торының параметрі а=4,04 А болса, оның алдындағы магнийдікі а=3,2 А, индийдікі а=4,87 А болса, оның алдындағы кадмийдікі а=2,97 А, қорғасындікі а=4,94 А болса, оның алдындағы сынаптікі а=3,83 А.
Әр түрлі кристалл құрылымы болуының себебін түсіндіру мақсатында көптеген теориялық зерттеулер болған. Солардың ішінде ең қарапайым таза металдарға кванттық механика арқылы атомдардың әр түрлі орналасуына анықталған атомдар арасындағы әсерлесу энергиясына қарағанда, кристалл құрылымының тұрақтылығына жүйенің (кристалдың) энергиясы минимальды болуы сәйкес келуімен дәлелденген.
Таза металдардың және интерметалды қосындылардың құрылымын түсіндіруде Юм-Розери өзінің ерекше ұсынысын жасаған. Юм-Розеридің гипотезасы электрондық концентрация түсінігіне негізделген. Тордың бір атомына келетін валенттік электрондардың санын электрондық концентрация деп атайды. Металл торының түйінінде орналасқан оң заряды бар иондардың электрон газдармен бірін-бірі тарту күшін тудыратын себебі, электрондық концентрациясы бірдей әр түрлі металдардың және қоспалардың байланыс күштері ұқсас болады және олардың кристалдық құрылымы бір типті болады. Эксперимент нәтижелері бұл Юм-Розери ұсынысының дұрыс екенін дәлелдейді. Менделеевтің периодтық кестесіндегі бір топта орналасқан химиялық элементтердің валенттік электрондары бірдей және олар негізінен бір құрылымға сәйкес кристаллизацияланады (1.1.-кесте). AgZn, Cu3Al, Cu3Sn және басқа көп интерметалды қосындылардың электрондық концентрациясы, жобамен 1,5 тең және олардың кристалдық құрылымы бірдей – көлем центрленген куб. AgCd3, CuZn3 т.б. интерметалды қосындылардың электрондық концентрациясы 1,75 тең, олар гексагоналды тығыз орналасқан құрылымға ие, т.с.с.
Бірақ электрондық концентрация ережесі барлық жағдайда орындала бермейді, кейбір кезде бір топта орналасқан элементтердің кристалдық торы әр түрлі болады. Сонымен қатар электрондық концентрациясы бірдей, бірақ кристалдың құрылымы әр түрлі көптеген қосындыларды көрсетуге болады. Бұл мәліметтерге қарағанда, кристалл құрылымын тек электрондық концентрация анықтай алмайды, сонымен қатар құрылымға тор элементтері арасындағы өріс күші де (оның интенсивтілігі, геометриясы), т.б. факторлар да өзінің әсерін тигізеді.