Файл: Реферат Массспектрометрия и спектроскопия методом мрт студента iv курса, 8 группы Педиатрического факультета.docx
Добавлен: 08.11.2023
Просмотров: 56
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Федеральное государственное бюджетное образовательное учреждение высшего образования «Волгоградский государственный медицинский университет» Министерства здравоохранения Российской Федерации
Кафедра внутренних болезней
Реферат
Масс-спектрометрия и спектроскопия методом МРТ
Студента:
IV курса, 8 группы
Педиатрического факультета
Шевченко Д.В.
Проверил(-а):
д.м.н, проф., Деревянченко М.В.
Волгоград, 2023 г.
Содержание
Введение и определения 3
МР-спектроскопия 3
Пики 4
Патологические сдвиги 5
Фосфорная спектроскопия 6
Углеродная спектроскопия 7
Список литературы 9
Введение и определения
Существенное отличие масс-спектрометрии от других аналитических спектральных, например оптических, методов состоит в том, что оптические методы детектируют излучение или поглощение энергии молекулами или атомами, а масс-спектрометрия – непосредственно сами частицы вещества. Прибор, осуществляющий измерение отношения массы фрагмента молекулы к его заряду, называется масс-спектрометр. Попадая в него, анализируемые молекулы, последовательно ионизируются, получившиеся в результате этого ионы разделяются в зависимости от присущих им отношений массы к заряду и детектируются. Масс-спектрометрия – метод исследования и анализа вещества, основанный на ионизации атомов и молекул, входящих в состав пробы, и регистрации спектра масс образовавшихся ионов.
Принцип работы масс-спектрометра можно предмтавить в виде следующей схемы.
-
Превратить нейтральные частицы определяемого вещества – атомы или молекулы в частицы заряженные – ионы. -
Разделить образовавшиеся ионы в пространстве в соответствии с их массой посредством электрического или магнитного поля. -
Измеряя электрический ток, образуемый направленно движущимися ионами, можно судить об изотопном, атомарном и молекулярном составе анализируемого вещества, как на качественном, так и на количественном уровне.
МР-спектроскопия
Магнитно-резонансная спектроскопия (МРС) — метод позволяющий определить биохимические изменения тканей при различных заболеваниях по концентрации определённых метаболитов. МР-спектры отражают относительное содержание биологически активных веществ в определённом участке ткани, что характеризует процессы метаболизма. Нарушения метаболизма возникают, как правило, до клинических проявлений заболевания, поэтому на основе данных МР-спектроскопии можно диагностировать заболевания на более ранних этапах развития.
МРС впервые использовали при исследовании эритроцитов в 1973 году Мун и Ричардс, а в 1974 году при помощи МРС Хаулт исследовал бедренную мышцу мыши.
Основные ядра для in vivo-МР-спектроскопии – это протоны (H), 31-фосфор (31P) и 13-углерод (13С). Из всех магнитных ядер протоны дают наибольший сигнал МР. Атомы водорода входят в состав всех биологических и медицинских препаратов, интермедиатов и продуктов. Поэтому протоны – удачный зонд для мониторинга метаболизма. Однако, протонная спектроскопия связана с большими техническими трудностями. Сигналы воды и липидов чаще всего не очень интересны с медицинской точки зрения. Концентрация протонов воды в тканях составляет 35 M, в то время как концентрация интересующих нас метаболитов находится в диапазоне ниже 10 мМ, т.е. она минимум в 3000 раз ниже. Поэтому маленькие сигналы метаболитов маскируются гигантскими по сравнению с ними сигналами воды и липидов. Только такие технически сложные методы, как селективное возбуждение, селективное насыщение, подавление за счет релаксации и многоквантовая спектроскопия, позволяют подавлять эти сигналы до уровня сигналов метаболитов и обнаружить сигналы таких метаболитов, как лактат (Lac), холин (Ch), креатин (Cr), N-ацетил-аспартат (NAA), фосфохолин (РСНО), д-инозитол и др. 1Н in vivo спектроскопия применяется прежде всего для изучения демилиенизирующих процессов белого вещества мозга и дифференциации.
Пики
-
лактат: резонирует при 1,3 м.д. -
липиды: резонирует при 1,3 м.д. -
аланин: резонирует при 1,48 м.д. -
N-ацетиласпартат (NAA): резонирует при 2,0 -
глутамин / глутамат: резонирует при 2,2-2,4 м.д. -
ГАМК: резонирует при 2,2-2,4 м.д. -
2-гидроксиглютарат: резонирует при 2,25 ppm -
цитрат: резонирует 2,6 м.д. -
креатин: резонирует при 3,0 м.д. -
холин: резонирует при 3,2 м.д. -
мио-инозитол: резонирует при 3,5 м.д. -
вода резонирует при 4,4 м.д.
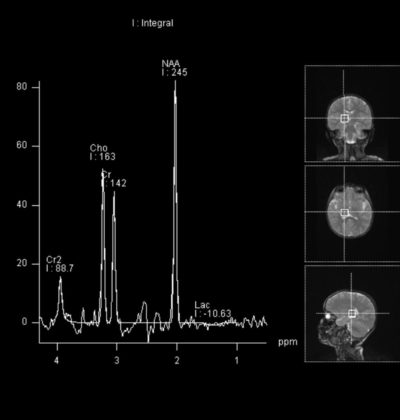
Патологические сдвиги
-
Глиома
По мере повышения уровня NAA и креатина снижаются, а холин, липиды и лактат увеличиваются. В условиях глиомы холин будет повышаться за пределами усиления контраста в соответствии с клеточной инфильтрацией.
-
Не-глиальные опухоли
Незначительные изменения пика NAA.
-
Лейкодистрофии
Прогрессирующая мультифокальная лейкоэнцефалопатия повышение Мио-инозитол. Болезнь Канавана повышение NAA.
-
Митохондриальные заболевания
Синдром Лея: повышение пика холина, снижение NAA и реже повышение пика лактата.
-
Инфекция
Пик NAA отсутствует при всех патологических процессах, разрушающих ткань головного мозга. При абсцессе пик лактата, аланина, ацетата повышен. Пик холина низкий или отсутствует при токсоплазмозе, а при лимфоме повышен, данный показатель используют для отличия одного патологического процесса от другого.
-
Ишемия и инфаркт
Пик лактата будет повышаться, как только клетки головного мозга переходят на анаэробный метаболизм. Пик липидов и всех остальных пиков будет снижаться.
Фосфорная спектроскопия
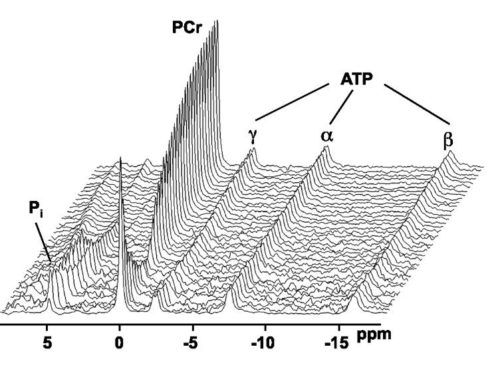
Пока технические проблемы протонной спектроскопии не были успешно преодолены, фосфорная спектроскопия in vivo занимала первое место в медикобиологических исследованиях. Во-первых, 31P, как и !И, имеет 100% изотопную распростренность и, следовательно, большую концентрацию, во вторых, в спектре появляется только ограниченное число известных легко идентифицируемых метаболитов таких, как 3 пика аденозинтрифосфата (АТФ, ATP), пики аденозиндифосфата (АДФ,ADP), фосфокреатина (PCr), неорганического фосфата (pi), фосфоэфиров (PE) и сахарных фосфатов (SP). Из положения линии неорганического фосфата можно однозначно определить внутриклеточное значение pH. Эти фосфорсодержащие метаболиты играют большую роль при энергетическом метаболизме и появляются в значительных количествах не только в мышцах, но, например, в мозге и в печени. Особенно интересно наблюдать за изменением соотношения метаболитов и pH во время нагрузки. 31P- спектроскопию можно также применять для наблюдения за эффективностью терапии рака.
Углеродная спектроскопия
В отличие от ТН и 31Р, магнитный изотоп углерода 13С не является самым распространенным изотопом этого ядра. Его абсолютная чувствительность примерно в 5000 раз ниже, чем для H, однако, современные методы МРС позволяют наблюдать и его сигнал с достаточной чувствительностью. 13С присутствует во всех биологических препаратах, и соответствующие сигналы имеют широкий интервал химических сдвигов, т.е. частоты химически неэквивалентных ядер настолько отличаются друг от друга, что вероятность их наложения невелика. Одним из преимуществ МРС 13С-спектроскопии является возможность проведения исследований с мечеными веществами. Давая животному или пациенту вещества, обогащенные 13С, мы можем следить за большими и четко различимыми сигналами этих меченых веществ и пытаться выяснить, как они метаболируют в организме. Поскольку каждому положению атома углерода в молекуле отвечает вполне характерный сигнал, эксперимент с метками можно использовать не просто для доказательства того, какие молекулы взаимодействуют с меткой, но и для достоверного указания точной внутримолекулярной позиции такого взаимодействия. Такая информация предельно полезна при изучении биохимических путей превращения одних молекул в другие в организме. 13С МР-спектроскопия может также обнаруживать сигналы от сахаров, липидов и гликогена в печени и в мышцах. Можно получить информацию об углеродном балансе энергетического метаболизма, которая дополняет информацию, приносимую об этом метаболизме с помощью МР 31Р-спектроскопии. Многообещающей областью применения UC МР-спектроскопии является анализ таких физиологических жидкостей, как кровь и моча. Эта процедура может осуществляться вполне рутинным образом с помощью аналитических МР- спектрометров с очень сильными магнитными полями.
Список литературы
-
Лебедев А.Т. Масс-спектрометрия в органической химии Издание второе, переработанное и дополненное Москва: ТЕХНОСФЕРА, 2015. – 704 с. -
Физическая энциклопедия / Под ред. А.М. Прохорова. М.: Большая рос. энциклопедия, 1992. Т. 3. – 672 с. -
Токсикологическая химия : учебник / Т. В. Плетенева, А. В. Сыроешкин, Т. В. Максимова ; под ред. Т. В. Плетенёвой. – М. : ГЭОТАР-Медиа, 2013. – 512 с. -
Основы метода масс-спектрометрии. Практическое применение метода : учебное пособие / Е. А. Илларионова, И. П. Сыроватский ; ФГБОУ ВО ИГМУ Минздрава России, Кафедра фармацевтической и токсикологической химии. – Иркутск : ИГМУ, 2021. – 49 с. -
https://www.philips.ru/healthcare/education-resources/research-projects/spectroscopy -
https://radiology24.ru/mrs-2/