Файл: Отчет по лабораторной работе 4 По дисциплине Аналитическая и физическая химия.docx
Добавлен: 08.11.2023
Просмотров: 150
Скачиваний: 6
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
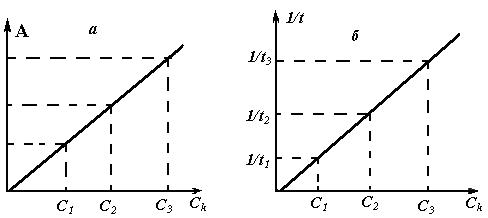
Рис.1. Определение концентрации катализатора по методам фиксированного времени (а) и фиксированной концентрации (б).
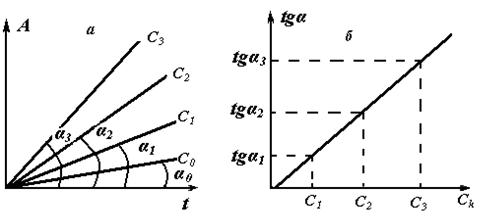
Рис.2. Определение концентрации катализатора по методу тангенсов.
По методу фиксированного времени при фотометрической оценке скорости реакции измеряют оптическую плотность исследуемого и стандартных растворов (с разной концентрацией катализатора индикаторной реакции) через одинаковый промежуток времени с момента начала реакции (рис.1а). Затем графическим способом устанавливают концентрацию катализатора в исследуемом растворе.
Используя метод фиксированной концентрации, определяют время t с момента начала реакции до достижения одним из продуктов или реагентов заданного значения концентрации в растворе. Затем строят зависимость в координатах «1/ t – концентрация вещества» (рис.1б).
В методе тангенсов (рис.2) сначала для заданных величин концентрации катализатора (стандартных растворов) определяют тангенс угла наклона кинетических зависимостей (при фотометрическом контроле скорости индикаторной реакции dA/dt). Затем строят график зависимости отношения dA/dt от концентрации катализатора и графически определяют его содержание в исследуемом растворе.
Применение кинетических методов анализа позволяет снизить значение минимальной определяемой концентрации, однако при этом возрастает погрешность анализа. Другим существенным недостатком кинетического метода является его слабая селективность. Обычно каталитическое действие на индикаторную реакцию может оказывать несколько видов ионов.
Ход работы.
| Объём стандарт. раствора,мл (V) Время,мин (t). | Оптическая плотность A | |||
| 3 | 6 | 9 | Анализ-ый раствор | |
| 2 | 0,163 | 0,267 | 0,271 | 0,263 |
| 3 | 0,192 | 0,297 | 0,302 | 0,281 |
| 4 | 0,215 | 0,323 | 0,327 | 0,300 |
| 5 | 0,234 | 0,344 | 0,345 | 0,332 |
| 6 | 0,251 | 0,362 | 0,369 | 0,363 |
| tg α | 0,0218 | 0,0237 | 0,0221 | 0,0251 |
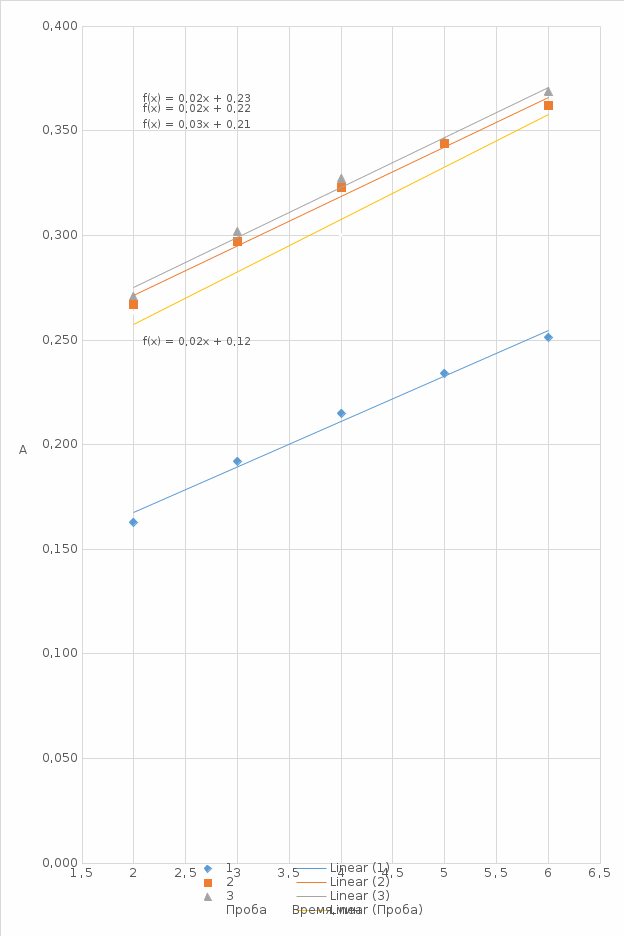
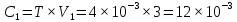 (мг)
(мг)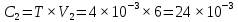 (мг)
(мг)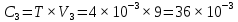 (мг)
(мг)| T*10-3, мг/мл | Cx*10-3, мг |
| 4 | 12 |
| 4 | 24 |
| 4 | 36 |
| | |
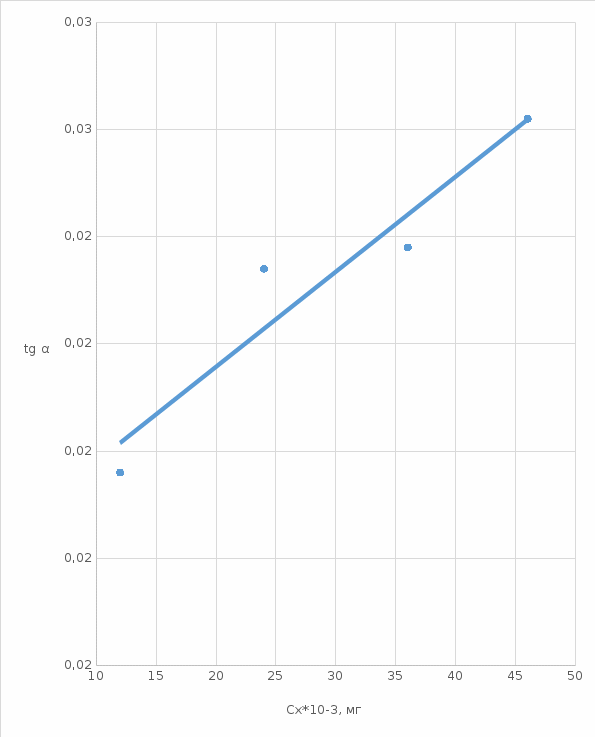
| Сиз графика | tg α |
| 46 | 0,0251 |
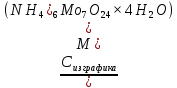
Вывод: в ходе лабораторной работы мы изучили основы кинетического метода анализа, а также оптические методы анализа, определили количество молибдена в пробе.