Добавлен: 09.11.2023
Просмотров: 47
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
МИНИСТЕРСТВО ТРАНСПОРТА РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ АВТОНОМНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ОБРАЗОВАНИЯ
«РОССИЙСКИЙ УНИВЕРСИТЕТ ТРАНСПОРТА»
(РУТ (МИИТ))
Кафедра: «Теплоэнергетика и водоснабжение на транспорте»
КУРСОВАЯ РАБОТА
По дисциплине: «ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА»
Тема: «Термодинамические циклы»
Рецензент Студент
К.т.н., доцент Драбкина Е.В. Соколов А.И.
Шифр: 1910-ц/ЭНб-2409
.
.
(подпись) (подпись)
.
.
(дата) (дата)
Москва 2022
Задача №1.
Для заданного кругового процесса (цикла), совершаемого рабочим телом в соответствии с табл. П1 и П3, определить:
Параметры состояния (P, V, T) в переходных точках;
Изменение внутренней энергии, энтальпии и энтропии в процессах;
Величину работы и теплоты для всех процессов (
Термический и относительный термический КПД;
Построить цикл в PV и TS координатах.
Исходные данные (последняя цифра шифра 9, вариант 1 в табл. П3):
Процессы: 1-2 (dq=0, Р2>Р1), 2-3 (P=const), 3-4 (Т=const), 4-1 (v=const);
Объемный состав газа:
,
Решение.
Средняя молекулярная масса смеси газов равна сумме произведений объемных долей на молекулярные массы отдельных газов, составляющих смесь:
Получим:
Газовую постоянную смеси газов определим по формуле:
Получим:
Далее определим изохорную и изобарную теплоемкость смеси. Для этого определим объемные теплоемкости каждого из компонентов смеси, используя формулу Майера. Имеем:
где
Для
Для
Для
Получим для смеси:
Показатель адиабаты смеси:
Далее определим параметры в основных точках цикла.
1-2: процесс адиабатный,
Точка 1:
По уравнению Менделеева-Клапейрона:
Точка 2:
Из уравнения адиабаты следует, что:
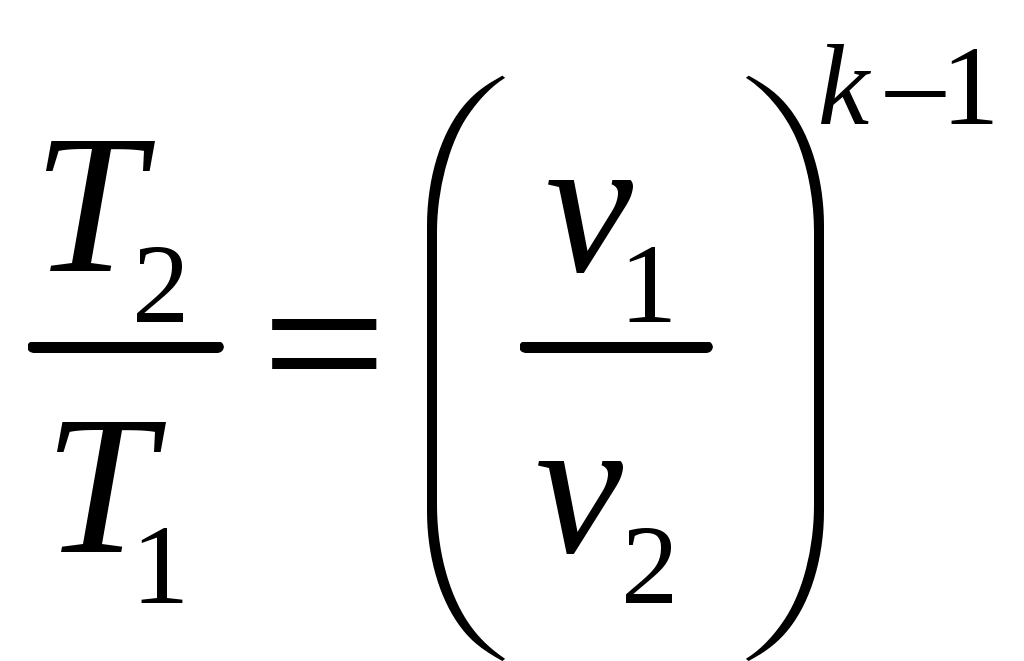 ;
;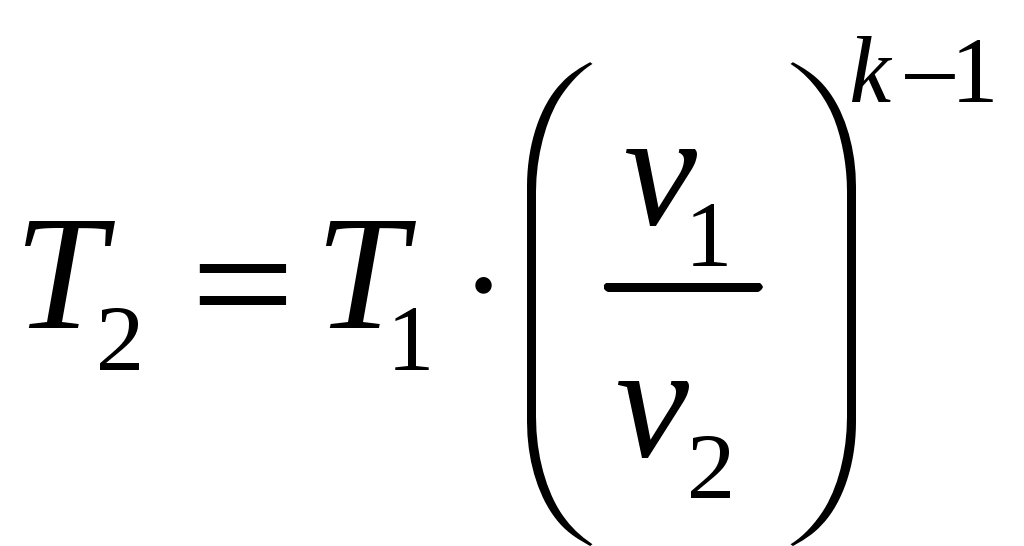 ;
;По уравнению Менделеева-Клапейрона:
Для обратимого адиабатного процесса
В адиабатном процессе работа определяется следующим образом:
-339,7кДж/кг.
По второму закону термодинамики:
Техническая работа:
2-3: процесс изобарный,
Количество теплоты, сообщенное телу в изобарном процессе при постоянной теплоемкости, равно:
Отсюда выразим температуру
К.
По уравнению Менделеева-Клапейрона:
Работа определяется следующим образом:
Для изобарного процесса при постоянной теплоемкости изменение энтропии находится следующим образом:
По второму закону термодинамики:
Техническая работа:
3-4: процесс изотермический,
По уравнению Менделеева-Клапейрона:
Энтальпия и внутренняя энергия смеси газов в изотермическом процессе не меняются, то есть:
В изотермическом процессе количество подведенной к рабочему телу теплоты численно равно работе изменения объема: