ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 09.11.2023
Просмотров: 76
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Работа 9. Исследование уравнения состояния идеального газа
Цель работы: исследовать взаимосвязь объемов, давлений и температур газа в двух его состояниях.
Оборудование: трубка-резервуар с двумя кранами, термометр, калориметр, измерительная лента, стержень штатива с муфтой и лапкой, укладочный короб.
Дополнительное оборудование: барометр-анероид (один на класс).
Исследуемым газом является воздух, находящийся внутри прозрачной эластичной трубки-резервуара с кранами на концах. В работе экспериментально проверяется утверждение о том, что для определенного количества газа в двух его состояниях соотношение между давлением, объемом и температурой остается постоянным и равно pV/T.
Первое состояние воздуха получают путем его нагревания. Кран на одном конце трубки-резервуара закрывают. Трубку закладывают потно, виток к витку внутрь стакана калориметра закрытым краном вниз.
Затем в калориметр наливают теплую воду так, чтобы ее уровень оказался выше открытого крана на несколько миллиметров. Воздух в трубке станет быстро нагреваться, и из открытого крана пойдут пузырьки. Прекращение их образования укажет на то, что температура воздуха и теплой воды сравнялись. Сразу после этого верхний кран закрывают.
Температуру воздуха в нагретом состоянии определяют по температуре воды в калориметре. Объем равен объему внутренней полости трубки, а давление равно атмосферному. (В эксперименте давление водяного столба высотой несколько миллиметров не учитывается).
Затем воздух переводят в другое состояние. Вначале теплую воду в калориметре заменяют таким же количеством воды комнатной температуры. Верхний кран открывают. Объем воздуха в трубке из-за охлаждения уменьшается и внутрь нее будет втягивать вода из стакана.
После того, как воздух охладится до комнатной температуры (обычно это происходит через 2-3 минуты), кран закрывают, а трубку извлекают из калориметра и несколько раз встряхивают, чтобы вода, вошедшая в нее, образовала вблизи крана неразрывный столбик
З
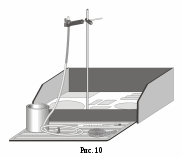 атем конец трубки с водой закрепляют вертикально лапками штатива, но так, чтобы внутренний канал трубки не пережимался (рис. 10).
атем конец трубки с водой закрепляют вертикально лапками штатива, но так, чтобы внутренний канал трубки не пережимался (рис. 10).Верхний кран открывают и наблюдают сжатие воздуха под действием силы давления водяного столба. Во втором состоянии параметры воздуха окажутся следующими. Давление равно сумме атмосферного давления и давления водяного столба, объем уменьшится на объем трубки, занятый водой и вошедшим после сжатия воздухом, температура равна комнатной. Измерив параметры воздуха в двух состояниях, проверяют выполнение равенства:
Объем измеряют в единицах длины воздушного столба.
При подготовке к работе ученикам следует напомнить формулу для расчета давления жидкости и значение плотности воды. Данные измерений и вычислений заносят в таблицу.
| L1, мм | t1, °C | Т1, К | p1, 103 Па | hB, мм | L2, мм | pB, 103 Па | p2, 103 Па | t2, °C | Т2, К | | |
В таблице:
L1и L2 - объем воздуха, соответственно, в нагретом и охлажденном состояниях, выраженный в единицах длины воздушного столба в трубке-резервуаре;
t1 и t2 - значение температуры воздуха в тех же состояниях;
Т1, и Т2 - те же значения температуры, но выраженные в градусах Кельвина;
hB - высота водяного столба в трубке-резервуаре;
р1, - давление воздуха в нагретом состоянии (определяют по показанию барометра-анероида);
рв - давление столба воды на воздух в трубке (рв = ρghB, ρ- плотность воды, g - ускорение свободного падения);
р2 - давление воздуха в трубке после охлаждения (