Файл: Лабораторная работа по учебному курсу Химия (наименование учебного курса).docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 09.11.2023
Просмотров: 867
Скачиваний: 77
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
 МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИфедеральное государственное бюджетное образовательное учреждение высшего образования
«Тольяттинский государственный университет»
Институт машиностроения
| (наименование института полностью) |
| Кафедра "Сварка, обработка материалов давлением и родственные процессы" |
| (Наименование учебного структурного подразделения) |
| 15.03.01 Машиностроение |
| (код и наименование направления подготовки / специальности) |
| Технологии сварочного производства и инженерия поверхностей |
| (направленность (профиль) / специализация) |
Лабораторная работа
по учебному курсу «Химия»
(наименование учебного курса)
Вариант ____ (при наличии)
| Обучающегося | Перлухин А. В. | |
| | (И.О. Фамилия) | |
| Группа | МСбп-2105б | |
| | | |
| Преподаватель | Авдякова О. С. | |
| | (И.О. Фамилия) | |
Тольятти 2023
Бланк выполнения лабораторной работы 1
«Определение эквивалентной и атомной массы»
Цель работы:
Определение эквивалентной и атомной массы металла по объему водорода
, вытесняемого металлом с известной массой при взаимодействии его с раствором кислоты, взятой в избытке.
Общий вид лабораторной установки:
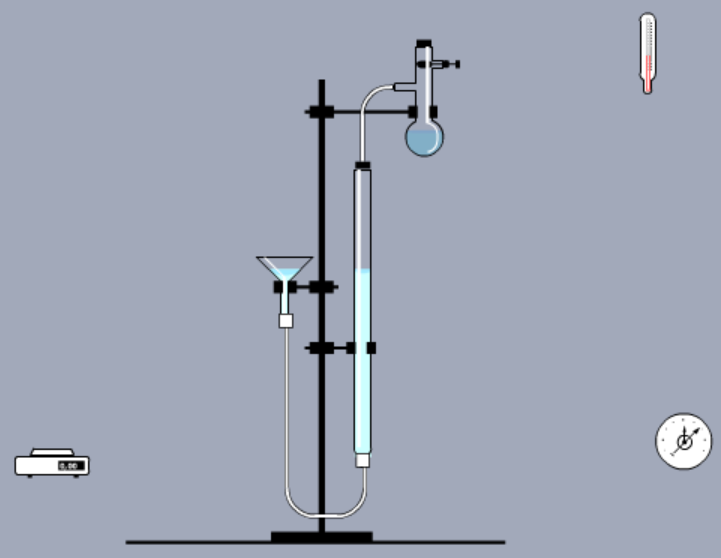
Начальные данные, измерения и расчет:
Масса исследуемого металла
m= 0,023 г.
Удельная теплоёмкость металла
Cуд = 0,39 Дж/(г · К)
Начальный уровень воды
V1 = 2,0 мл
Конечный уровень воды
V2 = 10,25 мл
Объём выделившегося водорода
V(H2) = 8,25·10-6 м3
Температура воздуха в лаборатории
t = 10 °C
Температура воздуха в лаборатории по абсолютной шкале
T = 283,15 K
Атмосферное давление
P = 747 мм рт. ст.
Давление водяного пара
P(H2O) = 9,2 мм рт. ст.
Давление водорода
P(H2) = 747-9,2=737,8 мм рт. ст.
Давление водорода (Па)
P(H2) = 98365,26 Па
Масса водорода
m(H2) = PVM/RT = (98365,26·8,25·10-6·2)/(8,314·283,15)=0,0007 г
Эквивалентная масса исследуемого металла
Mэк(Ме) = Мэк(Ме) = (m(Me)Mэк(H2))/m(H2) = (0,023·1)/0,0007 =
= 32,86 г/моль
Приблизительная атомная масса исследуемого металла
Ar ≈ 25/Суд=25/0,39= 64,10
Приблизительное значение валентности
B ≈ А/Мэк=64,10/32,86=2
Опытное значение атомной массы исследуемого металла
A = В·Мэк=2·32,86=65,72
Исследуемый металл
Исследуемым металлом является: цинк
Точное значение относительной атомной массы металла из периодической системы:
Ar = 65,41
Оценка погрешности определения атомной массы металла
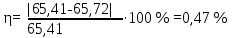
Вывод по работе: в ходе лабораторной работы определили эквивалентную и атомную массу металла по объему водорода, вытесняемого металлом с известной массой при взаимодействии его с раствором кислоты, взятой в избытке. Определяемый метал цинк, эквивалентная масса цинка по результатам опыта 32,86 г/моль, относительная атомная масса по результатам опыта 65,72, погрешность определения атомной массы 0,47 %.
Ответы на контрольные вопросы:
-
Совпадение уровней необходимо, чтобы давление газа в бюретке было равно атмосферному. Тогда, зная температуру, давление и объем газа, можно посчитать количество выделившегося водорода. -
Если уровень воды в уравнивающем сосуде выше уровня воды в бюретке, то давление в бюретке выше атмосферного, если ниже уровня воды в бюретке, то давление в бюретке ниже атмосферного, если на одном уровне с уровнем воды в бюретке - давление в бюретке равно атмосферному. -
Правило Дюлонга-Пти распространяется на металлы и некоторые неметаллы. Допустим, простое вещество - металл.
Ar(Ме) ≈ 25/Суд = 25/0,524 = 47,71
Закон эквивалентов:
m(Me)/m(MexOy) = Мэк(Ме)/Мэк(MexOy), учитывая молярную массу эквивалента кислорода = 16/2 = 8 г/моль
m(Me)/m(MexOy) = Мэк(Ме)/Мэк(Mе)+8
0,27/0,45 = Мэк(Ме)/Мэк(Mе)+8
Мэк(Mе) = 12 г/моль
Валентность:
В(Ме) = 47,71/12 = 4 это титан