Файл: Методические указания для проведения лабораторных занятий.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 23.11.2023
Просмотров: 203
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
3. Харина, Г. В. Химические свойства конструкционных металлов и сплавов [Электронный ресурс] : учебное пособие / Г. В. Харина, С. В. Анахов ; [рец.: Е. В. Русинова, А. С. Борухович] ; Рос. гос. проф.-пед. ун-т. - Электрон. текстовые дан. (1 файл : 28000 Кб). - Екатеринбург: Издательство РГППУ, 2019. - 168 с. : ил., табл. - Библиогр.: с. 167 (15 назв.).
Практическая работа №3 «Электролиз растворов и расплавов солей»
Цель практической работы: научиться составлять схемы электролиза.
Задачи практической работы: ответить на вопросы занятия, выполнить задания.
Оснащение занятия: раздаточный материал, электрохимический ряд напряжений металлов.
Продолжительность: __2_ академических часа.
Вопросы, рассматриваемые на занятии:
1. Что такое электролиз?
2. Какие электроды называют катодом и анодом? Какую роль играет внешний источник тока при электролизе?
3. Чем обусловлено направление движения ионов электролита при электролизе?
4. В чем отличие электролиза водных растворов электролитов от электролиза их расплавов?
5. Каковы отличия электролиза водных растворов солей с использованием активного и инертного анодов?
6. В чем сущность электролитического рафинирования металлов?
7. Что является критерием, определяющим природу частиц, разряжающихся на различных электродах?
8. Какой процесс протекает на катоде? Какова последовательность разрядки ионов и молекул воды на катоде?
9. Какой процесс протекает на аноде? Какова последовательность разрядки ионов и молекул воды на аноде?
10. Сформулируйте законы Фарадея. Приведите математическое выражение.
11. Дайте понятие электрохимического эквивалента вещества. Что такое выход по току?
12. Какой ион будет разряжаться на аноде в первую очередь при электролизе водного раствора, содержащего в одинаковых концентрациях ионы Cl-, I-, NO3-?
13. Определите, в какой последовательности будут выделяться металлы на катоде при электролизе водного раствора, содержащего в своем составе ионы Zn2+, Ni2+, Cu2+?
14. Какие ионы будут разряжаться на катоде при электролизе водного раствора
AgNO3?
15. Какие ионы будут разряжаться на аноде при электролизе водного раствора BaCl2?
Темы сообщений:
1. Получение чистых и сверхчистых металлов.
2. Электролитическое рафинирование меди в промышленности.
Литература:
1. Харина, Г. В. Основные аспекты химии [Электронный ресурс] : учебное пособие / Г. В. Харина, М. В. Слинкина ; [рец.: Е. В. Русинова, Б. Н. Гузанов] ; Рос. гос. проф.-пед. ун-т. - Электрон. текстовые дан. (1 файл : 256323 Кб). - Екатеринбург: Издательство РГППУ, 2017. - 140 с. : ил., табл. - Библиогр.: с. 140 (13 назв.).
2. Гончаров, Е.Г. Краткий курс теоретической неорганической химии [Электронный ресурс] : учеб. пособие / Е.Г. Гончаров, В.Ю. Кондрашин, А.М. Ховив, Ю.П. Афиногенов. — Электрон. дан. — Санкт-Петербург : Лань, 2017. — 464 с. — Режим доступа: https://e.lanbook.com/book/93591. — Загл. с экрана.
3. Харина, Г. В. Химические свойства конструкционных металлов и сплавов [Электронный ресурс] : учебное пособие / Г. В. Харина, С. В. Анахов ; [рец.: Е. В. Русинова, А. С. Борухович] ; Рос. гос. проф.-пед. ун-т. - Электрон. текстовые дан. (1 файл : 28000 Кб). - Екатеринбург: Издательство РГППУ, 2019. - 168 с. : ил., табл. - Библиогр.: с. 167 (15 назв.).
Практическая работа №4 «Защита металлов и сплавов от коррозии»
Цель практической работы: приобретение знаний и умений по рассмотрению механизма коррозии и подбору способов защиты металлов от коррозии.
Задачи практической работы: ответить на вопросы занятия, выполнить задания.
Оснащение занятия: раздаточный материал, электрохимический ряд напряжений металлов.
Продолжительность: __2_ академических часа.
Вопросы, рассматриваемые на занятии:
1. Что такое коррозия? Назовите виды коррозии.
2. Охарактеризуйте особенности химической коррозии.
3. От каких факторов зависит скорость коррозии?
4. В чем сущность электрохимической коррозии? Каков механизм протекания электрохимической коррозии?
5. Что такое деполяризаторы? Что является деполяризатором в кислой среде? В щелочной среде? Назовите виды электрохимической коррозии по механизму ее протекания.
6. Какой металл в коррозионном гальваническом элементе является анодом? Какой процесс протекает на аноде? Какой металл в коррозионном гальваническом элементе является катодом? Какой процесс протекает на катоде?
7. Какой вид коррозии протекает во влажном воздухе? Что является окислителем?
8. При каком соотношении потенциалов
металла и водорода (E0Ме+n/Ме0 и Е02Н+/Н2) возможно протекание электрохимической коррозии с водородной деполяризацией?
9. При каком соотношении потенциалов металла и кислорода (E0Ме+n/Ме0 и Е0О2/2Н2О) возможно протекание электрохимической коррозии с кислородной деполяризацией?
10. Перечислите основные способы защиты металлов от коррозии.
11. Какое покрытие металла называется анодным? Приведите примеры.
12. Какое покрытие металла называется катодным? Приведите примеры.
13. Почему некоторые достаточно активные металлы, например, алюминий, не корродируют на воздухе?
Темы сообщений:
1. Современные способы защиты металлов от коррозии
2. Проблема создания нержавеющих сталей.
Литература:
1. Харина, Г. В. Основные аспекты химии [Электронный ресурс] : учебное пособие / Г. В. Харина, М. В. Слинкина ; [рец.: Е. В. Русинова, Б. Н. Гузанов] ; Рос. гос. проф.-пед. ун-т. - Электрон. текстовые дан. (1 файл : 256323 Кб). - Екатеринбург: Издательство РГППУ, 2017. - 140 с. : ил., табл. - Библиогр.: с. 140 (13 назв.).
2. Гончаров, Е.Г. Краткий курс теоретической неорганической химии [Электронный ресурс] : учеб. пособие / Е.Г. Гончаров, В.Ю. Кондрашин, А.М. Ховив, Ю.П. Афиногенов. — Электрон. дан. — Санкт-Петербург : Лань, 2017. — 464 с. — Режим доступа: https://e.lanbook.com/book/93591. — Загл. с экрана.
3. Харина, Г. В. Химические свойства конструкционных металлов и сплавов [Электронный ресурс] : учебное пособие / Г. В. Харина, С. В. Анахов ; [рец.: Е. В. Русинова, А. С. Борухович] ; Рос. гос. проф.-пед. ун-т. - Электрон. текстовые дан. (1 файл : 28000 Кб). - Екатеринбург: Издательство РГППУ, 2019. - 168 с. : ил., табл. - Библиогр.: с. 167 (15 назв.).
4. . Пустов, Ю.А. Коррозионностойкие и жаростойкие материалы. Методы коррозионных исследований и испытаний. Курс лекций [Электронный ресурс] : учеб. пособие / Ю.А. Пустов, А.Г. Ракоч. — Электрон. дан. — Москва : МИСИС, 2013. — 128 с. — Режим доступа: https://e.lanbook.com/book/47452. — Загл. с экрана.
Практическая работа №5 «Гидролиз солей»
Цель практической работы: приобретение знаний и умений по рассмотрению схем гидролиза растворов солей.
Задачи практической работы: ответить на вопросы занятия, выполнить задания.
Оснащение занятия: раздаточный материал, Периодическая таблица Д.И. Менделеева, таблица растворимости.
Продолжительность: __2_ академических часа.
Вопросы, рассматриваемые на занятии:
1. Введите понятие «электролиты». Приведите примеры сильных и слабых электролитов.
2. Какой процесс называется гидролизом? Какие соли подвергаются гидролизу? Из приведенных ниже солей выберите те, которые подвергаются гидролизу: нитрат натрия, хлорид цинка, нитрат кальция, сульфид калия.
3. Напишите уравнения процесса гидролиза следующих солей: CuSO4, Na2CO3, (NH4)2S. Определите характер среды водных растворов этих солей.
4. Напишите уравнения реакций в молекулярной и ионной формах всех ступеней гидролиза для раствора Na3PO4. Дайте названия всем солям.
5. Почему растворNa2CO3 имеет щелочную среду, а раствор ZnSO4 – кислую? Ответ подтвердите ионно-молекулярными и молекулярными уравнениями.
6. Какие факторы влияют на гидролиз солей? Предложите способы увеличения гидролиза соли карбоната калия, описывающегося следующим уравнением:
K2CO3 +H2O ⇄ KНСОз + KOH, ∆H>0
7. Какие из указанных ниже солей подвергаются гидролизу и какая форма гидролиза (простой, ступенчатый, полный) будет иметь место в каждом отдельном случае: а) NaCN ; б) NaCl ; в) K3PO4 ; г) Al2S3 ;
д) Fe(NO3)3. Ответить на вопрос, не составляя уравнений реакций.
8. Усиление или подавление гидролиза цианида натрия вызовет прибавление к раствору а) кислоты; б) щелочи; в) хлорида аммония.
Литература:
1. Харина, Г. В. Основные аспекты химии [Электронный ресурс] : учебное пособие / Г. В. Харина, М. В. Слинкина ; [рец.: Е. В. Русинова, Б. Н. Гузанов] ; Рос. гос. проф.-пед. ун-т. - Электрон. текстовые дан. (1 файл : 256323 Кб). - Екатеринбург: Издательство РГППУ, 2017. - 140 с. : ил., табл. - Библиогр.: с. 140 (13 назв.).
2. Ахметов Н. С. Общая и неорганическая химия: учебник / Ахметов Н. С. — Санкт-Петербург : Лань, 2018. — 744 с. — Режим доступа: http://e.lanbook.com/book/107904.
3. Гончаров, Е.Г. Краткий курс теоретической неорганической химии [Электронный ресурс] : учеб. пособие / Е.Г. Гончаров, В.Ю. Кондрашин, А.М. Ховив, Ю.П. Афиногенов. — Электрон. дан. — Санкт-Петербург : Лань, 2017. — 464 с. — Режим доступа: https://e.lanbook.com/book/93591. — Загл. с экрана.
Практическая работа №6 «Комплексные соединения»
Цель практической работы: приобретение знаний и умений по составлению формул комплексных соединений и определению их устойчивости.
Задачи практической работы: ответить на вопросы занятия, выполнить задания.
Оснащение занятия: раздаточный материал, Периодическая таблица Д.И. Менделеева, справочник физико-химических величин.
Продолжительность: __2_ академических часа.
Вопросы, рассматриваемые на занятии:
1. Назовите следующие соединения: K2[HgJ4]; [Hg(NH3)6](NO3)2; K6[Pb(S2O3)4]; (NH4)2[Pb(CH3COO)4]. Напишите для этих соединений уравнения электролитической диссоциации по внешней координационной сфере.
2. Для вышеперечисленных комплексных соединений укажите центральный атом, лиганды, внутреннюю координационную сферу и внешнюю координационную сферу.
3. Какие из следующих ионов не могут быть комплексообразователями: Na+, Ba2+, Cr6+, Fe3+, Fe2+, Cu2+, Cu+?
4. Определите, чему равны заряд комплексного иона, координационное число и степень окисления комплексообразователя в соединениях: Na2[Cd(CN)4]; [Cr(H2O)4Cl2]Cl; [Co(H2O)2(NH3)3Cl]Cl.
5. Сравните константы нестойкости двух комплексных ионов [Cu(NH3)4]2+ и [Fe(CN)6]3-. Какой из них более прочный?
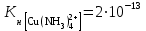 ;
; 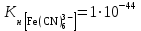
6. Составьте формулы следующих комплексных соединений: хлорида аквапентаамминкобальта (