ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 11
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Дополнительное задание по химии
11 класс
Дисперсной называют систему, в которой одно вещество в виде мелких частиц распределено в объёме другого. Дисперсная фаза – это вещество, которое присутствует в дисперсионной системе в меньшем количестве. Она может состоять и из нескольких веществ. Дисперсионная среда – это вещество, которое присутствует в дисперсионной системе в большем количестве, и в объеме которого распределена дисперсная фаза.
Заполните таблицу агрегатные состояния дисперсионной среды и фазы
| Дисперсионная среда | Дисперсионная фаза | Пример дисперсной системы |
| | | Туман |
| | | Плазма крови |
-
На рисунке изображена модель электронного строения атома некоторого химического элемента.
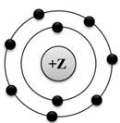
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите количество протонов, которые содержит этот элемент;
3) укажите количество заполненных энергетических уровней;
4) определите максимальную валентность этого элемента
Ответы запишите в таблицу.
| Символ химического элемента | Количество протонов | Количество заполненных энергетических уровней | Максимальная валентность |
| | | | |
-
С увеличением заряда ядра атомов наблюдается постепенное закономерное изменение свойств элементов и их соединений от металлических к типично неметаллическим, что связано с увеличением числа электронов на внешнем энергетическом уровне.
Учитывая эти закономерности, расположите в порядке увеличения неметаллических свойств, следующие элементы: N
a, Cl, Al, Si. Запишите обозначения элементов в нужной последовательности.
Ответ: ____________________________
-
Атом водорода, соединенный с атомом фтора, кислорода или азота (реже - хлора, серы или других неметаллов), может образовывать еще одну дополнительную связь. Водородная связь обусловлена электростатическим притяжением атома водорода (несущим положительный заряд δ+) к атому электроотрицательного элемента, имеющего отрицательный заряд δ−. В большинстве случаев она слабее ковалентной, но существенно сильнее обычного притяжения молекул друг к другу в твердых и жидких веществах.
Из предложенных соединений выберите 2 соединения, между молекулами которых образуются водородные связи: этаналь, этанол, водород, аммиак, кислород.
Запишите ответ в отведенном месте:
-
_________________________ -
_________________________
-
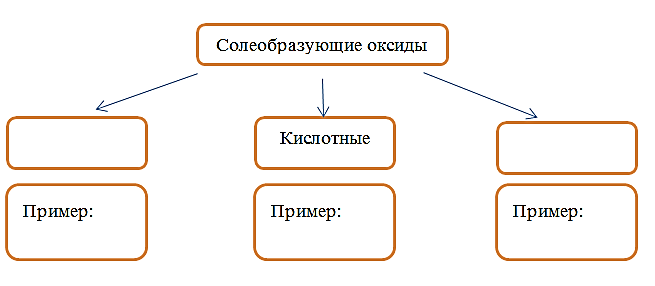
Солеобразующие оксиды классифицируют на три группы, как показано на схеме. В эту схему впишите пропущенные названия групп и приведите по два примера химических формул веществ, принадлежащих данной группе.
Прочитайте следующий текст и выполните задания 6–8.
Сульфат бария часто используется при рентгеновских исследованиях желудочно-кишечного тракта как радиоконтрастное вещество, так как тяжёлые атомы бария хорошо поглощают рентгеновское излучение. Хотя все растворимые соли бария ядовиты, сульфат бария практически нерастворим в воде (и в соляной кислоте, которая содержится в желудочном соке), поэтому он нетоксичен. Для рентгенографического исследования органов пищеварения пациент принимает внутрь суспензию сульфата бария («баритовую кашу») с содержанием бария 58,7 %.
Сульфат бария получают взаимодействием растворимых солей, оксида, пероксида или гидроксида бария с серной кислотой или растворимыми сульфатами. В аналитической химии сульфат бария применяют как хорошую гравиметрическую форму для определения сульфат-ионов и ионов бария в гравиметрическом анализе.
Кроме того, сульфат бария используется как цветовой компонент для пиротехнических средств, так как ионы бария способствуют окрашиванию пламени в зеленый цвет. В настоящее время для этих целей в основном используют нитрат бария, за счет того, что он является сильным окислителем и способствует энергичному горению пиротехнической смеси.
-
1) Составьте молекулярное уравнение реакции получения сульфата бария из пероксида бария, которая упоминалась в тексте.
Ответ: _____________________________________________________
-
Объясните, почему сульфат бария не оказывает токсического влияния на организм.
Ответ: ________________________________________________________________ ___________________________________________________________________________________________
-
1) Составьте молекулярное уравнение реакции между хлоридом бария и сульфатом натрия.
Ответ: _________________________________________________________________
-
Объясните, какие особенности этой реакции позволяют использовать хлорид бария в аналитической химии.
Ответ: ________________________________________________________________
-
1) Составьте сокращенное ионное уравнение реакции между хлоридом бария и сульфатом натрия.
Ответ: _____________________________________________________________
2) Объясните, почему нитрат бария предпочтительней сульфата бария в качестве цветового компонента для пиротехнических средств
______________________________________________________________________________________________________________________________________________________________________________
-
Дана схема окислительно-восстановительной реакции
PH3 + KMnO4 + H2SO4 → MnSO4 + H3PO4 + K2SO4 + H2O
-
Составьте электронный баланс этой реакции
______________________________________________________________________
-
Укажите окислитель и восстановитель
______________________________________________________________________
-
Расставьте коэффициенты в уравнении реакции
______________________________________________________________________
-
Дана схема превращений: Al → Na[Al(OH)4] → AlCl3 → Al(OH)3
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения
-
________________________________________________________________ -
________________________________________________________________ -
_________________________________________________________________
-
Установите соответствие между названием органического вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА КЛАСС/ГРУППА
А) Толуол 1) спирты
Б) Ацетилен 2) алкены
В) Этанол 3) арены
4) алкины
Запишите в таблицу выбранные цифры под соответствующими буквами.
| А | Б | В |
| | | |
Ответ:
-
В предложенные схемы химических реакций вставьте формулы пропущенных веществ и расставьте коэффициенты
-
CaC2 + H2O → …….. + ………………. -
CH3NH2 + ……….. → ……….. + N2 + H2O
-
Глауберова соль Na2SO4*10H2O применяется при лечении желудочно-кишечных заболеваний как слабительное. Сколько (г) Na2SO4.10H2O нужно для приготовления 250 г раствора, с массовой долей Na2SO4, равной 5%. Запишите подробное решение задачи.
Запишите подробное решение задачи.
-
Ацетон является популярным растворителем, применяется как сырье для синтеза многих важных химических продуктов, таких как уксусный ангидрид, метилметакрилат. Ацетон является естественным метаболитом, производимым организмами млекопитающих, в том числе и человеческим организмом. В соответствии с приведенной ниже схемой составьте уравнения реакций получения ацетона. При написании уравнений реакций используйте структурные формулы органических веществ.
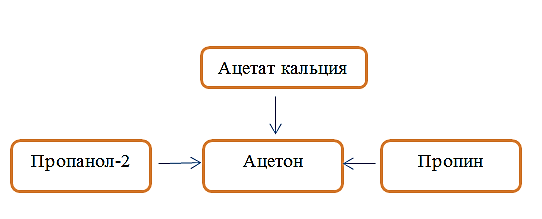
-
_________________________________________________________
-
_________________________________________________________ -
_________________________________________________________