ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 41
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
, а флаваноны – комплексы, окрашенные в коричневый.
В пробирки с водными экстрактами объемом 1 мл добавили кусочек магниевой ленты и 3 капли концентрированной соляной кислоты. Для ускорения реакции смесь нагревали на водяной бане. Флавонолы, флаваноны и флавоны при восстановлении магнием дают красное или оранжевое окрашивание.
2.2.2. Количественный метод определения витамина Р
Оборудование и материалы:
1. Водные экстракты и соки: лимона, яблока, перца, моркови;
2. 0,1 н раствор перманганата калия KМnO4
3. Бюретка для титрования
4. Конические колбы
5. Мерные цилиндры
6. Индигокармин
7. 0.1н раствор щавелевой кислоты
8. Дистиллированная вода.
Ход работы:
Приготовление водного экстракта:
навески продуктов массой (25г) перенесли в конические колбы, залили кипящей водой V 200 мл. Колбы закрыли воздушным холодильником и кипятили в течение 5 мин. Остудили и измерили получившийся объем экстракта.
Приготовление сока:
мелко измельченные продукты отжимали и фильтровали, измерили объем.
25 г. яблока - 15 мл свежевыжатого сока
25 г. перца - 17 мл свежевыжатого сока
25 г. лимона - 20 мл свежевыжатого сока
25 г. моркови - 14 мл свежевыжатого сока
Приготовление 0,1н раствора KМnO4:
KМnO4 массой 1,58 г. растворяли в прокипяченной и остуженной дистиллированной воде в мерной колбе емкостью 500 мл, раствор довели до метки той же водой.
Поправку на титр раствора KМnO4 устанавливали по щавелевой кислоте.
Бюретку для титрования заполняли рабочим раствором KМnO4.
В колбу для титрования вносили 10 мл 1 М раствора серной кислоты, нагревали ее на водяной бане до 70-80.
Добавляли в нее 10 мл стандартного раствора H2C2O4 * 2H2O и титровали горячую смесь раствором KМnO4. Титрование заканчивали при появлении бледно розовой окраски, устойчивой в течении 30 секунд.
Титрование повторяли до получения трех сходящихся результатов. По результатам титрования рассчитывали нормальность раствора KМnO4 и коэффициент поправки по формулам:
С экв(KМnO4) =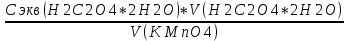 (1)
(1)
К (KМnO4) =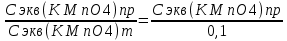 (2)
(2)
Приготовление индикатора (раствор индигокармина):
0,5 г индигокармина растирали в фарфоровой ступке и растворяли в 25 мл концентрированной серной кислоты. Раствор перенесли в мерную колбу емкостью 500 мл и довели водой до метки, затем отфильтровали через бумажный складчатый фильтр.
Титрование экстракта биофлавоноидов.
В колбу наливали 100 мл дистиллированной воды, 5 мл раствора индигокармина и 2 мл экстракта исследуемого продукта (пипеткой). Раствор в колбе, окрашенный в синий цвет, титровали 0,1н раствором марганцовокислого калия до появления желтого окрашивания. Раствор марганцовокислого калия прибавляли небольшими порциями, постоянно перемешивая жидкость в колбе. Одновременно провели контрольное титрование: в колбу налили 100 мл дистиллированной воды, 5 мл раствора индигокармина и титровали 0,1 н раствором перманганата. Опытное и контрольное титрования повторяли 3-4 раза. Суммарное содержание веществ Р-витаминного действия в исследуемых продуктах (в процентах) вычисляли по формуле:
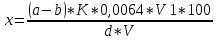 (3)
(3)
где, а — количество 0,1 н раствора KМnO4, израсходованное на титрование опытного раствора, мл;
b — то же для контрольного опыта;
К— поправка на титр 0,1 н раствора марганцовокислого калия;
0,0064 — количество чайного танина, окисляемое 1 мл 0,1 н раствора KМnO4, г;
V1 — объем экстракта исследуемого продукта, мл;
V2 — количество экстракта, взятое для титрования, мл;
d — навеска исследуемого продукта, г [1, с.50].
3. Результаты практического исследования
3.1. Качественное определение витамина Р
В ходе проделанной работы по качественному определению витамина Р мы наблюдали цветные реакции с магнием и соляной кислотой, с хлоридом железа(III). ( Приложение 1)
Результаты окрашивания биофлавоноидов в исследуемых продуктах отражены в таблице 1.
Таблица1. Качественное определение витамина Р
Проведя анализ полученных данных можно предположить, что в плодах перца, лимона, яблока и корнеплодах моркови больше флавонолов (становление зеленой окраски раствора).
Согласно тому, флавоноиды при восстановлении магнием дают красное или оранжевое окрашивание, то проведя анализ растворов с моими продуктами можно предположить их наличие исследуемых овощах и фруктах.
3.2. Количественное определения витамина Р
Установили концентрацию раствора KМnO4, используя формулу 1. Результаты отображены в таблице 2.
Таблица 2. Результаты титрования и нормальность раствора KМnO4.
Используя формулу 2 определили коэффициент поправки К необходимый для вычисления количества биофлавоноидов в продуктах питания.
К (KМnO4) =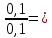 1
1
Результаты титрования биофлавоноидов отображены в таблице 3.
Результаты окрашивания титруемых водных экстрактов и соков. (Приложение 2)
Таблица. 3 Объем KМnO4, мл расходованный на титрование.
Используя формулу 3 рассчитали количество биофлавоноидов в исследуемых продуктах, которые представлены в таблице 4.
Таблица 3. Содержание биофлавоноидов в продуктах растительного происхождения в испытуемой массе и на 100г продукта.
Исходя из результатов в водных экстрактах мы не смогли определить количество биофлавоноидов, так как раствор очень разбавлен и термически обработан поэтому их количество невелико. Проведя анализ качественных реакций мы доказали наличие биофлавоноидов в наших продуктах и в связи с этим мы проверили свежевыжатые и разбавленные соки на содержание витамина Р. Наибольшее содержание биофлавоноидов показали свежевыжатые соки, в разбавленных соках их содержания меньше. В исследуемых продуктах лидером по содержанию биофлавоноидов является перец. Наименьшее количество витамина Р содержится в моркови. Это отображено в приложении 3.
Заключение
По результатам исследований можно сделать следующие выводы:
1) были выявлены методы определения биофлавоноидов: качественный метод определения витамина Р представлен цветными реакциями, количественное определение титрованием;
2) определили качественное и количественное содержание водорастворимого витамина Р в продуктах растительного происхождения: в плодах перца, лимона, яблока и корнеплодах моркови больше флавонолов.
Проведя анализ качественных реакций я доказа наличие биофлавоноидов в исследуемых продуктах. Наибольшее содержание биофлавоноидов показали свежевыжатые соки, в разбавленных соках их содержания меньше.
3) провел сравнительный анализ содержания витамина Р в продуктах растительного происхождения. В исследуемых продуктах лидером по содержанию биофлавоноидов является перец. Наименьшее количество витамина Р содержится в моркови.
Из этого следует, что наибольшим количеством биофлавоноидов обладают свежие продукты, чем водные экстракты этих продуктов. В своей работе я предполагал, что наибольшее количество витамина Р содержится в перце и лимоне. Таким образом, предполагаемая гипотеза подтвердилась: среди исследуемых продуктов наибольшее содержание биофлавоноидов в перце и лимоне.
В дальнейшем я планирую расширить количество исследуемых овощей и фруктов, провести исследование спиртовых экстрактов продуктов и изучить содержание витамина Р, используя хроматографические методы идентификации флавоноидов.
Список используемой литературы
[1] Бобрик Т.В., Тороп Е.И. Витаминология. Практическое пособие по выполнению лабораторных работ[Текст]- Г, 2004, с.59
[2] Важность витамина P. [Электронный ресурс]. - Режим доступа https://flavitax.jimdo.com.
[3] Влияние витамина Р. [Электронный ресурс]. - Режим доступа http://admsysert.ru/info/zashchita-prav-potrebiteley/2517.
[4] Коноплева М.М. Фармакогнозия: природные биологически активные вещества. Учебное пособие [Текст] –В, 2007. - с.273
[5] Определение содержания витамина Р в чае [Электронный ресурс]. - Режим доступа: http://mgk.olimpiada.ru/media/work/26218/витамин_Р.pdf.
[6]Понятие флавоноидов. [Электронный ресурс].- Режим доступа https://works.doklad.ru/view/4VwUIFvheTQ/all.html .
[7] Рутин в продуктах питания. [Электронный ресурс]. - Режим доступа http://caninavit.ru/vidy/rutin-v-produktah-pitaniya-tablitsa.html.
[8] Физико-химические свойства биофлавоноидов. [Электронный ресурс].- Режим доступа https://studopedia.ru/4_146416_fiziko-himicheskie-svoystva.html.
 Приложение 1
Приложение 1

Рис. 1 Водный раствор рутина Рис. 1.1 Качественные реакции


Рис.2 Водный экстракт лимона Рис.2.1 Качественные реакции


В пробирки с водными экстрактами объемом 1 мл добавили кусочек магниевой ленты и 3 капли концентрированной соляной кислоты. Для ускорения реакции смесь нагревали на водяной бане. Флавонолы, флаваноны и флавоны при восстановлении магнием дают красное или оранжевое окрашивание.
2.2.2. Количественный метод определения витамина Р
Оборудование и материалы:
1. Водные экстракты и соки: лимона, яблока, перца, моркови;
2. 0,1 н раствор перманганата калия KМnO4
3. Бюретка для титрования
4. Конические колбы
5. Мерные цилиндры
6. Индигокармин
7. 0.1н раствор щавелевой кислоты
8. Дистиллированная вода.
Ход работы:
Приготовление водного экстракта:
навески продуктов массой (25г) перенесли в конические колбы, залили кипящей водой V 200 мл. Колбы закрыли воздушным холодильником и кипятили в течение 5 мин. Остудили и измерили получившийся объем экстракта.
Приготовление сока:
мелко измельченные продукты отжимали и фильтровали, измерили объем.
25 г. яблока - 15 мл свежевыжатого сока
25 г. перца - 17 мл свежевыжатого сока
25 г. лимона - 20 мл свежевыжатого сока
25 г. моркови - 14 мл свежевыжатого сока
Приготовление 0,1н раствора KМnO4:
KМnO4 массой 1,58 г. растворяли в прокипяченной и остуженной дистиллированной воде в мерной колбе емкостью 500 мл, раствор довели до метки той же водой.
Поправку на титр раствора KМnO4 устанавливали по щавелевой кислоте.
Бюретку для титрования заполняли рабочим раствором KМnO4.
В колбу для титрования вносили 10 мл 1 М раствора серной кислоты, нагревали ее на водяной бане до 70-80.
Добавляли в нее 10 мл стандартного раствора H2C2O4 * 2H2O и титровали горячую смесь раствором KМnO4. Титрование заканчивали при появлении бледно розовой окраски, устойчивой в течении 30 секунд.
Титрование повторяли до получения трех сходящихся результатов. По результатам титрования рассчитывали нормальность раствора KМnO4 и коэффициент поправки по формулам:
С экв(KМnO4) =
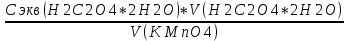 (1)
(1)К (KМnO4) =
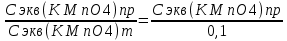 (2)
(2)Приготовление индикатора (раствор индигокармина):
0,5 г индигокармина растирали в фарфоровой ступке и растворяли в 25 мл концентрированной серной кислоты. Раствор перенесли в мерную колбу емкостью 500 мл и довели водой до метки, затем отфильтровали через бумажный складчатый фильтр.
Титрование экстракта биофлавоноидов.
В колбу наливали 100 мл дистиллированной воды, 5 мл раствора индигокармина и 2 мл экстракта исследуемого продукта (пипеткой). Раствор в колбе, окрашенный в синий цвет, титровали 0,1н раствором марганцовокислого калия до появления желтого окрашивания. Раствор марганцовокислого калия прибавляли небольшими порциями, постоянно перемешивая жидкость в колбе. Одновременно провели контрольное титрование: в колбу налили 100 мл дистиллированной воды, 5 мл раствора индигокармина и титровали 0,1 н раствором перманганата. Опытное и контрольное титрования повторяли 3-4 раза. Суммарное содержание веществ Р-витаминного действия в исследуемых продуктах (в процентах) вычисляли по формуле:
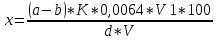 (3)
(3)где, а — количество 0,1 н раствора KМnO4, израсходованное на титрование опытного раствора, мл;
b — то же для контрольного опыта;
К— поправка на титр 0,1 н раствора марганцовокислого калия;
0,0064 — количество чайного танина, окисляемое 1 мл 0,1 н раствора KМnO4, г;
V1 — объем экстракта исследуемого продукта, мл;
V2 — количество экстракта, взятое для титрования, мл;
d — навеска исследуемого продукта, г [1, с.50].
3. Результаты практического исследования
3.1. Качественное определение витамина Р
В ходе проделанной работы по качественному определению витамина Р мы наблюдали цветные реакции с магнием и соляной кислотой, с хлоридом железа(III). ( Приложение 1)
Результаты окрашивания биофлавоноидов в исследуемых продуктах отражены в таблице 1.
| Водный экстракт продукта | Результат реакции с хлоридом железа(III), окрашивание | Результат реакции магнием и соляной кислотой, окрашивание |
| Рутин | зеленый цвет | красный цвет |
| Яблоко | светло-зеленого цвета | красный цвет |
| Лимон | темно-зеленого цвета | красный цвет |
| Перец | зеленый цвет | красный цвет |
| Морковь | зеленый цвет | красно-оранжевый цвет |
Таблица1. Качественное определение витамина Р
Проведя анализ полученных данных можно предположить, что в плодах перца, лимона, яблока и корнеплодах моркови больше флавонолов (становление зеленой окраски раствора).
Согласно тому, флавоноиды при восстановлении магнием дают красное или оранжевое окрашивание, то проведя анализ растворов с моими продуктами можно предположить их наличие исследуемых овощах и фруктах.
3.2. Количественное определения витамина Р
Установили концентрацию раствора KМnO4, используя формулу 1. Результаты отображены в таблице 2.
| V H2C2O4 * 2H2O, мл | V(KМnO4), мл | Vср(KМnO4), мл | Сн (KМnO4),моль-экв/л |
| 10,0 10,0 10,0 | 10,0 9,8 9,7 | 9,8 | 0.1 |
Таблица 2. Результаты титрования и нормальность раствора KМnO4.
Используя формулу 2 определили коэффициент поправки К необходимый для вычисления количества биофлавоноидов в продуктах питания.
К (KМnO4) =
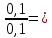 1
1Результаты титрования биофлавоноидов отображены в таблице 3.
Результаты окрашивания титруемых водных экстрактов и соков. (Приложение 2)
| название продуктов | Vср(KМnO4), мл водный экстракт | Vср(KМnO4), мл разбавленный сок | Vср(KМnO4), мл свежевыжатый сок | Vср(KМnO4), мл контрольное титрование |
| перец | 0,4 | 1,2 | 2 | 0,4 |
| лимон | 0,4 | 0,6 | 1 | 0,4 |
| морковь | 0,4 | 0,4 | 0,75 | 0,4 |
| яблоко | 0,4 | 0,5 | 0,8 | 0,4 |
Таблица. 3 Объем KМnO4, мл расходованный на титрование.
Используя формулу 3 рассчитали количество биофлавоноидов в исследуемых продуктах, которые представлены в таблице 4.
| Название продукта | водный экстракт, % | разбавленный сок, % | свежевыжатый сок, % | |||
| в 25г | в 100г | в 25г | в 100г | в 25г | в 100г | |
| перец | 0 | 0 | 1,74 | 6,96 | 3,51 | 13.98 |
| лимон | 0 | 0 | 0,51 | 2,04 | 1,56 | 6,17 |
| яблоко | 0 | 0 | 0,21 | 0,75 | 0,76 | 3,05 |
| морковь | 0 | 0 | 0 | 0 | 0,66 | 2,5 |
Таблица 3. Содержание биофлавоноидов в продуктах растительного происхождения в испытуемой массе и на 100г продукта.
Исходя из результатов в водных экстрактах мы не смогли определить количество биофлавоноидов, так как раствор очень разбавлен и термически обработан поэтому их количество невелико. Проведя анализ качественных реакций мы доказали наличие биофлавоноидов в наших продуктах и в связи с этим мы проверили свежевыжатые и разбавленные соки на содержание витамина Р. Наибольшее содержание биофлавоноидов показали свежевыжатые соки, в разбавленных соках их содержания меньше. В исследуемых продуктах лидером по содержанию биофлавоноидов является перец. Наименьшее количество витамина Р содержится в моркови. Это отображено в приложении 3.
Заключение
По результатам исследований можно сделать следующие выводы:
1) были выявлены методы определения биофлавоноидов: качественный метод определения витамина Р представлен цветными реакциями, количественное определение титрованием;
2) определили качественное и количественное содержание водорастворимого витамина Р в продуктах растительного происхождения: в плодах перца, лимона, яблока и корнеплодах моркови больше флавонолов.
Проведя анализ качественных реакций я доказа наличие биофлавоноидов в исследуемых продуктах. Наибольшее содержание биофлавоноидов показали свежевыжатые соки, в разбавленных соках их содержания меньше.
3) провел сравнительный анализ содержания витамина Р в продуктах растительного происхождения. В исследуемых продуктах лидером по содержанию биофлавоноидов является перец. Наименьшее количество витамина Р содержится в моркови.
Из этого следует, что наибольшим количеством биофлавоноидов обладают свежие продукты, чем водные экстракты этих продуктов. В своей работе я предполагал, что наибольшее количество витамина Р содержится в перце и лимоне. Таким образом, предполагаемая гипотеза подтвердилась: среди исследуемых продуктов наибольшее содержание биофлавоноидов в перце и лимоне.
В дальнейшем я планирую расширить количество исследуемых овощей и фруктов, провести исследование спиртовых экстрактов продуктов и изучить содержание витамина Р, используя хроматографические методы идентификации флавоноидов.
Список используемой литературы
[1] Бобрик Т.В., Тороп Е.И. Витаминология. Практическое пособие по выполнению лабораторных работ[Текст]- Г, 2004, с.59
[2] Важность витамина P. [Электронный ресурс]. - Режим доступа https://flavitax.jimdo.com.
[3] Влияние витамина Р. [Электронный ресурс]. - Режим доступа http://admsysert.ru/info/zashchita-prav-potrebiteley/2517.
[4] Коноплева М.М. Фармакогнозия: природные биологически активные вещества. Учебное пособие [Текст] –В, 2007. - с.273
[5] Определение содержания витамина Р в чае [Электронный ресурс]. - Режим доступа: http://mgk.olimpiada.ru/media/work/26218/витамин_Р.pdf.
[6]Понятие флавоноидов. [Электронный ресурс].- Режим доступа https://works.doklad.ru/view/4VwUIFvheTQ/all.html .
[7] Рутин в продуктах питания. [Электронный ресурс]. - Режим доступа http://caninavit.ru/vidy/rutin-v-produktah-pitaniya-tablitsa.html.
[8] Физико-химические свойства биофлавоноидов. [Электронный ресурс].- Режим доступа https://studopedia.ru/4_146416_fiziko-himicheskie-svoystva.html.
 Приложение 1
Приложение 1
Рис. 1 Водный раствор рутина Рис. 1.1 Качественные реакции


Рис.2 Водный экстракт лимона Рис.2.1 Качественные реакции

