Файл: Распространение и применение элементов 14 (IV) группы и их соединений.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 12
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
| 11.3 B Элементы 14 (IV)-группы | Школа: | ||||||||||||||||||||||
| Дата:01.02 | ФИО учителя: Рахметова Д | ||||||||||||||||||||||
| Класс: 11Б | Количество присутствующих: | отсутствующих: | |||||||||||||||||||||
| Тема урока | Распространение и применение элементов 14 (IV) группы и их соединений | ||||||||||||||||||||||
| Цели обучения, которые достигаются на данном уроке (ссылка на учебную программу) | 11.2.1.1 объяснять закономерности изменения физических и химических свойств элементов 14 (IV) группы | ||||||||||||||||||||||
| Цели урока | Учащиеся могут:
| ||||||||||||||||||||||
| Языковые цели | Учащиеся могут: Устно объяснять химический круговорот веществ в природе, используя ключевые фразы и термины. Лексика и терминология, специфичная для предмета: Круговороты воды, азота, фосфора, кислорода, углерода. Полезные выражения для диалогов и письма: Круговорот воды - это … В результате круговорота воды/углерода … Важность круговорота воды для природы заключается в том, что … По моему мнению, круговорот веществ очень важен для природы, потому что … | ||||||||||||||||||||||
| Ход урока | |||||||||||||||||||||||
| Запланированные этапы урока | Запланированная деятельность на уроке | Ресурсы | |||||||||||||||||||||
| Начало урока 0-5 5-8 | Проверяем знания учеников простыми ответами «да» или «нет» 1. 1s22s22p3 - электронная формула азота. да 2. N, P - элементы главной подгруппы VI группы. нет 3. На последнем энергетическом уровне атома азота находится пять электронов. да 4. Для элементов подгруппы азота характерны высшая степень окисления «+3» и низшая степень «-5». нет 5. Фосфор реагирует в обычных условиях с водородом. нет 6. Соли азотной кислоты называются нитратами. да 7. Азотная кислота реагирует с кислотными оксидами. нет 8. Оксид фосфора (V) - P2O3. нет 9. Водородное соединение с резким специфическим запахом NH3 да 10. Азотистая кислота - слабая одноосновная кислота Да | | |||||||||||||||||||||
| Середина урока 8-10 10-13 13-30 | 4. Пояснение учителя Элементы IV группы – это углерод, кремний, германий, олово и свинец. Более подробно рассмотрим свойства углерода и кремния. В таблице приведены важнейшие характеристики этих элементов. 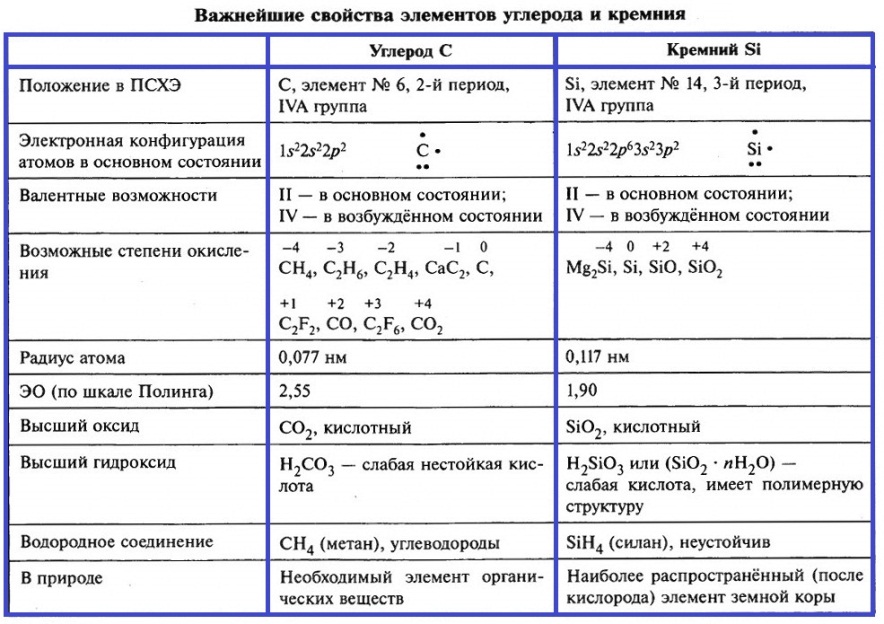 5. Химические свойства 1. Взаимодействие с кислородом: С + О2 изб →СO2 . С + О2 недост →СO Si + О2изб = SiO2, 2Si + O2недост = 2SiO, 2 Взаимодействие с водородом и с серой при нагревании С + 2Н2 = СН4 (метан). С + 2S = СS2 (cероуглерод). 4Si + S8 = 4SiS2 3) Восстановление металлов из их оксидов: С + 2СuO = 2Cu + CO2. При нагревании же с оксидами активных металлов углерод и кремний образуют карбиды СаО + 3С = СаС2 + СО↑, 2Аl2О3 + 9С = Аl4С3 + 6СО↑ или силициды 2МgО + 3Si= Мg2Si + 2SiO. 4) Взаимодействие с металлами: 3С + 4 Al = Al4C3 (карбид алюминия). 5) Оксид углерода (II) горит в кислороде и на воздухе с выделением большого числа теплоты. 2СО + О2 →2СO2 6) Оксид углерода (IV) растворяется в воде СО2 + Н2О →Н2СO3 6) Диоксид углерода – кислотный оксид, поэтому для него характерны реакции с основными оксидами и основаниями СО2 + BaО →BaСO3 СО2 + 2KOH →K2СO3 + Н2О СО2 + KOH →KHСO3 7) Взаимодействие с концентрированными кислотами: С + 2H2SO4 = 2SO2 ↑ + CO2 ↑ + 2H2O. 8) Получение диокисида углерода в промышленности Са СО3 = СаО+ CO2 9) Получение диоксида углерода в лаборатории Na2CO3 + H2SO4→Na2 SO4 + СО2 + Н2О 10) Угольная кислота проявляет свойства кислот Н2СO3+ 2NaOH→ Na2СO3 + 2Н2О Н2СO3+ BaCI2→ Ba2СO3 + 2НCI 7. Закрепление. 2 вариант
| | |||||||||||||||||||||
| Конец урока | 8. Рефлексия Учитель возвращается к целям урока, обсуждая уровень их достижения. | | |||||||||||||||||||||
| Дифференциация – каким образом Вы планируете оказать больше поддержки? Какие задачи Вы планируете поставить перед более способными учащимися? | Оценивание – как Вы планируете проверить уровень усвоения материала учащимися? | Здоровье и соблюдение техники безопасности | |||||||||||||||||||||
| | | | |||||||||||||||||||||