ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 05.12.2023
Просмотров: 581
Скачиваний: 26
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
10-сынып Биология зертханалық жұмыстар.
№1 зертханалық жұмыс «Редуцирленетін және редуцирленбейтін қанттардың тотықсыздандыру қабілетін зерттеу»
Редуцирленетін және редуцирленбейтін қанттардың сандық талдауы пациенттің қанындағы және зәріндегі қанттың деңгейін анықтау үшін медициналық зертханаларда жүргізіледі. Фармецевтикалық компанияларда дәрілік препараттарды өндіру және оларды сертификаттау кезінде; тамақ өнеркәсібінде шикізат пен тамақ өнімдеріндегі қанттың концентрациясын анықтау үшін; шарап жасауда және жеміс-көкөніс дақылдарын дайындау үдерісі кезінде жасалады.
Зертханалық жұмысты жүргізу үшін оны мұқият жоспарлау керек. Бұл зерттеу мақсатын тұжырымдауға, гипотезаны ұсынуға, эксперимент әдістемесін, реактивтер мен жабдықтарды таңдауға, жұмыс барысын құруға, нәтижелерді рәсімдеу тәсілдерін анықтауға мүмкіндік береді.
«Редуцирленетін және редуцирленбейтін қанттардың тотықсыздандыру қабілетін зерттеу» атты зертханалық жұмысын жүргізу үшін кестені қарау керек, ол әдетте экспериментті бастамас бұрын толтырылады.
| Практикалық жұмыс қадамдары | Жоспарланатын іс-әрекет |
| Тақырыптың тұжырымдалуы | Біз нені зерттейміз? | Редуцирленетін және редуцирленбейтін қанттардың тотықсыздандыру қабілеттері |
| Гипотезаның тұжырымдалуы | Біз қандай нәтиже ала аламыз? | Егер көмірсу өзінің тотықсыздандыру қабілетін көрсетсе, онда бұл – редуцирленетін қанттар. |
| Мақсаттың тұжырымдалуы | Зерттеуді не үшін жүргіземіз? | Редуцирленетін және редуцирленбейтін қанттардың тотықсыздандыру қабілетін анықтау |
| Зерттеу әдісін анықтау | Бұны қалай (әдіспен) зерттейміз? | Бенедикт реакциясы |
| Реактивтер мен жабдықтарды анықтау | Экспериментті не арқылы жүргізе аламыз? | 2 мл 10% глюкоза ерітіндісі, 4 мл 10% сахароза ерітіндісі, дистильденген су, 7 мл ерітіндісі, NaOH ерітіндісі, 1 мл сұйылтылған HCl, лакмус қағазы, шымшуыр, су моншасы немесе стақандағы ыстық су, штатив, үш сынауық, сынауықты ұстағыш, 200 мл стақан. |
| Жұмыс кезеңі | Мақсатқа жету үшін қандай қадамдар жасау керек? | 1. Редуцирленетін қанттың тотықсыздандыру қабілетін зерттеу. 2. Редуцирленбейтін қанттың тотықсыздандыру қабілетін зерттеу. |
| Нәтижелерді графикалық ұсыну тәсілдері | Зерттеу нәтижелерін қалай ұсынамын/көрсетемін? | Нәтижелер кестесі, зерттелетін ерітінділердің түс өзгерісінің суреті. |
| Қорытындыларды тұжырымдау | Зерттеу нәтижесімен не істеймін? | Нәтижелер редуцирленетін және редуцирленбейтін қанттардың тотықсыздандыру қабілетін түсіндіруге мүмкіндік береді. |
Редуцирленетін қанттарды зерттеуді глюкоза моносахариді арқылы жүргізуге болады. Сынауыққа 2 мл глюкоза және 2 мл мыс сульфаты бар Бенедикт ерітіндісі қосылады. Осыдан кейін сынауықты су моншасына немесе ыстық суы бар (қайнатылған) шыны стаканға салады. Глюкоза ерітіндісі және Бенедикт ерітіндісі бар сынауықта көк түс біртіндеп жасыл түске, содан кейін сары, қызғылт сары және соңында кірпіш-қызыл түске айналады.
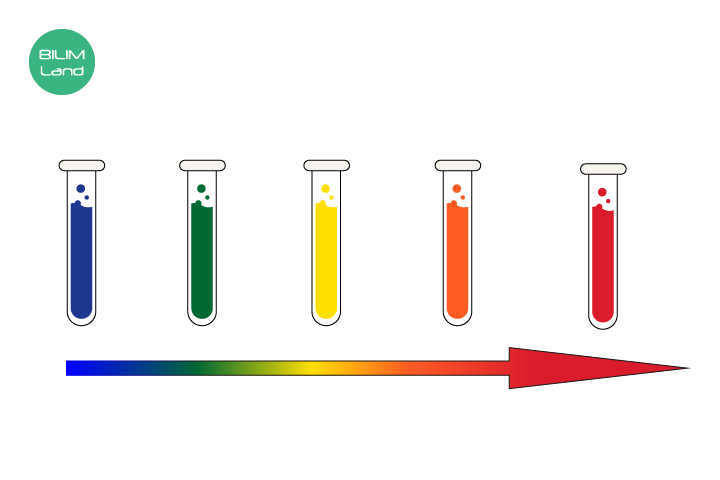
Глюкоза екі валентті мыс сульфатын тұнбаға түсетін кірпіш-қызыл мыс оксидін түзе отырып, бір валенттіге дейін тотықсыздандырды.

Редуцирленбейтін қантты зерттеу үшін сынауыққа 2 мл сахароза және 2 мл Бенедикт ерітіндісі қосылады. Осыдан кейін сынауықты су моншасына немесе ыстық суы бар (қайнатылған) шыны стаканға салады. Бірнеше минуттан кейін түс өзгеруі байқалмайды және ерітінді көк түсте қалады. Сахароза екі валентті мыс сульфатын ерімейтін кірпіш-қызыл мыс оксидін түзе отырып бір валентті мыс сульфатына дейін тотықсыздандырмады, сондықтан көк түс өзгерген жоқ.
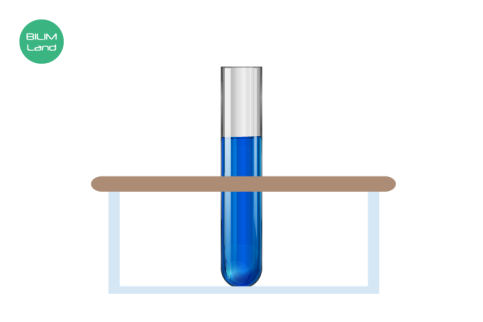
Экспериментті редуцирленбейтін көмірсу сахарозамен жалғастырамыз. Сахароза – редуцирленбейтін екі қанттан, глюкоза мен фруктозадан тұратын дисахарид. Сынауыққа 2 мл сахароза ерітіндісі және 1 мл сұйылтылған тұз қышқылы қосылады. Сынауық қауіпсіздік техникасын сақтай отырып, 1 минут бойы қыздырылады. Қайнату барысында сахароза дисахариді екі моносахаридті қалдықтарына дейін гидролизденеді. Осыдан кейін ерітіндіні бейтараптандыру үшін сынауыққа NaOH тамшылатып қосылады. Лакмус қағазы арқылы ортаның рН бақылауы оны бейтарап күйге жеткенге дейін жүзеге асырылады. Содан кейін сынауыққа 3 мл Бенедикт ерітіндісі қосылады және ол су моншасына түседі. Ерітіндінің түсі кірпіш-қызыл түске ие болады, себебі тотықсыздандыру қабілеттерін глюкоза мен фруктоза көрсетті.
Артқа
№2 зертханалық жұмыс
Нәруыз денатурациясы мен ренатурациясы. «Нәруыздардың құрылымына әртүрлі жағдайлардың әсері (температура, pH)» зертханалық жұмысы
Денатурация – нәруыз молекуласының биологиялық қызметін жоғалта отырып, құрылымын бұзу үдерісі. Түрлі факторлардың әсерінен нәруыздың конформациясы тарқатылады, бірақ молекуладағы аминқышқылдар тізбегінің реттілігі өзгеріссіз қалады.
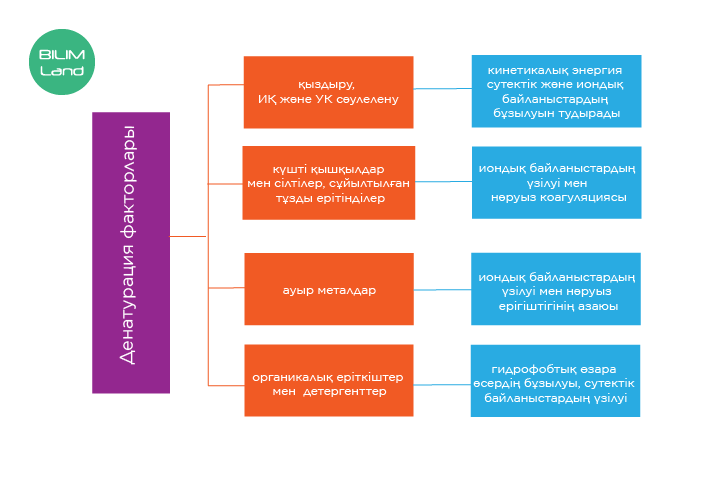
Денатурация нәруыздың төртінші, үшінші және екінші реттік құрылымының шетінен бұзылуына әкелуі мүмкін. Денатурация уақытша немесе тұрақты болуы мүмкін.
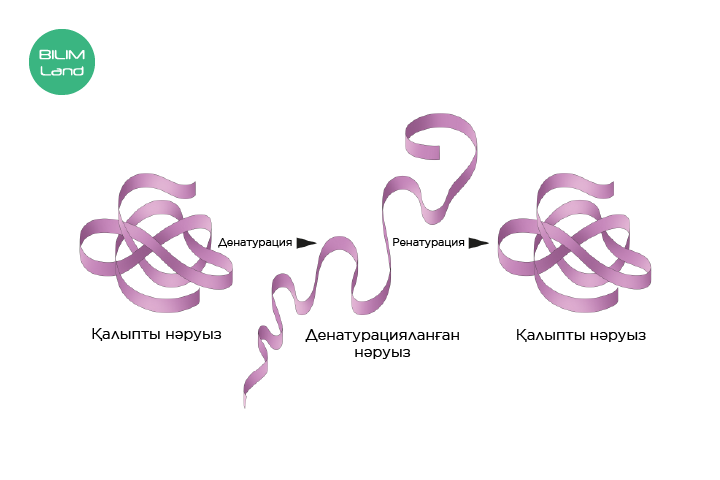
Нәруыз денатурациясының мысалы ретінде жоғары температураның әсерінен жұмыртқа альбумині молекуласының үшінші реттік құрылымын жоғалтуын айтуымызға болады.
Денатурацияның белгісі немесе үшінші реттік құрылымның белгісі оның ерігіштігінің жоғалуы және тұтқырлығының жоғарылауы болады. Нәруыз молекуласының денатурациясы кезінде сутектік және дисульфидтік байланыстар, сондай-ақ гидрофобты өзара әрекеттесу бұзылады.
Денатурацияланған нәруыз тиісті жағдайларда өзінің үшінші реттік құрылымын қалпына келтіре алады, бұл ренатурация деп аталады. Барлық нәруыз молекулалары ренатурациялана алмайды.
№3 зертханалық жұмыс
«Нәруыздардың құрылымына түрлі жағдайлардың (температура, pH) әсері» зертханалық жұмысын жоспарлау үшін әдетте эксперимент басталғанға дейін толтырылатын кестені қарастыру керек.
| Зертханалық жұмыстың қадамдары | Жоспарланатын іс-әрекет |
| Тақырыптың тұжырымдалуы | Біз нені зерттейміз? | Нәруыздардың құрылымына әртүрлі жағдайлардың әсері (температура, pH) |
| Гипотезаның тұжырымдалуы | Біз қандай нәтиже ала аламыз? | Егер нәруыз молекуласына жоғары температурамен әсер етсек және рН деңгейін өзгертсек, онда нәруыз денатурациясы болады. |
| Мақсаттың тұжырымдалуы | Зерттеуді не үшін жүргіземіз? | Нәруыз құрылымына температура және pH әсерін зерттеу |
| Зерттеу әдісін анықтау | Бұны қалай (әдіспен) зерттейміз? | Қыздыру, pH ортасын өзгерту |
| Реактивтер мен жабдықтарды анықтау | Экспериментті қалай жүргізе аламыз? | 8 мл жұмыртқа альбумині, 1 мл HCL, 1 мл NaOH, тамшуыр, pH-метр немесе лакмус қағазы, 4 сынауық, сынауыққа арналған штатив, сынауықты ұстағыш, спиртті жанарғы, сіріңке |
| Жұмыс кезеңдері | Мақсатқа жету үшін қандай қадамдар жасау керек? | 1.Температураның өзгеруі кезінде нәруыз молекуласы құрылымының өзгеруін зерттеу 2. рН көрсеткішінің өзгеруі кезінде нәруыз молекуласы құрылымын зерттеу |
| Нәтижелерді графикалық ұсыну тәсілдері | Зерттеу нәтижелерін қалай ұсынамын/көрсетемін? | Нәтижелер кестесі |
| Қорытындыларды тұжырымдау | Зерттеу нәтижесімен не істеймін? | Нәтижелер температура мен pH нәруыз молекуласының құрылым әсерін түсіндіруге мүмкіндік береді. |
Нәруыз молекуласы құрылымының өзгеруіне температураның әсерін зерттеу үшін сынауыққа 2 мл жұмыртқа нәруызы салынады. Осыдан кейін сынауық ашық жанып жатқан жалынның үстінде қыздырылады. Бірнеше секундтан кейін нәруыз лайлана бастайды, содан кейін мөлдір емес ақ түске айналады.

pH көрсеткішінің өзгеруінен нәруыз молекуласының құрылымының өзгеруін зерттеу үшін үш сынауыққа 2 мл жұмыртқа альбумині құйылады. Эксперимент нәтижелерін бақылауға ыңғайлы болуы үшін сынауықтар арнайы штативке қойылады және санмен немесе әріптермен таңбаланады. Бірінші сынауыққа тамшуыр арқылы 1 мл тұз қышқылы, екіншісіне 1 мл NaOH, ал үшіншісіне 1 мл дистильденген су қосылады. Үшінші сынауық осы экспериментте бақылауға алынған болады. Барлық үш сынауық бөлме температурасында зерттеледі. Түстің өзгеруі, яғни нәруыздың денатурациясы бірінші және екінші сынауықта қышқыл мен сілтінің (негіз) әсерінен пайда болады, үшінші сынауықта өзгерістер болмайды және ерітінді мөлдір күйінде қалады.
Бірінші экспериментте тәуелді айнымалы жұмыртқа альбуминінің түсі болады, тәуелсіз айнымалы температура, ал бақыланатын айнымалы ерітіндінің көлемі болады. Екінші экспериментте тәуелді айнымалы – зерттелетін нәруыздың түсі, ал тәуелсіз айнымалы pH ортасының деңгейі болады. Бақыланатын айнымалы – бөлменің ауа температурасы мен ерітінділердің көлемі.
№4 зертханалық жұмыс
Биологиялық нысандарда нәруыздың болуы. «Биологиялық нысандарда нәруыздың болуын анықтау» зертханалық жұмысы
Жануарлар ағзасында нәруыздың мөлшері өсімдік ағзасына қарағанда жоғары болады. Бұл жануар ағзасының ағзаға тағаммен түсетін амин қышқылдарынан нәруыз молекулаларын синтездей алу мүмкіндігіне байланысты.
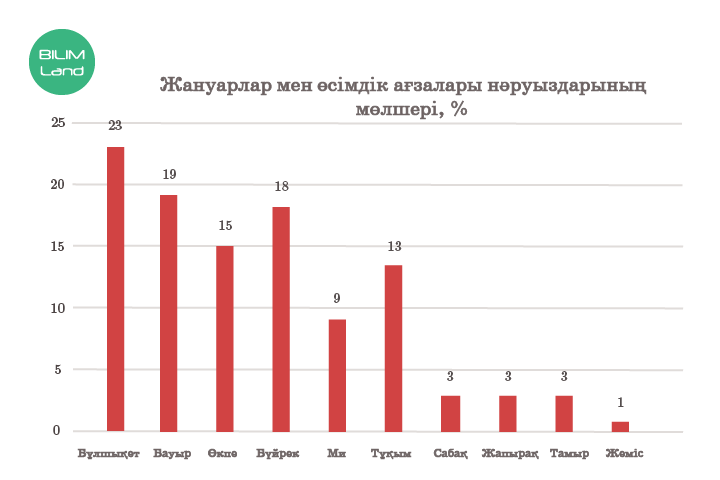
Ағзада нәруыздың болуы адам қызметінің көптеген салалары үшін маңызды рөл атқарады. Пациенттердің қаны мен зәріндегі нәруыздарды клиникалық зертханаларда нақты диагноз қойып, уақтылы емдеу үшін анықтайды. Тамақ өнеркәсібінде, шикізаттағы және азық-түлік өнімдеріндегі нәруызды анықтау, бұл – тауарды сертификаттаудың міндетті шарты. Тоқыма өнеркәсібінде, мысалы, терідегі коллаген нәруызының құрамын ескереді. Бұл олардың сапасы мен бағасына әсер етеді. Химия өнеркәсібіндегі ферменттерді иммобилизациялау жаңа буын жуғыш ұнтақтарын өндіруге мүмкіндік береді. Нәруыз молекулаларын және олардың биологиялық нысандарда болуын зерттеумен алдыңғы қатарлы нанотехнология, биохимия, жасушалық және гендік инженерия, генетика және т.б. зертханалар айналысады.
№5 зертханалық жұмыс
«Биологиялық нысандардағы нәруыздың болуын анықтау» зертханалық жұмысын жоспарлау үшін кестені қарап алған жөн. Ол эксперимент басталмас бұрын толтырылады.
| Зертханалық жұмыстың қадамдары | Жоспарланатын іс-әрекет | Жоспарланатын іс-әрекет |
| Тақырыптың тұжырымдалуы | Біз нені зерттейміз? | Зерттеу нәтижесімен не істеймін? |
| Гипотезаның тұжырымдалуы | Біз қандай нәтиже ала аламыз? | Егер биологиялық нысандарды зерттесе, онда нәруыздың болуын анықтауға болады. |
| Мақсаттың тұжырымдалуы | Зерттеуді не үшін жүргіземіз? | Биологиялық нысандарда нәруыздың болуын анықтау |
| Зерттеу әдісін анықтау | Бұны қалай (әдіспен) зерттейміз? | Биурет реакциясы |
| Реактивтер мен жабдықтарды анықтау | Экспериментті қалай жүргізе аламыз? | 10 мл жұмыртқа альбумині, 10 мг желатин, 2 мл сүт, 2 мл өсімдік майы, 2 мл сахароза, 10 мл 5% калий гидроксиді (КОН), 1 мл NaOH, 2 мл CuSO4, тамшуыр, 5 сынауық, сынауықтарға арналған штатив, 100 мл 2 өлшеуіш стақан. |
| Жұмыс кезеңдері | Мақсатқа жету үшін қандай қадамдар жасау керек? | 1. Нәруыз және желатин ерітінділерін дайындау. 2. Зерттелетін нысандардағы нәруызды анықтау. |
| Нәтижелерді графикалық ұсыну тәсілдері | Зерттеу нәтижелерін қалай ұсынамын/көрсетемін? | Нәтижелер кестесі. |
| Қорытындыларды тұжырымдау | Зерттеу нәтижесімен не істеймін? | Нәтижелер нысандарда нәруыздың болуын анықтауға мүмкіндік береді. |
Биологиялық нысандарда нәруызды анықтау үшін Биурет, Миллон, Паули реакциясы, ксантопротеинді және т.б. бірнеше әдістер бар. Сапалық реакция жүргізу үшін ерітінді түсінің өзгеруі маркер болған кезде Биурет реакциясы жиі қолданылады. Биурет реакциясын жүргізу кезінде қарапайым реактивтер мен зертханалық жабдықтар және аз ғана уақыт қажет.
Нәруызды анықтау үшін бір жұмыртқа ақуызын өлшеуіш стақанға саламыз. Стақанға жұмыртқа ақуызы мен дистильденген су (1:1) бірдей көлемде құйып, жұмыртқа ақуызының алынған ерітіндісін шыны таяқшамен мұқият араластырамыз. 100 мл ыстық суы бар басқа өлшеуіш стаканда негізі коллаген 10 мг тағамдық желатин ериді.