Файл: Комплексов переходных металлов с органическими лигандами и их светоизлучающие свойства мутузова м. Х., Уматгериева х. Л., Хесмикова м.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 11.12.2023
Просмотров: 18
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
УДК 541.49, 546.562, 547.84, 543.429.22, 543.428
ИССЛЕДОВАНИЯ КОМПЛЕКСОВ ПЕРЕХОДНЫХ МЕТАЛЛОВ С ОРГАНИЧЕСКИМИ ЛИГАНДАМИ И ИХ СВЕТОИЗЛУЧАЮЩИЕ СВОЙСТВА
МУТУЗОВА М.Х., УМАТГЕРИЕВА Х.Л., ХЕСМИКОВА М.
Чеченский государственный университет им. А.А.Кадырова, Россия
E-mail: malika557711@gmail.com
Аннотация: Исследованы строения смешаннолигандных координационных соединений с биологически активными лигандами. Изучены ИК -спектры полученных соединений, проведен анализ положения полос поглощения функциональных групп - гидроксильной и карбоксильной групп и соответствующих им ионов, также уделено внимание сравнению спектров гетерометаллических координационных соединений неодима(III) и железа (III).
Ключевые слова: координационные соединения, железо (III) медь (II), ,редкоземельные элементы, люминофоры, эмиттеры, органические светоизлучающие диоды, салициловая, никотиновая, бензойная, яблочная кислоты, асимметричные и симметричные валентные колебания.
STUDY OF THE STRUCTURE AND LIGHT-EMITTING PROPERTIES OF TRANSITION METAL COMPLEXES WITH ORGANIC LIGANDS
MUTUZOVA M.H., UMATGERIEVA H.L., HESMIKOVA M.,
Chechen State University named after A.A. Kadyrov, Russia
Annotation: The structures of mixed ligand coordination compounds with biologically active ligands have been studied. The IR spectra of the obtained compounds were studied, the position of the absorption bands of functional groups - hydroxyl and carboxyl groups and their corresponding ions was analyzed, attention was also paid to comparing the spectra of heterometallic coordination compounds of neodymium(III) and iron (III).
Key words: coordination compounds, iron (III) copper (II), ,rare earth elements, phosphors, emitters, organic light-emitting diodes, salicylic, nicotinic, benzoic, malic acids, asymmetric and symmetric valence vibrations.
Светоизлучающие диоды– это устройства, в которых электрическая энергия преобразуется в световое излучение в результате явления электролюминесценции. Одними из наиболее важных типов органических светоизлучающих диодов являются светодиоды на так называемых малых молекулах – комплексных соединениях, красителях и др. Возрастающее число исследований в этой области за рубежом показывает перспективность использования органических светоизлучающих диодов на основе комплексных соединений лантаноидов. Это связано с тем, что степень преобразования энергии при использовании триплетных эмиттеров может достигать 100%, а помимо дорогостоящих металлорганических соединений (иридия, рутения и других редких металлов платиновой группы) к таким люминофорам относятся и координационные соединения лантаноидов. В отличие от металлов платиновой группы каждый ион лантаноида имеет характерный уникальный спектр испускания, положение пиков в котором при смене лигандов практически не изменяется, изменяется только интенсивность и характер расщепления спектров.
Таким образом, основная задача поиска новых люминесцирующих координационных соединений сводится к подбору лиганда (высокой вероятности образования триплетного уровня, его оптимального расположения по отношению к излучающему уровню лантаноида, хорошей координирующей способности) для каждого иона лантаноида. Одним из важных преимуществом комплексов лантаноидов является малая ширина полос испускания в спектрах люминесценции, в отличие от широких полос в спектрах органических соединений и комплексов d-металлов, что позволяет получать относительно «чистые» цвета и делает перспективным применение органических светоизлучающих диодов на основе комплексов лантаноидов в системах отображении информации.
Получены и исследованы комплексные соединения меди (II), железа (III) и неодима (III) с органическими карбоксилатными лигандами (салициловой, никотиновой, бензойной, фталевой, яблочной кислотами), которые могут проявлять синергизм, так как металлы, используемые в качестве комплексообразователей, являются «металлами жизни». Некоторые процессы, протекающие в биологических системах, включает в себя взаимодействие ионов металла с несколькими лигандами, поэтому особый интерес представляет получение и исследование строения смешаннолигандных комплексных соединений. Следует также отметить усиление синергизма в смешаннолигандных соединениях меди (II) содержащих по два биоактивных лиганда (салициловая, никотиновая, бензойная кислоты) в каждом комплексном соединении. Гетерометаллические комплексные соединения карбоновых кислот с редкоземельными металлами и железом (III) могут применяться в качестве лекарственных препаратов при онкологических заболеваниях, иммунодефиците и заболеваниях крови[1].Также путем пиролиза этих соединений возможно получение смешанных оксидов железа (III) и неодима (III) определенной структуры, которые широко используются в современной технике для записи и хранения информации, в микроволновых устройствах, в качестве датчиков сенсорных устройств, катализаторов различных окислительно-восстановительных реакций[2].
Получены смешаннолигандные и гетерометаллические комплексные соединения: меди (II) с бензойной, никотиновой, салициловой кислотами; железа (III) и неодима (III) с яблочной и фталевой кислотами [3]электрохимическим методом с применением импульсного тока переменной скважности
Методом ИК- спектроскопии определены состав и строение полученных комплексных соединений . По данным ИК- спектроскопии определен способ координации карбоновых кислот.
В ИК - спектрах полученных соединений основное внимание было уделено анализу положения полос поглощения функциональных групп - гидроксильной и карбоксильной групп и соответствующих им ионов. Из литературных источников [4,5] известно, что идентификация карбоновых кислот и их комплексных солей по ИК-спектрам не представляет трудностей; кислоты имеют слабую полосу 2500-2800 см-1 и сильную полосу валентных колебаний С=О 1700 см-1, а спектры комплексных соединений не имеют этих полос, а содержат сильную полосу асимметричных валентных колебаний СОО- 1560-1600 см-
Для определения дентатности и степени ионности-ковалентности связи М-L используется разность Dν(СOO-)=νas(СOO-)-νs(СOO-). Как показали результаты сравнения значений Dν(СOO-) полученных веществ с литературными данными в исследуемых комплексных соединениях карбоксильная группа координирована бидентатно, так как значение Dν(СOO-) для комплексов во всех случаях менее 200 см-1. Тип связывания атомов кислорода карбоксильной группы с ионом металла, является преимущественно ионным, так как Dν(СOO-) для комплексов намного менее 225 см-1.
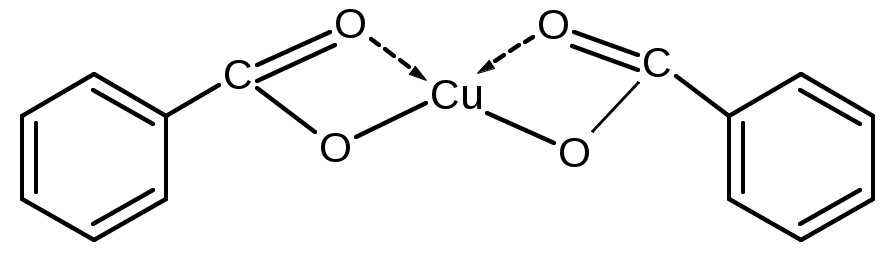
В спектре бензойной кислоты можно отметить интенсивные полосы поглощения в области 2365 и 2336 см-1, которые относятся к поглощению димеров, образованных за счет наличия водородных связей. В области 1686 см-1 проявляется интенсивный пик поглощения с плечом при 1603 см-1, причем данная полоса является уширенной, что может являться следствием наложения двух пиков поглощения принадлежащих карбоксильной группе и бензольному кольцу. В случае спектра поглощения координационного соединения – бензоата меди (II) имеется ряд важных отличий. Полосы поглощения как димерной формы бензойной кислоты, так и полоса поглощения в области 1665 см-1 исчезают, появляются новые полосы в области 1599 см-1 и 1562 см-1. Кроме того, в спектре появляется высокоинтенсивная полоса поглощения при 1408 см-1, которая на основании литературных данных [4] может быть отнесена к симметричным валентным колебаниям ионизированной карбоксильной группы. Разность между максимумами полос поглощения νas-νs составляет в этом случае 154 см-1
. Предполагаемая структура координационного узла без учета молекул растворителя:
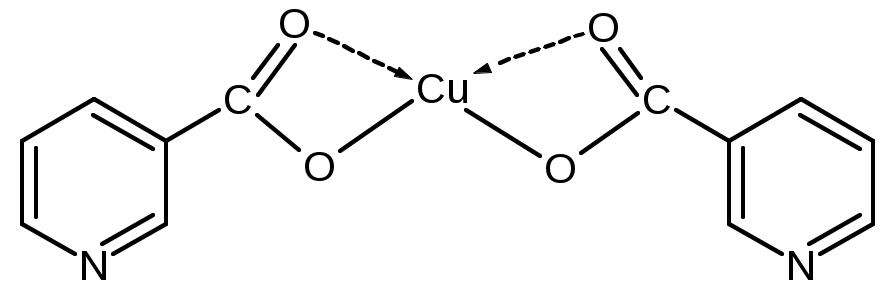
Полосы поглощения пиридинового кольца практически не смещаются, так как интенсивные полосы поглощения при 1483 см-1 и 1596 см-1 отмеченные в спектре никотиновой кислоты могут быть отнесены к колебаниям C-N и С-С практически не смещаются при комплексообразовании и расположены при 1473 см-1 и 1595 см-1, что позволяет сделать вывод об отсутствии координации по азоту пиридинового кольца. Согласно литературным данным [4,5] в этом случае, сдвиг полос поглощения должен достигать значительно больших величин. Предполагаемая структура комплекса меди (II) с никотиновой кислотой без учета молекул растворителя:
У салициловой кислоты существует возможность координации по оксигруппе. Интенсивные поглощения соответствующие деформационным колебаниям оксигруппы в нашем случае при 1483 см-1, отнесение этой полосы сделано на основании спектров записанных в щелочной среде для однозамещенных и двухзамещенных салицилатов.
В спектре салицилата меди (II) эта полоса смещается к 1468 см-1, что позволяет сделать вывод о ее участии в координации.
Таким образом, на основании всего выше изложенного возможно предположить следующее строение координационного узла в синтезированном продукте.
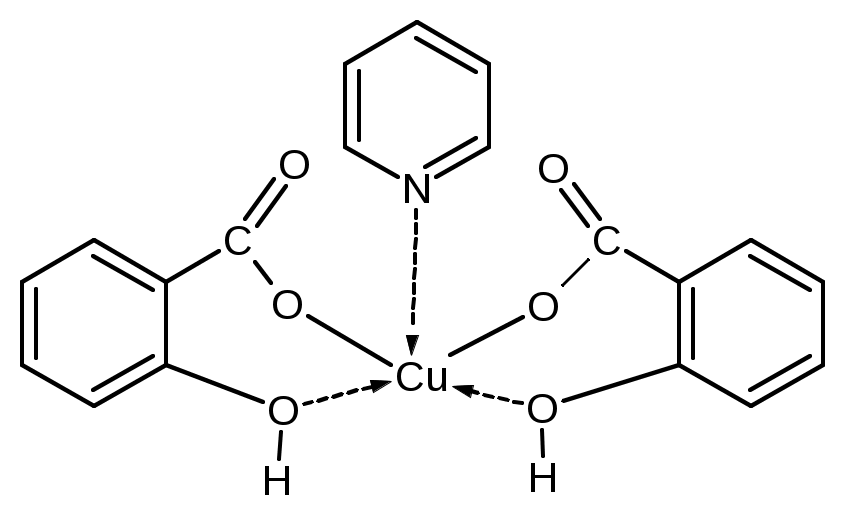
В спектре смешаннолигандного координационного соединения меди встречается ряд полос (1653, 1630, 1599, 1570 см-1), которые могут быть отнесены к поглощениям ионизированных карбоксильных групп, так и к поглощению ароматического и гетероароматического кольца. Полоса при 1599 см-1 относится к поглощению гетерокольца. Другим доказательством подобного отнесения является достаточно малое смещение максимума данной полосы при комплексообразовании. Если в спектре никотиновой кислоты данная полоса проявляется при 1596 см-1, то в спектре координационного соединения с медью при 1595 см-1, а в спектре разнолигандного комплекса наблюдается уширенная полоса при 1599 см-1.
Полоса при 1717 см-1 характерная для никотиновой кислоты и полоса 1686 см-1 характерная для бензойной кислоты, в случае разнолигандного комплексного соединения исчезают, а наиболее интенсивная полоса соответствует 1630 см
-1 с плечом при 1653 см-1, наличие которого может быть вызвано присутствием депротонированных карбоксильных групп бензойной и никотиновой кислот.
В области симметричных колебаний групп полоса никотиновой кислоты при 1417 см-1 и бензойной при 1454 см-1 исчезают, и наблюдается полоса при 1423 см-1. Полосы поглощения бензойной и никотиновой кислоты в заметной степени перекрываются, но даже и при определенных оговорках можно считать, что при Δν=207 см-1 характер связывания – бидентантный.
Практически постоянное значение максимума поглощения при 1596, 1599 и 1595 см-1 для разнонолигандного комплексного соединения, никотината меди (II) и никотиновой кислоты предпологает , что гетероатом азота не принимает участие в координации и в данном случае координация происходит через карбоксильные группы никотиновой и бензойной кислот , обе эти группы связаны бидентантно. Характер такого связывания для полифункциональных органических лигандов подтверждается литературными данными [5].
В случае разнолигандного соединения бензойной и салициловой кислоты можно отметить наличие тех же закономерностей, которые были ранее установлены для комплексообразования никотиновой и бензойной кислот с медью (II), то есть полоса поглощения бензойной кислоты при 1686 см-1 в спектре смешаннолигандного соединения исчезает, также, как и полоса при 1660 см-1 наличие которой отмечено в спектре салициловой кислоты. В спектре смешаннолигандного соединения возникают полосы поглощения при 1628 см-1, в тоже время следует отметить отсутствие полос поглощения в области 1599 см-1, которые характерны для ранее описанного соединения меди с бензойной кислотой. В спектре полученного соединения отсутствуют и полосы поглощения при 1483 см-1 характерные для фенольной группы салициловой кислоты, таким образом, можно предположить, что реализуется структура в которой карбоксилат ион салициловой кислоты является монодентантным, а хелатный цикл замыкается за счет кислорода фенольной группы, в то время как бензойная кислота входит в состав комплексного соединения в виде бидентантного карбоксилат аниона, однако учитывая что полоса поглощения соответствующая валентным ассиметричным колебаниям при 1444 см-1 для салициловой кислоты и 1454 см-1 для бензойной в спектре разнолигандного комплексного соединения проявляются при 1450 см