ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.12.2023
Просмотров: 17
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
 МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИфедеральное государственное бюджетное образовательное учреждение высшего образования
«Тольяттинский государственный университет»
Федеральное государственное бюджетное образовательное учреждение высшего образования «Тольяттинский государственный университет»
| (наименование института полностью) |
| Архитектурно-строительный институт |
| (Наименование учебного структурного подразделения) |
| СТРбп-2003а |
| (код и наименование направления подготовки / специальности) |
| Строительство |
| (направленность (профиль) / специализация) |
ЛАБОРАТОРНАЯ РАБОТА №3
по учебному курсу «Физика1»
(наименование учебного курса)
Вариант 2
| Обучающегося | Ю.С. Трифонов | |
| | (И.О. Фамилия) | |
| Группа | СТРбп-2003а | |
| | | |
| Преподаватель | Н.М. Смоленская | |
| | (И.О. Фамилия) | |
Тольятти 2022
Лабораторная работа № 3 «Теплоемкость идеального газа»
Цель работы:
Знакомство с теплоемкостью идеального газа в изохорическом и изобарическом процессах.
Экспериментальное подтверждение закономерностей изопроцессов.
Экспериментальное определение количества степеней свободы и структуры молекул газа в данной модели.
Исходные данные:
| Первая буква фамилии студента | Номер бригады |
| Б, К, Т, Э | 2 |
Результаты измерений и расчетов:
1. Одноатомный газ: V0=50, p0=160, ν=2,2
Таблица 2
| Т, К | 300* | 400 | 500 | 600 | 700 | 800 |
| QV,кДж | 2,74 | 5,48 | 8,23 | 10,97 | 13,71 | 16,45 |
| Qр,кДж | 4,57 | 9,14 | 13,48 | 18,28 | 22,85 | 27,42 |
*Значения абсолютной температуры может не совпадать с рекомендуемым, но должно быть близким по значению и одинаковым для Qp и QV в столбце.
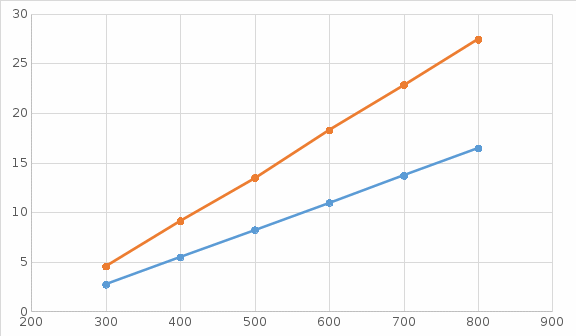
Графики зависимостей QV=f(T) и Qp=f(T) для одноатомного газа (на одном чертеже) по табл.2.
(Все графики могут быть выполнены с использованием спецсредств MSOffice или др. приложений Определение Cp теплоемкости и cp молярной теплоемкости газа при постоянном давлении:
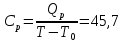
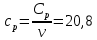
Определение CV теплоемкости и cV молярной теплоемкости газа при постоянном объеме:
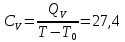
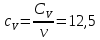
Определение γ постоянной адиабаты:
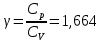
Определение iчисла степеней свободы молекул газов:
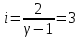
2. Двухатомный газ: V0=50, p0=160, ν=2,2
Таблица 3
| Т, К | 300 | 400 | 500 | 600 | 700 | 800 |
| QV,кДж | 4,57 | 9,14 | 13,71 | 18,28 | 22,85 | 27,42 |
| Qр,кДж | 6,4 | 12,8 | 19,2 | 25,59 | 31,99 | 38,39 |
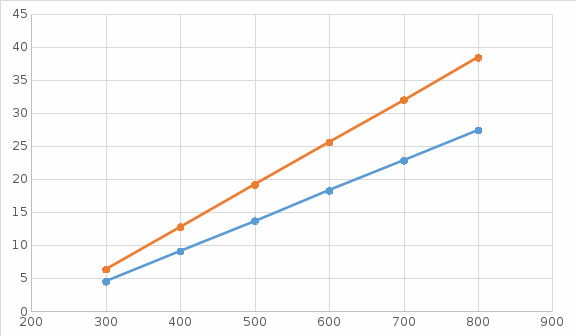
Графики зависимостей QV=f(T) и Qp=f(T) для двухатомного газа (на одном чертеже) по табл.3:
Определение Cp теплоемкости и cp молярной теплоемкости двухатомного газа при постоянном давлении:
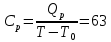 ,98
,98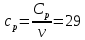
Определение CV теплоемкости и cV молярной теплоемкости двухатомного газа при постоянном объеме:
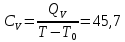
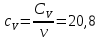
Определение γ постоянной адиабаты:
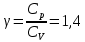
Определение iчисла степеней свободы молекул газов:
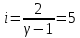
3. Трехатомный газ: V0=50, p0=160, ν=2,2
Таблица 4
| Т, К | 300 | 400 | 500 | 600 | 700 | 800 |
| QV,кДж | 5,48 | 10,97 | 16,45 | 21,94 | 27,42 | 32,91 |
| Qр,кДж | 7,31 | 14,63 | 21,94 | 29,25 | 36,56 | 43,88 |
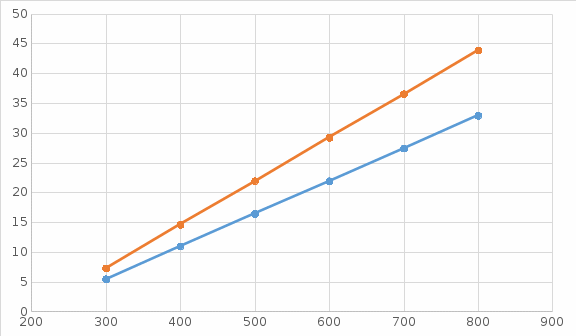
Графики зависимостей QV=f(T) и Qp=f(T) для трехатомного газа (на одном чертеже) по табл.4:
Определение Cp теплоемкости и cp молярной теплоемкости трехатомного газа при постоянном давлении:
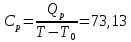
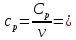 33,24
33,24Определение CV теплоемкости и cV молярной теплоемкости трехатомного газа при постоянном объеме:
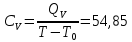
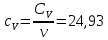
Определение γ постоянной адиабаты:
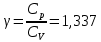
Определение iчисла степеней свободы молекул газов:
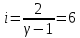
Вывод:
При экспериментальном исследовании определено следующее : - теплоёмкость газа при постоянном давлении Cp всегда закономерно выше значения теплоёмкости Cv при постоянном объёме - все полученные графики для изобарного изохорного процессов имеют линейность в представленном диапазоне температур для газов различной атомности - Количество атомов в молекуле газа подтверждено экспериментально с помощью нахождения i числа степеней свободы молекул газов .Для одноатомных молекул i= 3, двухатомных и трехатомных соответственно i= 5 и i= 6.