Файл: Ароматические углеводороды. Гомологичный ряд. Изомерия. Номенклатура.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.12.2023
Просмотров: 14
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Дата: «___» «__________» 202_ г.
Класс:
Тема урока: Ароматические углеводороды. Гомологичный ряд. Изомерия. Номенклатура.
| № | Части урока | Время |
| 1 | Организационный момент: Приветствие, рапорт дежурного. | 3-минут |
| 2 | Проверка домашнего задания. Ответы на вопросы. | 10-минут |
| 3 | Новая тема: Словарная работа. Объяснение учителя. | 14-минут |
| 4 | Закрепление: | 15-минут |
| 5 | Подведение итога урока: Оценивание. | 2 -минут |
| 6 | ЗНД | 1-минут |
Тип урока: изучение нового материала
Цель урока: сформировать понятие об ароматических углеводородах.
Задачи: образовательные: способствовать формированию у учащихся понятий об ароматических углеводородах, о гомологическом ряде, изомерии и номенклатуре аренов; развивающие: продолжить развивать понятие о строении вещества, об изомерии и ее видах; продолжить развивать умения давать названия органическим соединениям по номенклатуре ИЮПАК и строить формулы веществ по названию; развивать умения сравнивать, обобщать, делать выводы; воспитательные: продолжить воспитание познавательного интереса к науке, формировать коммуникативные качества учащихся через организацию групповой работы на уроке;
Методы: объяснительно-иллюстративный; наглядные (демонстрация шаростержневых моделей молекул), интерактивные.
Оборудование: доска, мел, учебник по химии 10 класс, компьютер, проектор карточки для раздачи, презентация к уроку.
Формы организации познавательной деятельности:
- индивидуальная
- групповая
-
Организационный момент:
1.Приветствие. Рапорт дежурного.
2.Привлечь внимание учащихся к уроку.
3. Объявление темы и цели урока.
-
Повторение пройденной темы. Метод «Дождливые вопросы» -
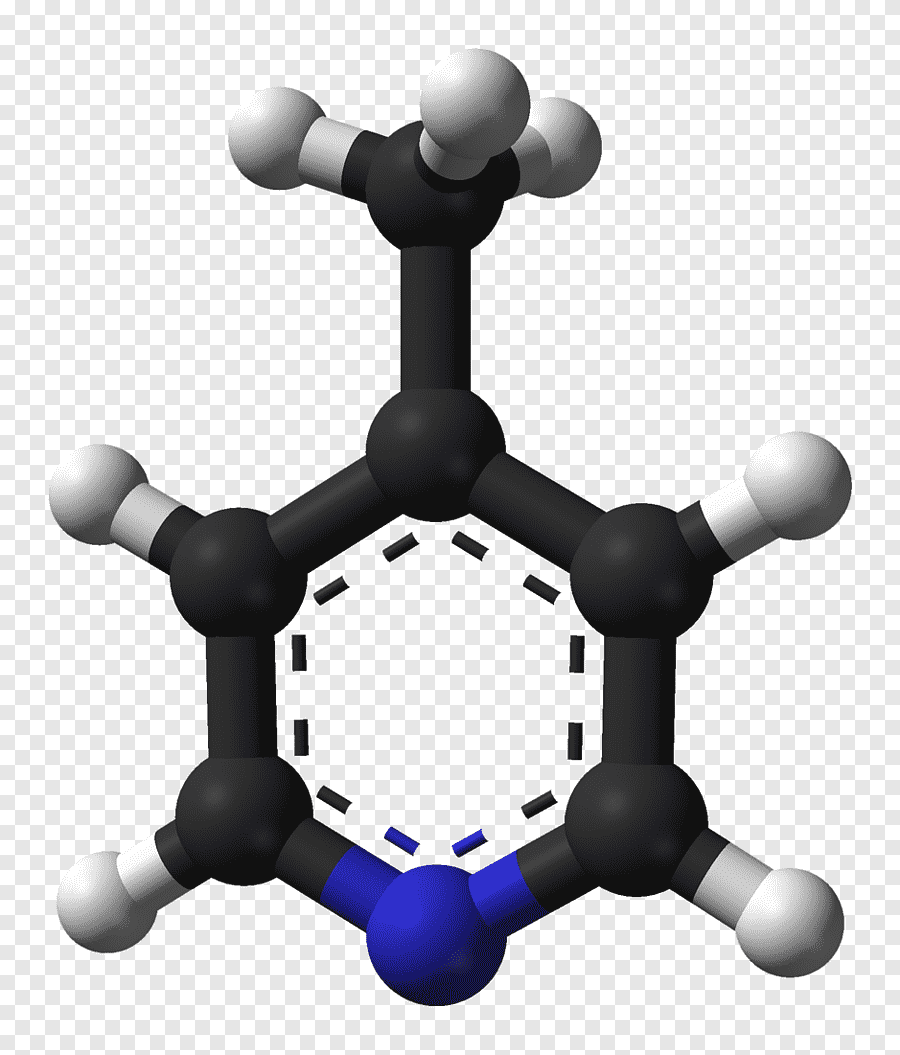
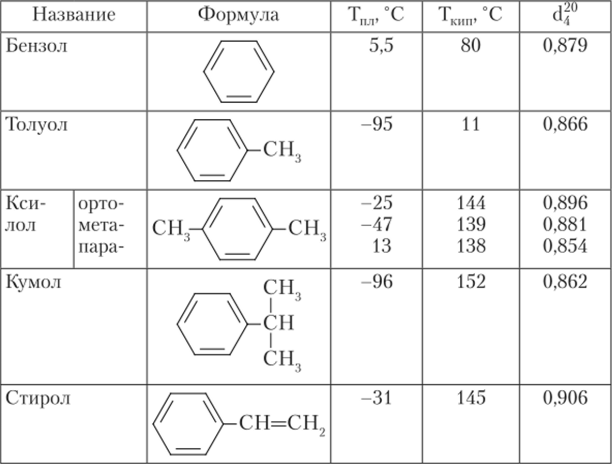
Новая тема: Ароматические углеводороды – это соединения, в молекуле которых имеется специфическая связанная циклическая группа атомов – бензольное ядро. Бензол был выделен М. Фарадеем в 1825 году из световой жидкости, использовавшейся в то время для уличного освещения. Первая структурная формула бензола – C6 H6 была предложена в 1865 году. А. Кекуле предположил, что молекула бензола опирается на правильное шестиугольное основание, образованное шестью атомами углерода, соединенными между собой чередующимися одинарными и двойными связями. Согласно этой структуре бензол должен обесцвечивать водный раствор перманганата калия и брома, но этого не происходит. Противоречие можно объяснить наличием особого типа связи в молекуле бензола — ароматического кольца. Шесть атомов углерода образуют плоское шестичленное кольцо в состоянии sp2 -гибридизации, в котором каждый атом углерода образует три первичные σ-связи: две связи с соседними атомами углерода и одну связь с атомом водорода. Валентные углы между этими тремя σ-связями равны между собой. Каждый атом углерода имеет еще один негибридизованный p-электрон. Эти шесть электронов параллельны друг другу, перпендикулярны плоскому σ-скелету. При их взаимодействии образуется единое π-электронное облако, которое изображается в виде окружности внутри шестичленного кольца. Наибольшая плотность p-электронов в этой сопряженной системе выше и ниже плоскости σ-скелета.(презентация)
-
Закрепление: учащиеся делятся на 3 группы.
1-задание: Игра «Викторина».
2-задание: Интерактивное задание «Погоня в лабиринте»
-
Подведение итога урока: Оценивание. -
Домашнее задание: Нарисуйте структурные изомеры гомолога бензола с 10 атомами углерода.
Заместитель директора по учебно-воспитательной работе: _________ Куттумуратова В.

АЛХИМИКИ

АТОМЫ

ХИМИЛЯНДИЯ