Файл: Контрольная работа По дисциплине химия Вариант 8 фио студента Кондратьев. С. А группа 1123з Оценка 20 г.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.12.2023
Просмотров: 18
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
ГБПОУ «Курганский промышленный техникум»
Контрольная работа
По дисциплине «химия»
Вариант 8
ФИО студента Кондратьев.С.А
Группа 112/3з
Оценка_______«___»______20__г.
Преподаватель. Михайлова.И.А
1 вопрос
Физические свойства сложных эфиров:
Летучие, бесцветные жидкости
Плохо растворимы в воде
Чаще с приятным запахом
Легче воды
Название сложных эфиров:
Краткие названия сложных эфиров строятся по названию радикала (R') в остатке спирта и названию группы RCOO- в остатке кислоты.
Например, этиловый эфир уксусной кислоты CH3COOC2H5 называется этилацетат.
2.Классификация жиров:
1) твердые – это жиры, в состав которых входят предельные карбоновые кислоты. Это жиры животного происхождения (говяжий, свиной, бараний и т.д.), исключение составляет рыбий жир;
2) жидкие – это жиры, в состав которых входят непредельные карбоновые кислоты. Это жиры растительного происхождения, или масла (подсолнечное масло, соевое масло, рапсовое масло и т.д.), исключение составляет пальмовое масло.
А). Жиры нерастворимы в воде, но хорошо растворимы в органических растворителях – бензоле, гексане;
Б). Гидрированием жидких жиров получают твердые сложные эфиры. Именно эта реакция лежит в основе получения из растительного масла твердого жира – маргарин.
Мыла – натриевые или калиевые соли высших карбоновых кислот. Натриевые соли высших карбоновых кислот имеют твердое агрегатное состояние, а калиевые – жидкое (жидкое мыло).
При изготовлении мыла в него добавляют душистые вещества, глицерин, красители, антисептики, растительные экстракты.
Исходным сырьем для получения мыла служат растительные масла (подсолнечное, хлопковое и др.), животные жиры, а также гидроксид натрия или кальцинированная сода. Растительные масла предварительно подвергаются гидрогенизации, т. е. их превращают в твердые жиры. Применяются также заменители жиров — синтетические карбоновые жирные кислоты с большей молекулярной массой.
»
Почему мыло теряет свою моющую способность в жесткой воде?
Если мы используем для мытья и стирки жесткую воду, а такая вода содержит ионы Са 2+ и Mg2+,то мыло теряет свою моющую способность.
Химические свойства жиров обусловлены наличием:
сложных эфирных связей;
двойных связей в углеводородных радикалах жирных кислот;
наличием глицерина в составе жира.
Гидролиз, или омыление
В зависимости от условий гидролиз бывает:
кислотный (в присутствии кислоты в качестве катализатора);
щелочной (под действием щелочей);
водный (без катализатора, при высоких t0 и P);
ферментативный (происходит в живых организмах).
1. Кислотный гидролиз
Жирам как сложным эфирам свойственна обратимая реакция гидролиза, катализируемая минеральными кислотами:
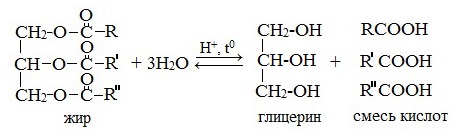
Вопрос 2
Кристаллическая решетка и металлическая связь
Металлы имеют металлическую кристаллическую решетку, в узлах которой расположены отдельные атомы. Они слабо удерживают валентные электроны, которые по этой причине свободно перемещаются по всему объему металла, формируя единое электронное облако и в равной степени притягиваются всеми атомами. Такая связь называется металлической.
Общие свойства металлов – пластичность, способность отражать свет, тепло- и электропроводность – объясняются особенностями их строения. При сильном надавливании кусок металла изменяет форму – часть атомов смещается, но не рассыпается: общее электронное облако прочно удерживает все атомы вместе. В электрическом поле свободные электроны начинают двигаться в определенном направлении, такое упорядоченное движение электронов называют электрическим током.
Чем больше в металле свободных электронов и чем сильнее колебания атомов, находящихся в узлах решетки, тем быстрее происходит выравнивание температуры во всем куске металла, то есть тем больше его теплопроводность. Поэтому относительные значения тепло- и электропроводности для многих металлов близки.
Физические свойства металлов
Агрегатное состояние и температуры плавления. Температуры плавления металлов меняются в очень широких пределах. Самый легкоплавкий из металлов – ртуть – при комнатной температуре является жидкостью. Металл галлий плавится от теплоты человеческого тела. Из металлов широко применяемых в технике, наиболее легкоплавкие – олово и свинец. Наибольшую температуру плавления имеет вольфрам, из которого изготавливают нити накаливания лампочек. Металлы с температурой плавления выше 1000oC принято называть тугоплавкими.
Электро- и теплопроводность. Все без исключения металлы хорошо проводят электрический ток. Наибольшей электропроводностью обладает серебро, немного уступают ему медь и золото. Серебро – очень дорогой металл. Его используют в электротехнике при изготовлении высокоточных дорогостоящих приборов. Самые хорошие провода, применяемые в быту, медные. Они во много раз превосходят по самим характеристикам провода, изготовленные из алюминия. При прохождении через металл электрического тока часть электрической энергии преобразуется в тепловую – металл нагревается. Использование алюминиевых проводов при больших нагрузках на электрическую сеть может привести к их плавлению. Особенно опасны места стыка алюминиевых и медных проводов – они нагреваются намного быстрее. Неисправная электропроводка является причиной многих пожаров.
Пластичность. Многие металлы пластичны, то есть обладают способностью изменять форму, например, расплющиваться при ударе молотком. Наибольшей пластичностью обладают золото, серебро, медь, олово. Их можно раскатывать в фольгу.
Вопрос 3
а) Fe + ZnSO₄ ≠б) 3Ag + AuCl₃ = 3AgCl + Au (восстановитель: Ag)в) Zn + 2HCl = ZnCl₂ + H₂↑(восстановитель: Zn)г) 2Al + 6H₂O = 2Al(OH)₃ + 3H₂↑ (t), (если удалить оксидную плёнку)(восстановитель: Al)д) 2Al + 3CuSO₄ = Al₂(SO₄)₃ + 3Cu(восстановитель: Al)е) Ag + H₂SO₄ (разб.) ≠ж) CuO + C = Cu + CO(восстановитель: C)з) Ba + 2H₂O = Ba(OH)₂ + H₂↑(восстановитель: Ba)