Файл: Отчет. Лабораторная работа 34 По дисциплине Аналитическа химия я наименование.docx
Добавлен: 10.01.2024
Просмотров: 17
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
ПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ РОССИИ

МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
федеральное государственное бюджетное образовательное учреждение
высшего образования
«САНКТ-ПЕТЕРБУРГСКИЙ ГОРНЫЙ УНИВЕРСИТЕТ»
Кафедра общей химии
Отчет. Лабораторная работа №3-4
По дисциплине: Аналитическа химия я
(наименование учебной дисциплины согласно учебному плану)
Тема: Разделение ионов по аналитическим группам и внутри группы
Автор: студент гр. ИЗБ-22-1 / Тригус Н.А/
(шифр группы) (Подпись) (ФИО)
ОЦЕНКА:
Дата:
ПРОВЕРИЛ
(должность) (подпись) (Ф.И.О.)
Санкт-Петербург
2023 г
РАЗДЕЛЕНИЕ ИОНОВ ПО АНАЛИТИЧЕСКИМ ГРУППАМ И ВНУТРИ ГРУППЫ
ЦЕЛЬ РАБОТЫ: Изучить реакции разделения катионов на аналитические группы и соответствующие схемы анализа.
Оборудование и реактивы
В штативе: хлорид натрия, хлорид калия, хлорид аммония, дигидроантимонат натрия, нитрат свинца (II), йодид калия, хромат калия, хлорид бария, сульфат натрия, хлорид кальция, ацетат натрия, сульфат магния, гидроортофосфат натрия, гидроксид аммония, сульфат марганца (II), хлорид железа (III), роданид (тиоцианат) калия, сульфат меди (II), сульфат кобальта (II), сульфат никеля (II), нитрат кадмия (II), гидроксид натрия, гидроксид калия – 5% растворы.
В лаборатории: держатели для пробирок, воронки, фильтры, индикаторная бумага, пробирки, стеклянные палочки
В вытяжном шкафу: соляная кислота, азотная кислота, серная кислота, уксусная кислота – 2 н. растворы, гидроксид калия, гидроксид натрия – 6 н. растворы, гидроксид аммония – концентрированный раствор, сульфид натрия – 5 % раствор, бромная вода, гексанитрокобальтат натрия, реактив Несслера, нитрат серебра, нитрат ртути (I), нитрат ртути (II) – 1 % растворы, нитрат натрия, нитрат калия, хлорид цинка, хлорид алюминия, хлорид хрома (III) – 5 % растворы; ацетон; гексацианоферрат (II) калия, гексацианоферрат (III) калия, тетрароданомеркурат (II) аммония – 5 % растворы, алюминон – 1% раствор, висмутат натрия крист., хлорид аммония крист., диметилглиоксим – 1 % спиртовой раствор, перекись водорода.
ВЫПОЛНЕНИЕ РАБОТЫ
АНАЛИЗ КАТИОНОВ ПЕРВОЙ И ВТОРОЙ АНАЛИТИЧЕСКИХ ГРУПП
1.Разделение катионов первой и второй аналитических групп.
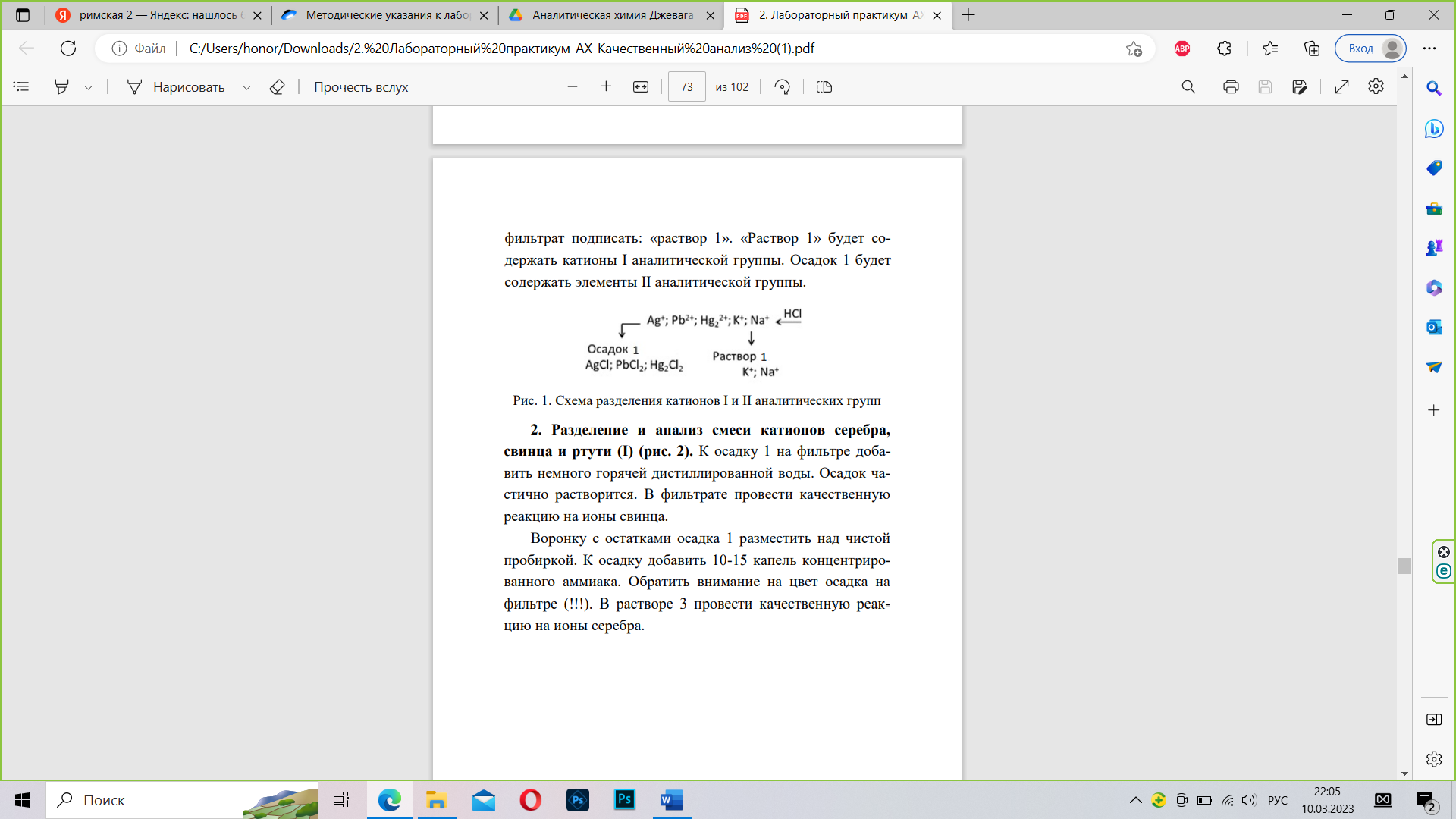
В пробирку налить по 3-4 капли растворов нитратов свинца, серебра, ртути (I), калия и натрия. К полученной смеси добавить около 3 мл дистиллированной воды, перемешать и добавить 3 мл 2 н. раствора соляной кислоты. Хлорид свинца трудно осаждаем, поэтому пробирку с раствором охладить под струей холодной воды и осаждать PbCl2, потерев стеклянной палочкой о внутренние стенки пробирки. Осадок отфильтровать. Воронку с осадком разместить над чистой пробиркой. Полученный 73 фильтрат подписать: «раствор 1». «Раствор 1» будет содержать катионы I аналитической группы. Осадок 1 будет содержать элементы II аналитической группы.
Наблюдаем образование осадка катионов II аналитической группы.

2. Разделение и анализ смеси катионов серебра, свинца и ртути (I).
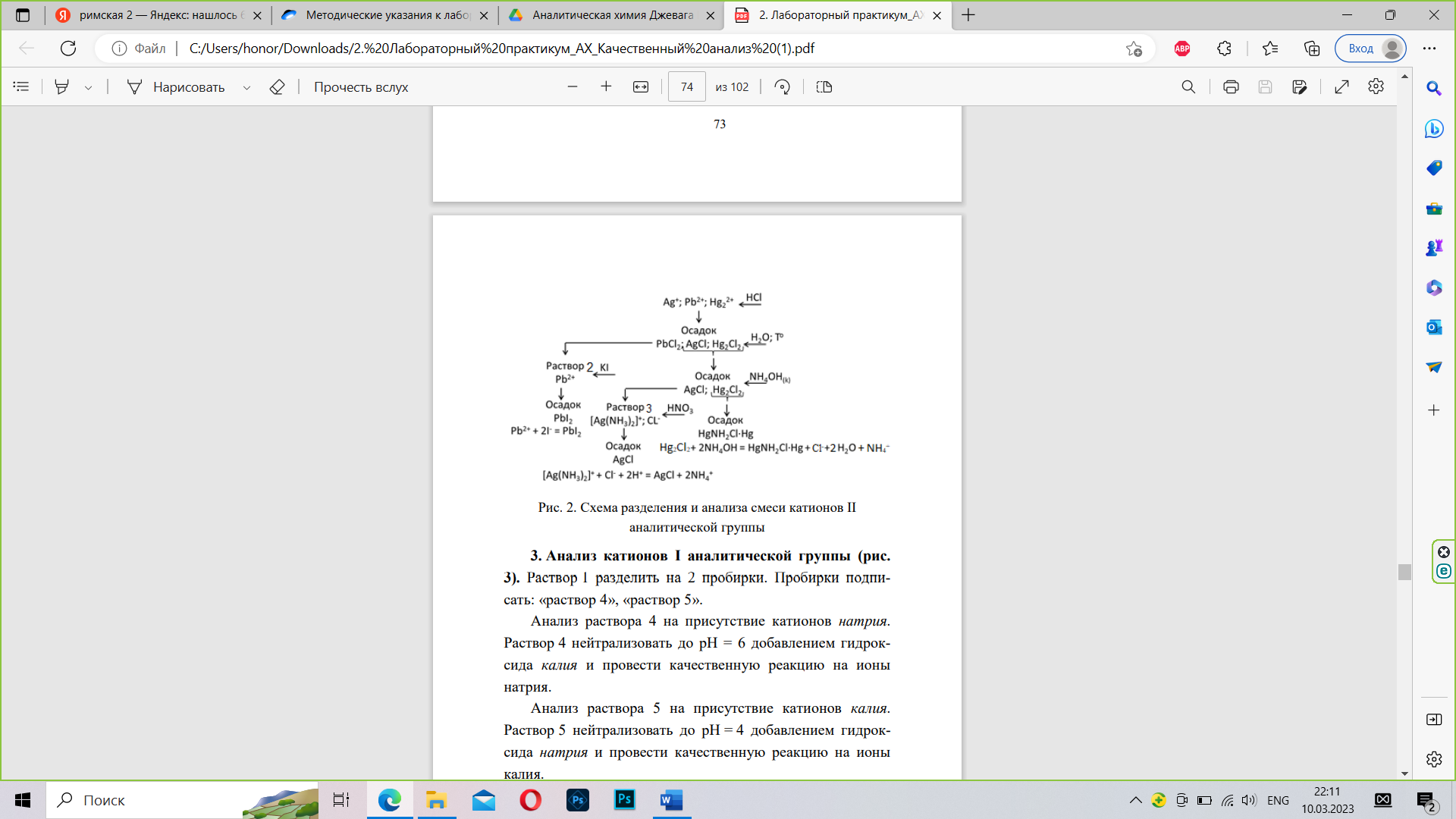
К осадку 1 на фильтре добавить немного горячей дистиллированной воды. Осадок частично растворится. В фильтрате провести качественную реакцию на ионы свинца. Воронку с остатками осадка 1 разместить над чистой пробиркой. К осадку добавить 10-15 капель концентрированного аммиака. Обратить внимание на цвет осадка на фильтре (!!!). В растворе 3 провести качественную реакцию на ионы серебра.
Наблюдаем растворение белого осадка, а затем его образование. На фильтре остался темный осадок HgNH2Cl*H.
3. Анализ катионов I аналитической группы.
Раствор 1 разделить на 2 пробирки. Пробирки подписать: «раствор 4», «раствор 5». Анализ раствора 4 на присутствие катионов натрия. Раствор 4 нейтрализовать до рН = 6 добавлением гидроксида калия и провести качественную реакцию на ионы натрия. Анализ раствора 5 на присутствие катионов калия.
Раствор 5 нейтрализовать до pH = 4 добавлением гидроксида натрия и провести качественную реакцию на ионы калия.
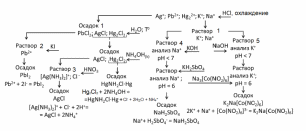
Наблюдаем образование белого осадка NaH2SbO4 и желтого осадка двойной основной соли K2Na[Co(NO3)6].

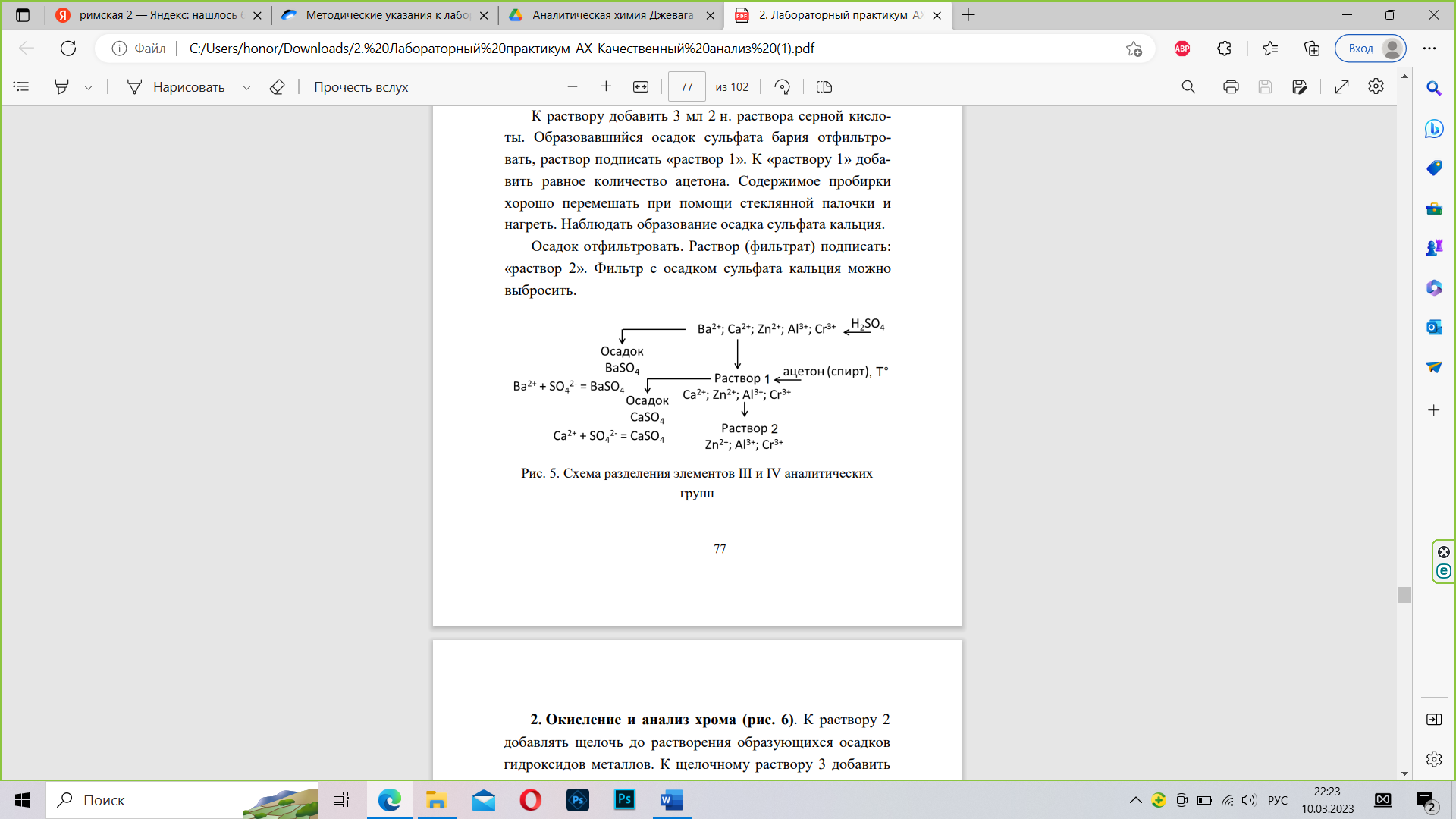
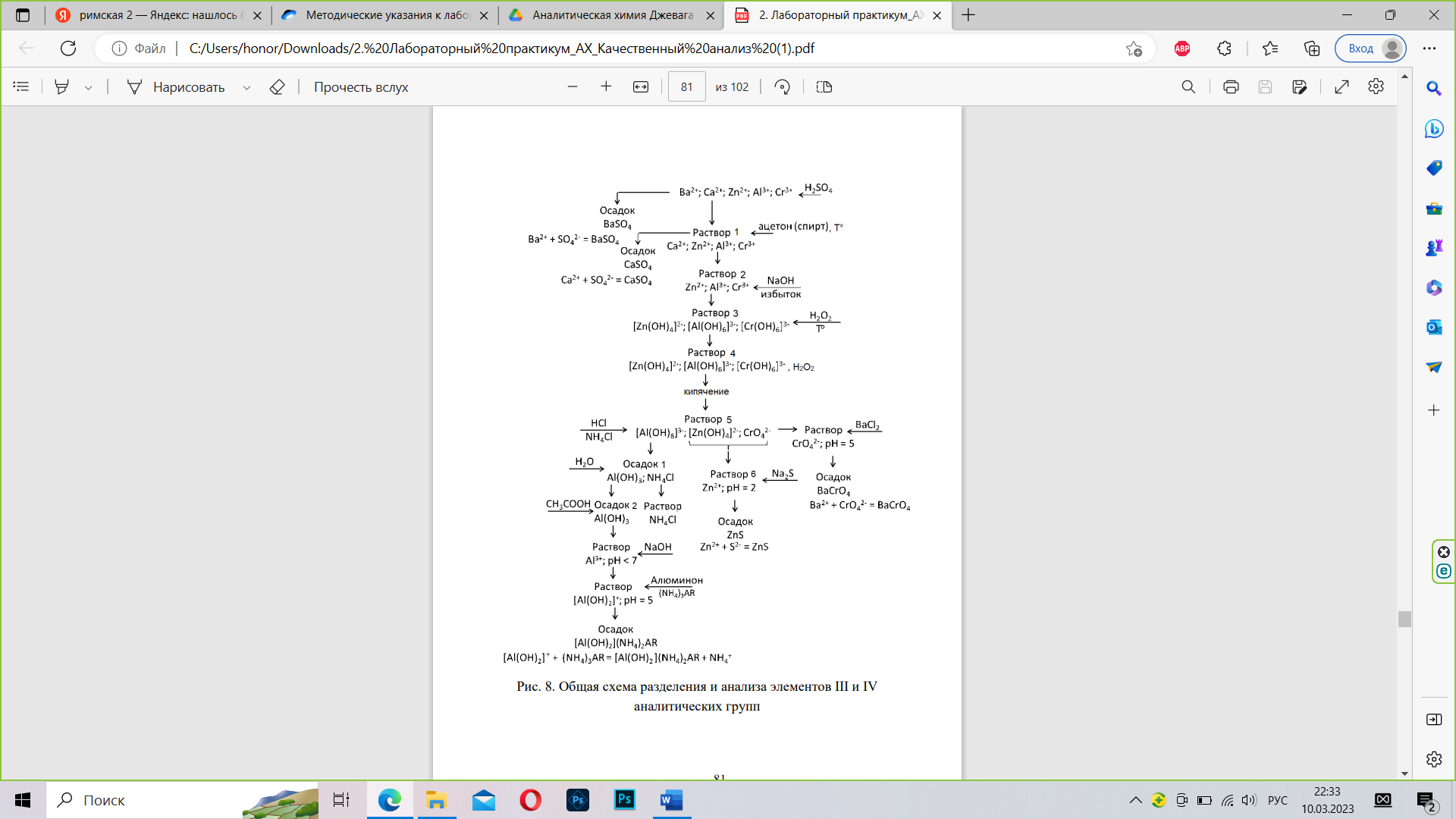
АНАЛИЗ КАТИОНОВ III И IV АНАЛИТИЧЕСКИХ ГРУПП 1.Разделение элементов III и IV аналитических групп и анализ бария и кальция (рис. 5). В чистую пробирку отобрать по 3-4 капли растворов солей бария, кальция, алюминия, цинка и хрома. К полученной смеси добавить около 3 мл дистиллированной воды и перемешать. К раствору добавить 3 мл 2 н. раствора серной кислоты. Образовавшийся осадок сульфата бария отфильтровать, раствор подписать «раствор 1». К «раствору 1» добавить равное количество ацетона. Содержимое пробирки хорошо перемешать при помощи стеклянной палочки и нагреть. Наблюдать образование осадка сульфата кальция. Осадок отфильтровать. Раствор (фильтрат) подписать: «раствор 2». Фильтр с осадком сульфата кальция можно выбросить.
Сначала образуется белый осадок сульфата бария. При добавлении ацетона и нагревании образуется белый осадок сульфата кальция.
2. Окисление и анализ хрома.
К раствору 2 добавлять щелочь до растворения образующихся осадков гидроксидов металлов. К щелочному раствору 3 добавить перекись водорода. Должен образоваться раствор желтого или оранжевого цвета (раствор 4). Пробу этого раствора отлить в чистую пробирку и проделать качественную реакцию на присутствие хрома. После окисления хром (VI) не мешает определению катионов Zn2+ и Al3+.
Н
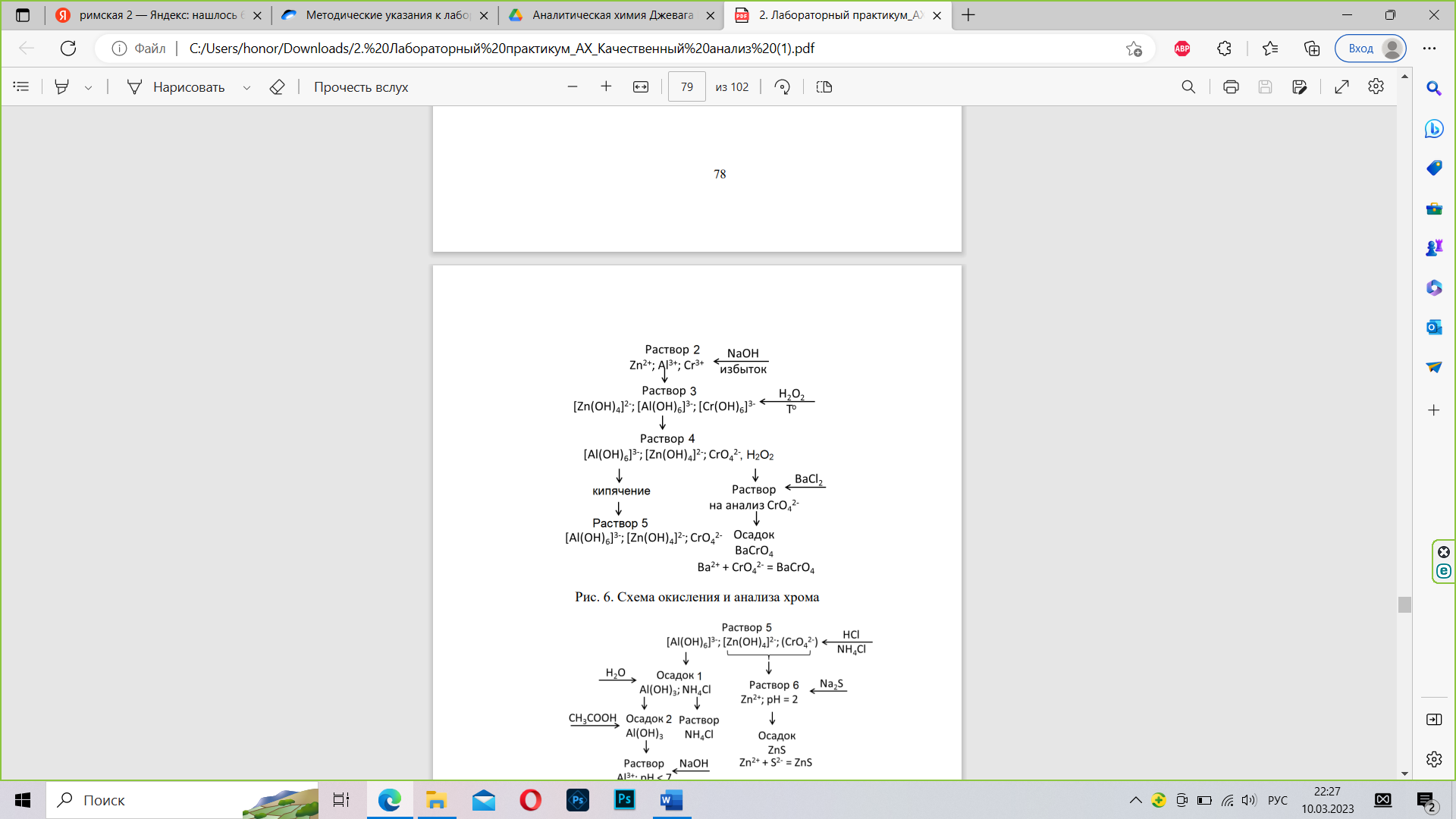 аблюдаем выпадение желтого осадка хромата бария
аблюдаем выпадение желтого осадка хромата бария3. Разделение и анализ алюминия и цинка.
Разделение алюминия и цинка. Раствор 4 прокипятить для удаления примеси перекиси водорода и охладить. К раствору 5 прибавить избыток хлорида аммония до образования насыщенного раствора. При помощи индикаторной бумаги определить рН полученной смеси и провести ее нейтрализацию до рН = 5. Отфильтровать образующийся осадок 1, представляющий собой смесь хлорида аммония и гидроксида алюминия. Раствор подписать: «Раствор 6».
4. Анализ алюминия. Воронку с осадком 1 разместить над чистой пробиркой. К осадку на фильтре добавить дистиллированную воду для растворения хлорида аммония. На фильтре останется только гидроксид алюминия. Раствор выбросить. Воронку с фильтром с осадком 2 гидроксида алюминия разместить над чистой пробиркой и к осадку на фильтре добавить 2 н. раствор уксусной кислоты. В полученном растворе провести качественную реакцию на присутствие катионов алюминия. Добавляем гидроксид аммония и алюминон. Образуется красный осадок.
5. Анализ цинка В растворе 6, после доведения его до pH = 2, провести качественную реакцию на цинк.
Наблюдаем выпадение белого осадка.
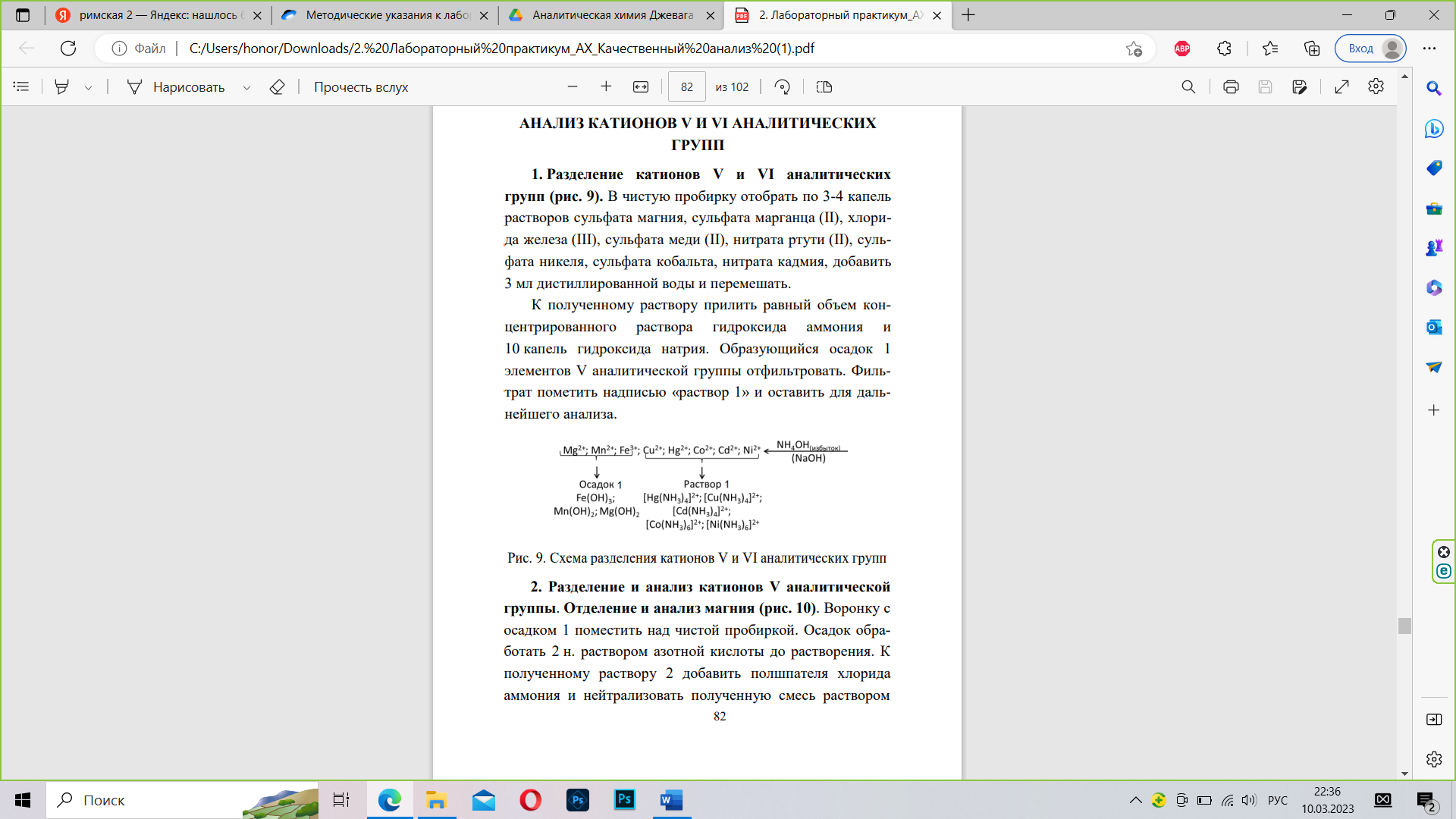
АНАЛИЗ КАТИОНОВ V И VI АНАЛИТИЧЕСКИХ ГРУПП 1. 1. 1.Разделение катионов V и VI аналитических групп.
В чистую пробирку отобрать по 3-4 капель растворов сульфата магния, сульфата марганца (II), хлорида железа (III), сульфата меди (II), нитрата ртути (II), сульфата никеля, сульфата кобальта, нитрата кадмия, добавить 3 мл дистиллированной воды и перемешать. К полученному раствору прилить равный объем концентрированного раствора гидроксида аммония и 10 капель гидроксида натрия. Образующийся осадок 1 элементов V аналитической группы отфильтровать. Фильтрат пометить надписью «раствор 1» и оставить для дальнейшего анализа.
2. Разделение и анализ катионов V аналитической группы.
Отделение и анализ магния (рис. 10). Воронку с осадком 1 поместить над чистой пробиркой. Осадок обработать 2 н. раствором азотной кислоты до растворения. К полученному раствору 2 добавить полшпателя хлорида аммония и нейтрализовать полученную смесь раствором 83 аммиака до рН = 9-10 по индикаторной бумаге. При этом железо и марганец должны выпасть в осадок 2 в виде гидроксидов, а магний остаться в растворе 3. Осадок 2 гидроксидов железа и марганца отфильтровать. Воронку с фильтром разместить над чистой пробиркой. В фильтрате (раствор 3) провести качественную реакцию на катион магния.
Образуется белый кристаллический осадок.
3.Анализ железа и марганца.
Фильтр с осадком 2 (гидроксиды железа (III) и марганца (II)) обработать 2 н. раствором азотной кислоты до растворения осадка. Раствор 4 поделить на 2 части. В одной части провести качественную реакцию на катион железа (III), в другой – качественную реакцию на катион марганца.
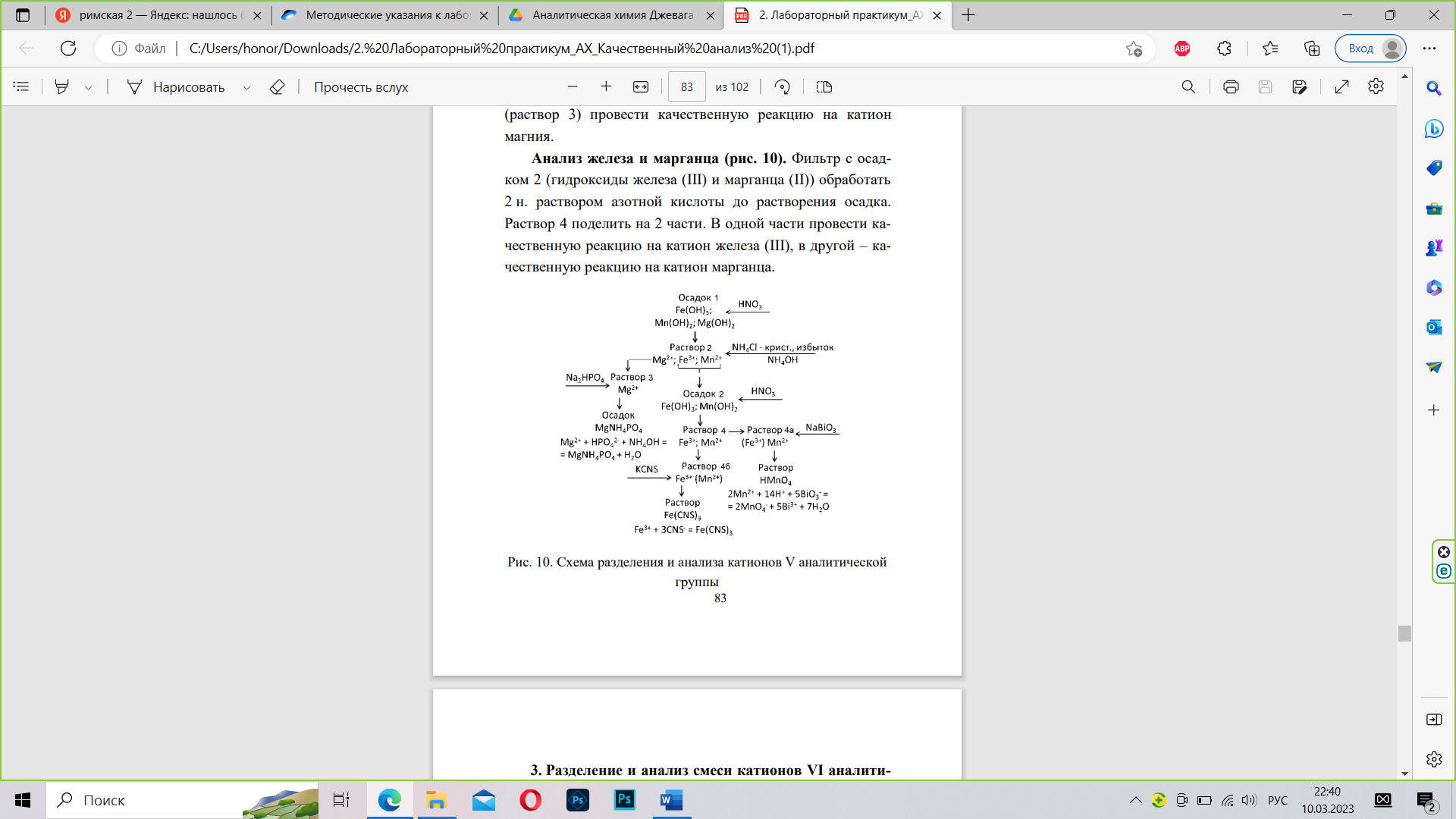
Образование кроваво-красного осадка, образование розового раствора.
4. Разделение и анализ смеси катионов VI аналитической группы. Отделение и анализ меди и ртути. При нагревании и энергичном перемешивании раствор 1 нейтрализовать 2 н. раствором серной кислоты до рН = 1−2. К раствору 5 при нагревании и энергичном перемешивании добавить 5-7 капель 2 н. раствора тиосульфата натрия Na2S2O3. Наблюдать образование темного осадка 3, содержащего сульфиды меди и ртути (II). Осадок отфильтровать. Фильтр с осадком разместить над чистой пробиркой. Фильтрат подписать: раствор 6. Осадок сульфидов меди и ртути (II) обработать 2 н. раствором азотной кислоты. При этом сульфид меди растворится, а ртуть останется в виде темного осадка на фильтре. В фильтрате провести качественную реакцию на присутствие ионов меди 2+.
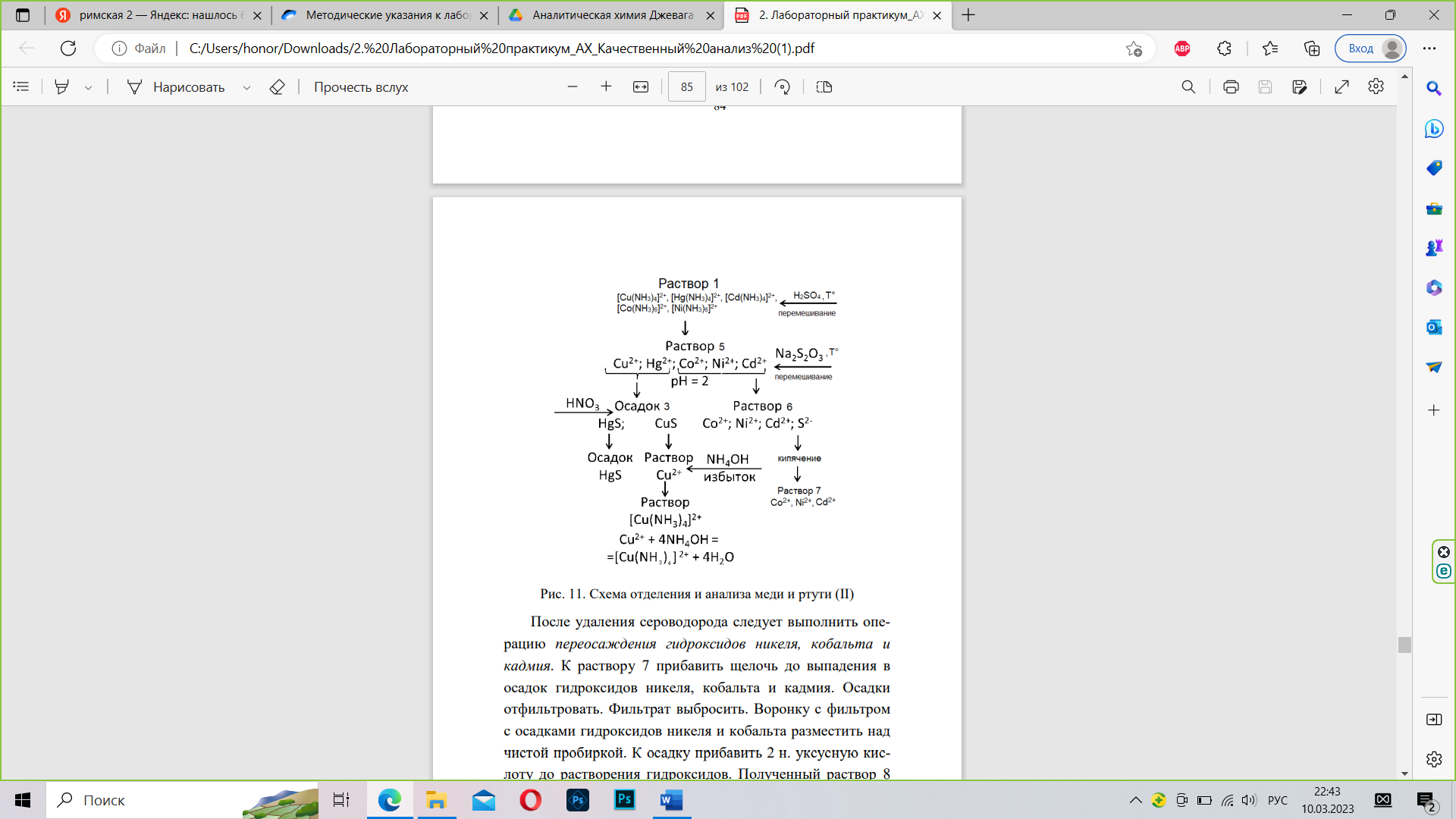
Образование зелено-голубого осадка, а затем его растворение с образование ярко-синего раствора.
5.Анализ никеля, кадмия, кобальта.
Раствор 6 прокипятить для удаления сероводорода. Проверка полноты удаления осуществляется на фильтровальной бумаге, смоченной раствором нитрата свинца: отсутствие черного (темного) пятна на смоченной Pb(NO3)2 фильтровальной бумаге после нанесения на нее капли раствора свидетельствует о полноте удаления сероводорода.
После удаления сероводорода следует выполнить операцию переосаждения гидроксидов никеля, кобальта и кадмия. К раствору 7 прибавить щелочь до выпадения в осадок гидроксидов никеля, кобальта и кадмия. Осадки отфильтровать. Фильтрат выбросить. Воронку с фильтром с осадками гидроксидов никеля и кобальта разместить над чистой пробиркой. К осадку прибавить 2 н. уксусную кислоту до растворения гидроксидов. Полученный раствор 8 разделить на 3 части. В одной провести качественную реакцию на катион никеля, в другой – на катион кобальта, в третьей – на катион кадмия.
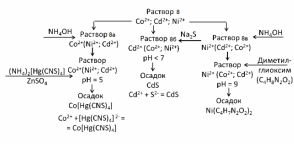
Образование коллоидного раствора желтого цвета, синий кристаллический осадок, малиновый осадок.
Вывод: я изучила реакции разделения катионов на аналитические группы и соответствующие схемы анализа.