Добавлен: 11.01.2024
Просмотров: 20
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
ПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ РОССИИ

МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
федеральное государственное бюджетное образовательное учреждение
высшего образования
«САНКТ-ПЕТЕРБУРГСКИЙ ГОРНЫЙ УНИВЕРСИТЕТ»
Кафедра общей и физической химии
Отчет по лабораторной работе №6
По дисциплине ОБЩАЯ ХИМИЯ
(наименование учебной дисциплины согласно учебному плану)
Тема: АНАЛИЗ СМЕСИ КАТИОНОВ ПЯТОЙ И ШЕСТОЙ АНАЛИТИЧЕСКИХ ГРУПП
Автор: студент группы ИЗБ-22-1 / Сень С. С. /
(шифр группы) (подпись) (Ф.И.О.)
ОЦЕНКА:
Дата: 2023 г.
ПРОВЕРИЛ / /
(должность) (подпись) (Ф.И.О.)
Санкт-Петербург
2023 г.
ЦЕЛЬ РАБОТЫ
Установить качественный состав раствора, содержащий катионы V и VI аналитических групп.
Оборудование и реактивы
В штативе: гидроортофосфат натрия, сульфат цинка, роданид (тиоцианат) калия, гидроксид аммония, гидроксид натрия, гидроксид калия – 5% растворы. В лаборатории: держатели для пробирок, воронки, фильтры, индикаторная бумага, пробирки, стеклянные палочки. В вытяжном шкафу: соляная кислота, азотная кислота, серная кислота – 2 н. растворы; гидроксид калия, гидроксид натрия – 6 н. растворы; гидроксид аммония – концентрированный раствор; сульфид натрия – 5 % раствор, гексацианоферрат (II) калия, гексацианоферрат (III) калия, тетрароданомеркурат (II) аммония – 5 % растворы, висмутат натрия крист., хлорид аммония крист., диметилглиоксим – 1 % спиртовой раствор.
Ход работы
Анализируемый раствор может содержать катионы пятой (Mn2+ , Mg2+ , и Fe3+) и шестой (Hg2+ , Cu2+ , Ni2+ , Co2+ , Cd2+) аналитических групп. Схема анализа приведена на рис. 1
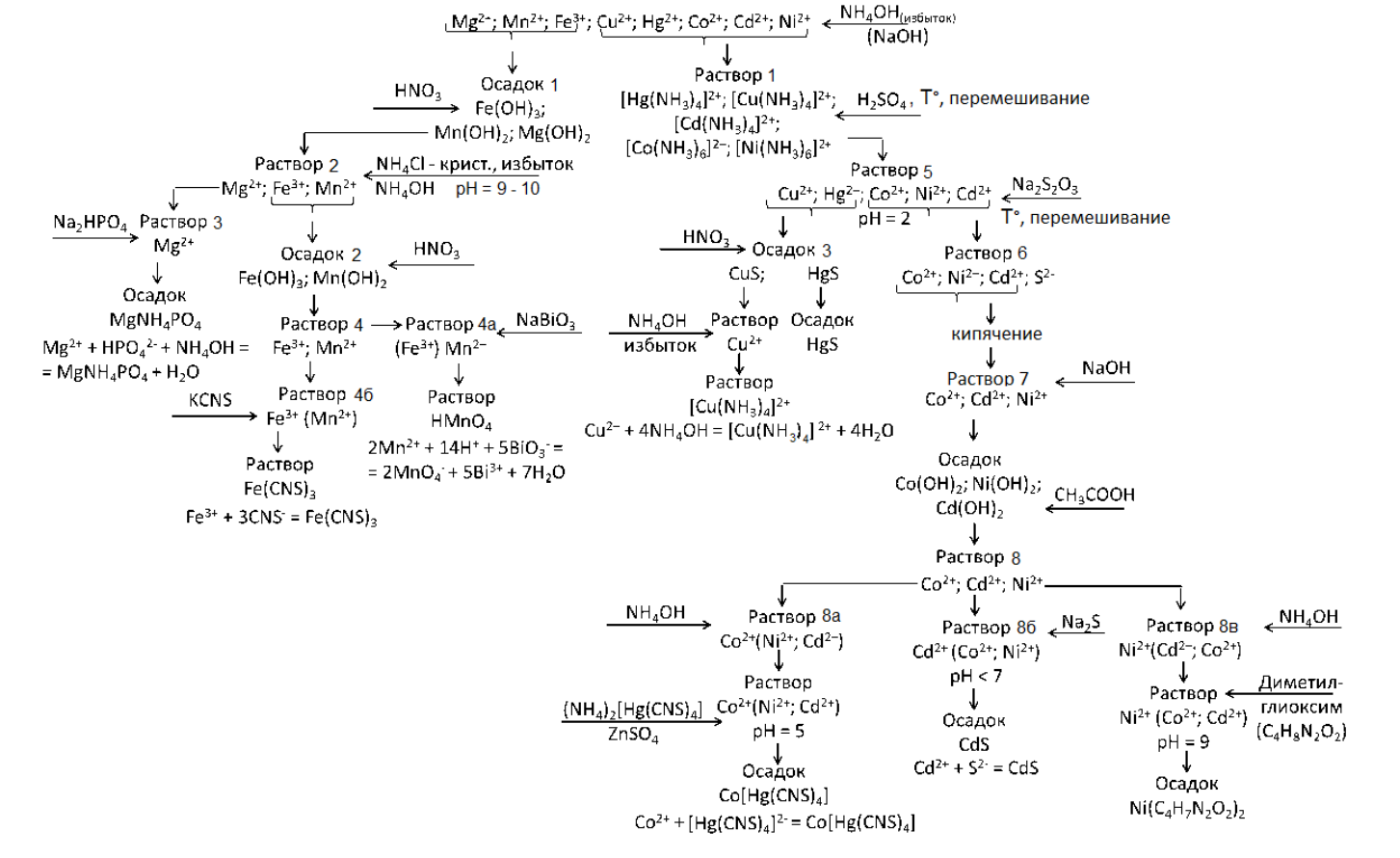
1. Провел предварительные испытания, целью которых является возможное упрощение схемы анализа; установление, как версии (но не как факта обнаружения), наличия или отсутствия в растворе определенного типа ионов.
При проведении предварительных испытаний выполнил дробный анализ раствора на обнаружение катионов
= Fe3+ по реакции с роданидом аммония или калия;
= Cu2+ по реакции с гидроксидом аммония;
= Hg2+ по реакции с медной пластинкой;
= Mn2+ по реакции с висмутатом натрия.
По результатам предварительных испытаний установил нахождение в растворе катиона Mn2+
Ход анализа: К двум каплям раствора соли марганца (II) прибавил 2 мл раствора азотной кислоты 1 : 1 и немного кристаллического висмутата натрия. Смесь перемешал. При этом образовался раствор марганцовой кислоты розового цвета.
2. Разделил катионы V и VI групп, последовательно добавив избыток концентрированного раствора гидроксида аммония; нескольких капель 6 н. раствора гидроксида калия или натрия для полного выделения катионов магния в виде Mg(OH)2. После фильтрации получаю: осадок 1, содержащий гидроксиды V аналитической группы, и раствор 1, содержащий аммиакаты VI (аммиачной) аналитической группы.
3. Растворение осадка катионов V аналитической группы. Осадок 1 на фильтре растворил 2 н. азотной кислотой. Растворимость гидроксидов группы увеличивается в следующей последовательности: Fe(OH)3 – Mn(OH)2 – Mg(OH)2. В азотнокислой среде магний обязательно перейдет в раствор, а часть гидроксидов железа и марганца может остаться на фильтре в виде бурого осадка.
4. Отделение магния. К раствору 2 прибавил полшпателя кристаллического хлорида аммония и нейтрализовал раствор до рН = 10-11. Осадок отфильтровал. В фильтрате 3 – катион магния, в осадке 2 – гидроксиды железа и марганца.
5. Анализ присутствия магния. В растворе 3, полученном в п. 4, провел качественную реакцию на магний.
В ходе данной реакции белого кристаллического осадка двойной соли ортофосфата аммония-магния не образовалось
Ионы Cu2+ и Hg 2+ в анализируемом растворе отсутствуют, операция их удаления из раствора исключается.
10. Анализ катионов Ni2+ , Co2+ и Cd2+
К раствору 7 прибавил щелочь до выпадения в осадок гидроксидов никеля, кобальта и кадмия. Осадки отфильтровал. Фильтрат выбросил. Воронку с фильтром с осадками гидроксидов никеля, кобальта и кадмия разместил над чистой пробиркой. К осадку прибавил 2 н. уксусную кислоту до растворения гидроксидов. Полученный раствор 8 разделил на 3 части. В одной провел качественную реакцию на катион никеля, в другой – на катион кобальта, в третьей – на катион кадмия. По итогу был выявлен только катион кадмия.
Образовался желтый осадок сульфида кадмия
Вывод: В ходе данной работы я установил, что в растворе под номером 38 содержатся катионы марганца и кадмия.