Файл: Лабораторная работа По дисциплине Методы и приборы контроля ос и экологический мониторинг Тема Атомноабсорбционная спектрометрия Автор студент гр. Изб201 Суржик М. Е.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 72
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
ПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ РОССИИ

МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
федеральное государственное бюджетное образовательное учреждение
высшего образования
«САНКТ-ПЕТЕРБУРГСКИЙ ГОРНЫЙ УНИВЕРСИТЕТ»
Кафедра геоэкологии
Лабораторная работа
По дисциплине: Методы и приборы контроля ОС и экологический мониторинг
Тема: Атомно-абсорбционная спектрометрия
Автор: студент гр. ИЗБ-20-1 Суржик М.Е.
(шифр группы) (подпись) (Ф.И.О.)
Дата:
ПРОВЕРИЛ доцент, к.т.н Чукаева М.А
(должность) (подпись) (Ф.И.О.)
Санкт-Петербург
2023 год
Цель работы: определение массовой концентрации катионов Ca и Mg в пробах воды методом атомно-абсорбционная спектрометрии, на основе полученных значений концентрацией определить общую жесткость проб воды.
Теоретические сведения
Атомно-абсорбционная спектрометрия – метод количественного физико-химического анализа, позволяющий определять около 70 элементов – металлов, металлоидов (As, B, Ge, Si, Te, Sb) и некоторых неметаллов (P, I, Se). Важные элементы, такие как сера, азот, кислород, галогены не определяются.
Метод ААС основан на поглощении излучения оптического диапазона невозбужденными свободными атомами в газообразном состоянии. В основе метода лежит закон Бугера-Ламберта-Бера:
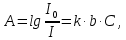
где: А – атомное поглощение, k – коэффициент атомного поглощения, b – толщина поглощаемого слоя, C – концентрация определяемого элемента.
Для анализа методом ААС используют преимущественно жидкие пробы либо же суспензии, гораздо реже анализируют твердые вещества, порошки.
Достоинства метода атомно-абсорбционной спектрометрии:
-
Хорошая воспроизводимость результатов; -
Простота анализа; -
Возможность коррекции неселективного поглощения; -
Определение как макро-, так и микрокомпонентов.
Недостатки:
1. Необходимость перевода анализируемого образца в раствор;
2. Невозможность определения ряда элементов
3. Потребность в дополнительных комплектующих и расходных материалах.
Сведения о приборе
Анализ проводился на двухлучевом атомно-абсорбционном спектрометре SHIMADZU АА-7000 для пламенного и электротермического атомно-абсорбционного анализа (ААС). На данном АА-спектрометре возможно использование 2 видов атомизаторов: электротермический и пламенный.
Электротермический атомизатор может использоваться при определении такого элемента, как хром при 2700°С. (Графитовые печи выдерживают более высокие температуры и делают возможным высокотемпературный анализ).
Пламенный атомизатор, используемый в ходе лабораторной работы, состоит из титановой горелки, распылительной камеры из термоустойчивого и ударопрочного пластика, платино-иридиевого распылителя и керамического импактора. При пламенной ААС проба готовится в жидком виде и распыляется в пламя. Возможность быстрого анализа, хорошая воспроизводимость, а также относительная простота в эксплуатации относятся к преимуществам данного вида атомизации пробы. К недостаткам относятся чувствительность, необходимость подачи воспламеняемых газов и необходимость отсутствия в пробе избыточных количеств растворенных твердых веществ.
Пробоподготовка
Перед проведением анализа проба подвергаться лишь фильтрованию с помощью фильтровальной бумаги.
Также для проведения анализа были подготовлены стандартные образцы с известными концентрациями катионов Ca и Mg для проведения градуировки. В таблице 1 представлены значения концентраций. Расчеты проб аликвоты проводились по формуле 1.
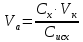 , мл (1)
, мл (1)Где:
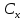 – значение нужной концентрации, мг/л
– значение нужной концентрации, мг/л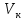 – объем колбы, мл
– объем колбы, мл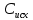
– исходная концентрация, мг/л
Исходная концентрация катионов Са и Mg – 100 мг/л, объем колбы – 50 мл. Приведем пример расчетов для Mg;
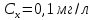 :
: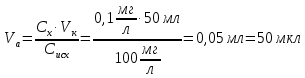 – данное значение меньше 100 мкл, и так как этот объем невозможно отобрать, приготовим промежуточный раствор с концентрацией 10 мг/л.
– данное значение меньше 100 мкл, и так как этот объем невозможно отобрать, приготовим промежуточный раствор с концентрацией 10 мг/л.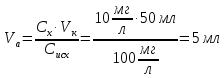 – для того, чтобы приготовить промежуточный раствор с концентрацией Mg 10 мг/л нужно отобрать 5 мл раствора с концентрации 100 мг/л, а оставшийся объем колбы довести дистиллированной водой.
– для того, чтобы приготовить промежуточный раствор с концентрацией Mg 10 мг/л нужно отобрать 5 мл раствора с концентрации 100 мг/л, а оставшийся объем колбы довести дистиллированной водой.Тогда для отбора аликвоты Mg с
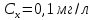 потребуется:
потребуется: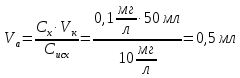
Этот промежуточный раствор будет использовать в дальнейших расчетах в случае Mg; для Ca исходной концентрацией останется 100 мг/л.
По формуле 1 были рассчитаны оставшиеся объемы аликвоты.
Таблица 1 – Основа для приготовления градуировочных растворов
| № пробы со значениями концентраций, мг/л |  , мл , мл | 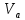 для Ca, мл для Ca, мл | 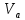 для Mg, мл для Mg, мл |
| 0 – дистиллированная вода | |||
| 1 – 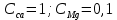 | 50 | 0,5 | 0,5 |
| 2 – 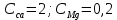 | 50 | 1 | 1 |
| 3 – 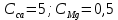 | 50 | 2,5 | 2,5 |
| 4 – 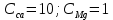 | 50 | 5 | 5 |
Ход работы
1. Пробоподготовка:
1) Фильтрование двух проб воды через бумажный фильтр;
2) Разбавление двух проб для сравнения сигнала абсорбции.
2. Определяемые компоненты Mg и Ca – макрокомпоненты в воде, поэтому для анализа в качестве атомизатора выбрано пламя;
3. В качестве значений для градуировочного графика для Ca выбраны следующие концентрации: 0 мг/л , 1 мг/л, 2 мг/л, 5 мг/л, 10 мг/л; для Mg: 0 мг/л , 0,1 мг/л, 0,2 мг/л, 0,5 мг/л, 1 мг/л. Приготовлены стандартные растворы.
4. Работа с прибором:
1) включение прибора (пламени);
2) ввод данных для проведения анализа в программе (установка нужной лампы, ее прогрев, корректировка исходящего излучения в нужную область, при необходимости установление нужной длины волны);
3) калибровка прибора (фиксация абсорбционного сигнала в порядке возрастания массовой концентрации определяемого элемента);
4) промывка дистиллированной водой;
5) ввод пробы;
4) проведение анализа программой;
5) промывка водой;
6) ввод следующей пробы.
Результаты измерений
На лабораторной работе нашей бригадой были проанализированы 2 пробы воды: из общежития №3 на ул. Наличной 46 и вода из крана Горного университета.
В процессе проведения анализа программа строит график в координатах время- сигнал абсорбции и по ранее построенному градировочному графику определяет концентрацию. Выдаваемый программой результат представлен на рисунке 1.
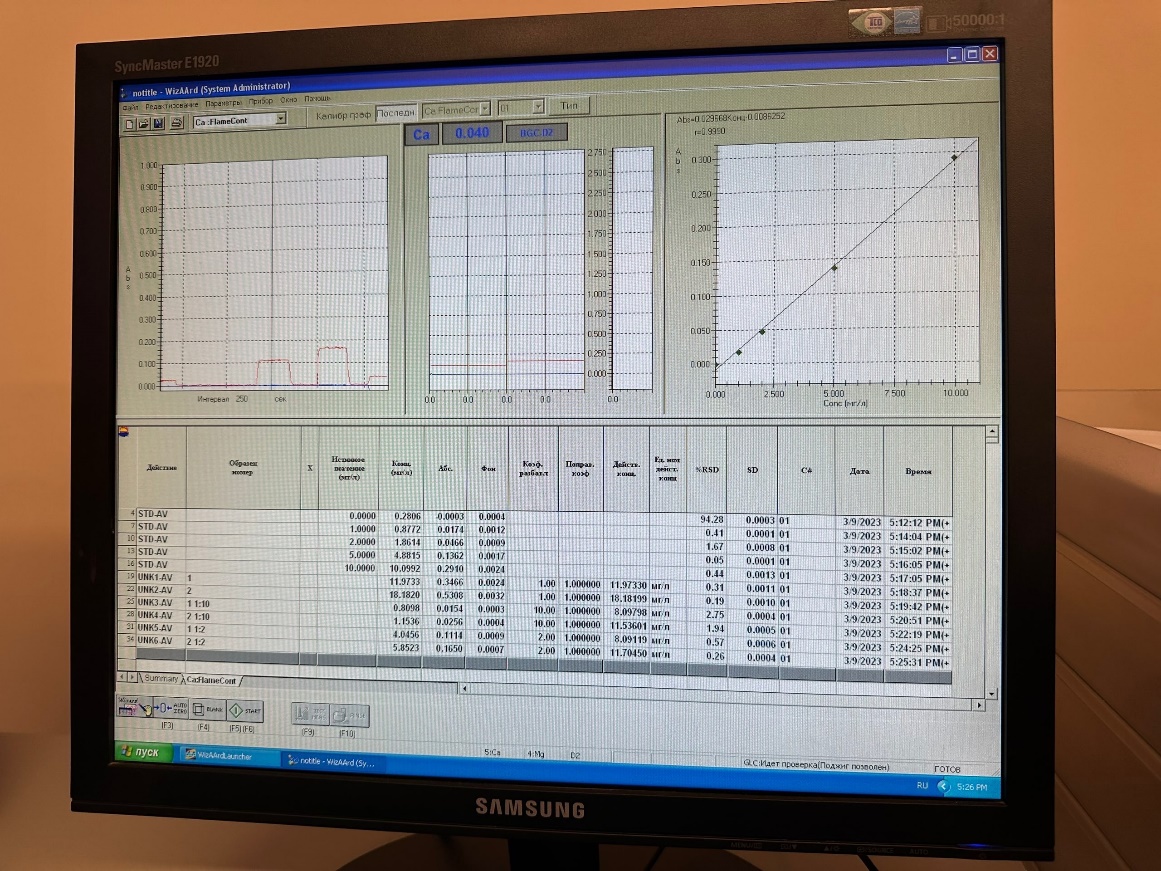
Рисунок 1 – Результаты измерений для Ca
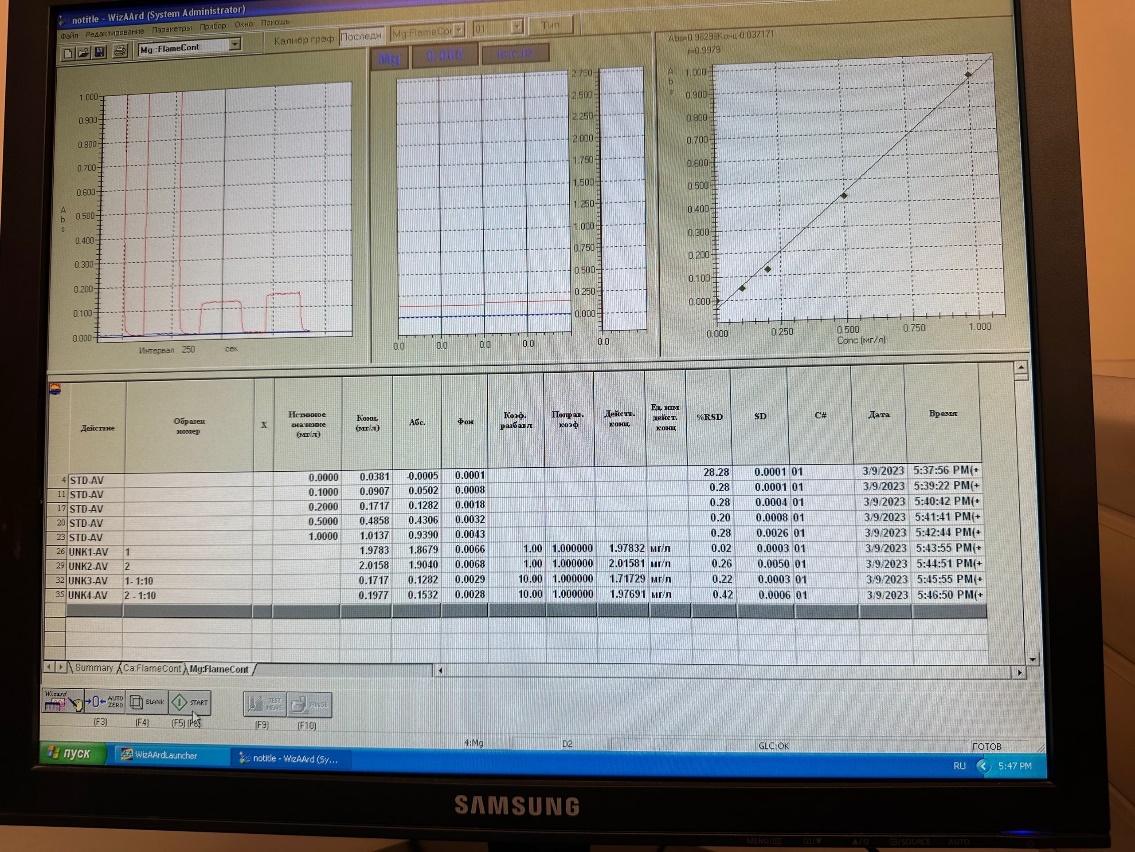
Рисунок 1 – Результаты измерений для Mg
Таблица 2 – Данные для построения градуировчных графиков
| Значения концентраций (Ca), мг/л | Сигнал абсорбции для Ca | Значения концентраций (Mg), мг/л | Сигнал абсорбции для Mg |
| 0 | -0,0003 | 0 | -0,0005 |
| 1 | 0,0174 | 0,1 | 0,0502 |
| 2 | 0,0466 | 0,2 | 0,1282 |
| 5 | 0,1362 | 0,5 | 0,4306 |
| 10 | 0,2910 | 1 | 0,9390 |
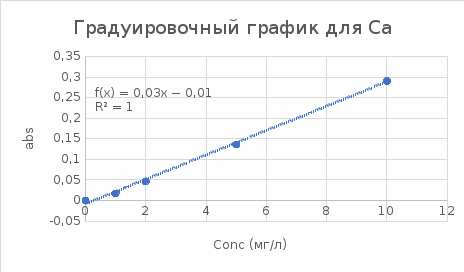
Рисунок 3 – Градуировочный график для Ca
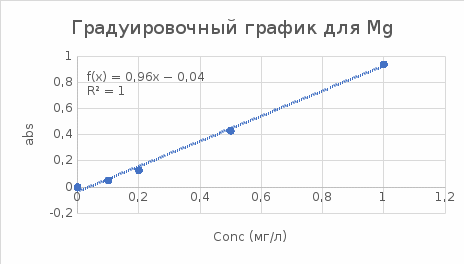
Рисунок 4 – Градуировочный график для Mg
В таблице 3 и 4 представлены результаты измерений концентрацией катионов. Определение погрешностей производилось с согласно методике М-02-2406-13 по формуле:
Где U0 - относительная расширенная неопределенность измерений при k=2, значение в %.
Таблица 3 – Концентрации катиона Ca
Название пробы | Сигнал абсорбции | Измеренная концентрация, мг/л | Коэффициент разбавления | Действительная концентрация, мг/л | Погрешность, мг/л | Результат измерения с учетом погрешности, мг/л |
1 (Общежитие) | 0,1114 | 4,0456 | 2 | 8,09119 | 1,0 | 8,0 |
2 (Горный) | 0,1650 | 5,8523 | 2 | 11,70450 | 1,5 | 11,7 |
Таблица 4 – Концентрации катиона Mg
Название пробы | Сигнал абсорбции | Измеренная концентрация, мг/л | Коэффициент разбавления | Действительная концентрация, мг/л | Погрешность, мг/л | Результат измерения с учетом погрешности, мг/л |
1 | 0,1282 | 0,1717 | 10 | 1,71729 | 0,2 | |
2 | 0,1532 | 0,1977 | 10 | 1,97691 | 0,2 | |
 1,0
1,0