ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.12.2023
Просмотров: 132
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
=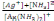 .
.
73. Стандартты тотығу-тотықсыздану жұбының потенциалына сәйкес келетін жағдай
A) Т > 298 К.
B) Т < 293 К.
C) n > 1.
D) [Ox] = [Red] = 1.
E) [Red] < 1.
74. Әлсіз тотықсыздандырғыш қасиет көрсететін қосылыс және оған сәйкес жұп
A) (NH4)2S2O8 , φo (S2O82- / 2SO42-) = +2,01 В.
B) KIO4, φo (IO4-/I3-)=+1,28 B.
C) O20 , φo(O2/H2O2)=+0,69 B.
D) Br2o, φo(Br2/2Br-)=+1,09 B.
E) KMnO4, φo(MnO4-/Mn2+)=+1,51B.
75. [Fe3+] / [Fe2+] жұбы төмендегі қай қатынасқа тең болғанда редокс жұбының потенциалыстандарттан үлкен болады (φ°( (Fe3+/Fe2+) < φ°(Fe3+/Fe2+))
A) 1:10.
B) 1:1.
C) 10 : 1.
D) 5:2.
E) 5:5.
76. Ерітінді рН мәнінің өзгеруі потенциалына әсер етпейтін редокс жұбтары
A) J20 / 2J-, Fe3+ / Fe2+.
B) NO3- / NO, Cr2O72- / 2Cr3+.
C) Cr2O72- / 2Cr3+, Fe3+ / Fe2+.
D) NO3- / NO, J20 / 2J-.
E) SO32- / H2S, NO3- / NO.
77. Тотықтырғыш KMnO4 –тың күшті қышқылдық ортада тотықсыздану реакциясы және оған
сәйкес редокс потенциалы
A) MnO4- + 8H+ +5e → Mn2+ + 4H2O, φ0 = +1,51B.
B) MnO4- + 4H+ + 3e-→MnO20 + 2H2O, φ°=+1,69 B.
C) MnO4- + 2H+ + 3e- → MnO20 + 4OH-, φ° =+0,59 B.
D) MnO4- + 4OH- + e- → MnO42- + 2H2O + O20, φ° =+0,58 B.
E) MnO4- - e- → Mn0 + 2O20, φ°= +1,18 B.
78. Стандартты редокс потенциалдары φ°(BrO3-/Br-) = +1,42 B және φ°(Br20/2Br-) = +1,09B тең жүйедегі BrO3- + 5Br- + 6H+ → 3 Br20 + 3H2O реакциясы
*солдан оңға қарай жүреді
*оңнан солға қарай жүредi
*реакция жүруi мүмкiн емес
*реакция тепе-теңдiкте болады
*редокс потенциалы ешқандай мәлiмет бермейдi
79. Ерітіндідегі Ag+, Zn2+, Cu2+,Ni2+, Co2+ иондар қоспасына HCl ертіндісін қосқанда тұнбаға түсетін ион
A) Ag+.
B) Zn2+.
C) Cu2+.
D) Ni2+.
E) Co2+.
80. Ертіндідегі Al3+, Zn2+, Cr3+, Fe3+, Sn4+ иондар қоспасына NaOH ертіндісінің артық мөлшерін қосқанда тұнбаға түсетін катион
A) Al3+.
B) Zn2+.
C) Cr3+.
D) Fe3+.
E) Sn4+.
81. Қызыл қан тұзының ионы
A) [Fe(CN)6]3-.
B) [Fe(CN)6]4-.
C) [HgJ4]2-.
D) ClO3-.
E) NO2-.
82. Калий ионынмен микрокристаллоскопиялық реакция беретін реактив
A) Na3[Co(NO2) 6].
B) Na2Pb[Cu(NO2)6].
C) K2[HgJ4].
D) NaHC4H4O6.
E) CH3COOН.
83. IV,V,VI топ гидроксидтері ерітінділеріне концентрлі аммиак ерітіндісімен әсер еткенде ерітінідіге өтетін катиондар тобы
A) II.
B) VI.
C) IV.
D) V.
E) III.
84. Калий ионын Na3 [Co(NO2)6] реактивімен ашуда кедергі келтіретін реагент
A) H2O.
B) Na2SO4.
C) NH4Cl.
D) NaCl.
E) NaNO3.
85. Ca2+ ионын Ba2+ ионынан бөледі
A) Сірке қышқылының еритін тұздарымен.
B) Калий хроматымен.
C) Алдымен құмырсқа қышқылымен, кейін калий дихроматы.
D) Калий дихроматымен,рН = 5 ортада.
E) Құмырсқа қышқылы және калий хроматымен.
86. Жүйелік талдауда барий ионын калий дихроматымен K2Cr2O7 бөлетін және ашатын буферлік жүйе
A) Na2HPO4 + NH2PO4.
B) CH3COOH + CH3COONa.
C) HCOOH + HCOONa.
D) NH4OH + NH4Cl.
E) H2CO3 + NaHCO3.
87. Кобальт және никель сульфиттерін еріту үшін қолданатын реактив
A) H2SO4.
B) NaOH.
C) (NH4)2S.
D) HCl + H2O2.
E) H2O.
88. Мырыш, қалайы және кадмий тұздары ерітінділері қоспасына KOH ерітіндісінің артық мөлшерін қосқанда тұнбаға түседі
A) Zn(OH)2.
B) Sn(OH)2.
C) Барлық иондар тұнбаға бірге түседі.
D) Cd(OH)2.
E) Тұнбаға түспейді.
89. Барий, қорғасын және кальций тұздары ерітінділері қоспасына аммоний сульфаты ерітіндісінің артық мөлшерін қосқанда тұнбаға түседі
A) PbSO4, BaSO4, CaSO4.
B) BaSO4.
C) PbSO4, BaSO4.
D) BaSO4, CaSO4.
E) PbSO4.
90. Мышьяк (III) және сурьма (III) сульфидтерін еріту үшін қолданатын реактив
A) CH3COOH.
B) (NH4)2Sx.
C) (NH4)2CO3.
D) (NH4)2S.
E) H2S.
91. Ag2S тұнбасын ерітетін реактив
A) HCl.
B) Na2S.
C) NaOH.
D) KCN.
E) H2SO4.
92. Қорғасын мен барий сульфаттарын бөлу үшін қолданатын реагент
A) HCl.
B) NH4Cl.
C) CH3COONH4.
D) NH4OH.
E) NaOH.
93. Hg2(NO3)2 ерітіндісіне SnCl2 реагентін қосқанда түзілетін өнімдер
A) HgCl2+Sn0.
B) Hg0+SnCl4.
C) HgCl2+Sn(NO3)2.
D) Hg2Cl2
+Sn0.
E) Hg0+Sn0.
94. Al3+ ионымен ашық қызыл түсті қосылыс түзетін реактив
A) Ализарин .
B) Несслер реактиві.
C) Дитизон.
D) Тиомочевина.
E) Бензидин.
B) NH4OH.
C) Na2S2O3.
D) K4[Fe(CN)6].
E) K3[Fe(CN)6].
95. VI аналитикалық топтың катиондарымен негіздік тұз түзетін реактив
A) Na2SO4.
B) NH4OH(конц).
C) NaOH.
D) NaH2PO4.
E) H2S.
96. Жүйелік талдауда никель ионын ашатын реактив
A) Ильинский.
B) Чугаев.
C) Ринман.
D) Фишер.
E) Тенаров.
97. AI3+ ионының топ реагентімен әрекеттесуінен түзілетін қосылыс
A) AI(OH)3.
B) AI2O3.
C) NaAIO2.
D) HAIO2.
Е) КAIO2
98. Cr3+ ионының Н2О2 қатысында топ реагентімен әрекеттесуінен түзілетін қосылыс
A) Cr2O3.
B) (CrOH)3.
C) Na2CrO4.
D) NaCrO2.
E) Na2Cr2O7.
99. Топ реагентінің Co2+ ионымен әрекеттесуінен түзілетін қосылыс
A) [Cо(NH3)6]2+.
B) Co(OH)2.
C) CoO.
D) Co(OH)3.
E) CoSO4.
100. Hg22+ ионының топ реагентімен әрекеттесуінен түзілетін қосылыс
A) HgO.
B) Hg2(OH)2.
C) Hg(NO3)2.
D) Hg2CI2.
E) HgSO4.
101. Аммиакатты комплексті қосылыс түзетін катиондар
A) Na+, Ca2+, Zn2+.
B) K+, Ba2+, Zn2+.
C) Ag+, Cd2+, Cu2+.
D) Ca2+, K+, Cu2+.
E) Ba2+, Na+, Cd2+.
102. Массаны дәл өлшеуге негізделген талдау
A) Титриметрия.
B) Потенциометрия.
C) Гравиметрия.
D) Амперометрия.
E) Кулонометрия.
103. 2, 5324 г өлшенген массаның дәлдігі
A) 1.
B) 0,1.
C) 0,01.
D) 0,001.
C) 0,0001.
104. Аморфты тұнба түзілетін жағдайдағы гравиметриялық түрдің массасы (г) болу керек
A) 0,01.
B) 0,1.
C) 0,5.
D) 1,0.
E) 10,0.
105. Кристалды тұнба түзілетін жағдайдағы гравиметриялық түрдің массасы (г) болу керек
A) 0,01.
B) 0,1.
C) 0,5.
D) 1,0.
E) 10,0.
106. Темірді гравиметриялық анықтаудағы пайдаланылатын аналитикалық көбейткіштің F(Fe/Fe2O3)=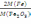 = 0,6994 алымындағы шама
= 0,6994 алымындағы шама
A) Анықтайтын заттың түр.
B) Тұндырушының түр.
C) Сынама формуласы.
D) Өлшенетін түрі.
E) Тұндырылған түрі.
107. Өлшеудегі ауытқу немесе қателік
A) Өлшенетін шаманың нақты мәнінен өлшеу нәтижесінің ауытқуы.
B) Абсолютті ауытқудың орташа мәнге қатынасы.
C) Өлшеу қателігі қайта өлшеу кезінде тұрақты болады немесе белгілі бір зандылықпен өзгереді.
D) Өлшеу қателігінің қайта өлшеу кезінде кездейсоқ өзгеруі.
E) Белгілі жағдайда байқалатын қателіктен артық болатын өрескел қате.
108. Аналитикалық таразыда өлшеу дәлдігі
A) 1,0 • 10-1г.
B) 1,0 • 10-5г.
C) 1,0 • 10-2г.
D) 1,0 • 10-4г.
E) 1,0 • 10-3г.
109. Тұнбаға түсіруші реагенттің қосылатын мөлшері артық болу керек
A) 5 есе.
B) 2 есе.
C) 6 есе.
D)1,5 есе.
E) 0,5 есе.
110. Мор тұзының құрамындағы темірді анықтауда тұнбаны қай ионнан жуады
A) SO42-.
B) NO3-.
C) OH-.
D) Cl-.
E) NH4+.
111. Барий хлоридінен барийді гравиметриялық анықтауда тұнбаны қай ионнан жуады
A) SO42-.
B) NO3-.
C) OH-.
D) Cl-.
E) NH4+.
112. Магнийді анықтаудағы оның гравиметриялық түрі
A) MgNH4PO4.
B) Mg2P2O7.
C) Mg(PO3)2.
D) MgH PO4.
E) Жоқ.
113. Кристалл тұнба түзілетін жағдайда сынама өлшендісінің массасын есептейтін қатынас
A) M(A) · 0,5/ nM(A1).
B) mMA· 0,1/ nM(A)1.
C) nMA1· 0,5/ mM(A1).
D) nMA1· 0,1/ mM(A).
E) M(A1) / M(A)
114. Гравиметриялық анықтауда тұндырылған және гравиметриялық түрлері бірдей қосылыстар
A) CaCO3 , Fe2O3.
B) CaC2O4 , Al(OH)3.
C) Fe2O3 , CaC2O4.
D) Al(OH)3 , CaCO3.
E) BaSO4 , AgCl.
115. H3PO4 + 3KOH = K3PO4 + 3H2O реакциясындағы фосфор қышқылының эквиваленттік
факторы
A) 1.
B) 1/2.
C)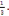
D) 3.
E) 5.
116. Na2CO3 + HCl = NaHCO3 + NaCl реакциясындағы натрий карбонатының эквивалентінің молярлық массасы (г/моль)
A) 106.
B)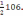
C)10,6.
D)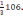
E)5,3.
117. Na2CO3 + 2HCl = Na2CO3 + 2NaCl реакциясындағы натрий карбонатының эквивалентінің молярлық массасы (г/моль)
A) 106.
B)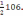
C) 10,6.
D)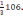
E) 5,3.
118. Көлемі 1 литр ерітіндідегі еріген заттың массасымен анықталатын концентрация (г/л)
A) Массалық концентрация.
B) Мольдік үлес.
C) Молярлық концентарция.
D) Эквиваленттің молярлық концентрациясы.
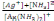 .
.73. Стандартты тотығу-тотықсыздану жұбының потенциалына сәйкес келетін жағдай
A) Т > 298 К.
B) Т < 293 К.
C) n > 1.
D) [Ox] = [Red] = 1.
E) [Red] < 1.
74. Әлсіз тотықсыздандырғыш қасиет көрсететін қосылыс және оған сәйкес жұп
A) (NH4)2S2O8 , φo (S2O82- / 2SO42-) = +2,01 В.
B) KIO4, φo (IO4-/I3-)=+1,28 B.
C) O20 , φo(O2/H2O2)=+0,69 B.
D) Br2o, φo(Br2/2Br-)=+1,09 B.
E) KMnO4, φo(MnO4-/Mn2+)=+1,51B.
75. [Fe3+] / [Fe2+] жұбы төмендегі қай қатынасқа тең болғанда редокс жұбының потенциалыстандарттан үлкен болады (φ°( (Fe3+/Fe2+) < φ°(Fe3+/Fe2+))
A) 1:10.
B) 1:1.
C) 10 : 1.
D) 5:2.
E) 5:5.
76. Ерітінді рН мәнінің өзгеруі потенциалына әсер етпейтін редокс жұбтары
A) J20 / 2J-, Fe3+ / Fe2+.
B) NO3- / NO, Cr2O72- / 2Cr3+.
C) Cr2O72- / 2Cr3+, Fe3+ / Fe2+.
D) NO3- / NO, J20 / 2J-.
E) SO32- / H2S, NO3- / NO.
77. Тотықтырғыш KMnO4 –тың күшті қышқылдық ортада тотықсыздану реакциясы және оған
сәйкес редокс потенциалы
A) MnO4- + 8H+ +5e → Mn2+ + 4H2O, φ0 = +1,51B.
B) MnO4- + 4H+ + 3e-→MnO20 + 2H2O, φ°=+1,69 B.
C) MnO4- + 2H+ + 3e- → MnO20 + 4OH-, φ° =+0,59 B.
D) MnO4- + 4OH- + e- → MnO42- + 2H2O + O20, φ° =+0,58 B.
E) MnO4- - e- → Mn0 + 2O20, φ°= +1,18 B.
78. Стандартты редокс потенциалдары φ°(BrO3-/Br-) = +1,42 B және φ°(Br20/2Br-) = +1,09B тең жүйедегі BrO3- + 5Br- + 6H+ → 3 Br20 + 3H2O реакциясы
*солдан оңға қарай жүреді
*оңнан солға қарай жүредi
*реакция жүруi мүмкiн емес
*реакция тепе-теңдiкте болады
*редокс потенциалы ешқандай мәлiмет бермейдi
79. Ерітіндідегі Ag+, Zn2+, Cu2+,Ni2+, Co2+ иондар қоспасына HCl ертіндісін қосқанда тұнбаға түсетін ион
A) Ag+.
B) Zn2+.
C) Cu2+.
D) Ni2+.
E) Co2+.
80. Ертіндідегі Al3+, Zn2+, Cr3+, Fe3+, Sn4+ иондар қоспасына NaOH ертіндісінің артық мөлшерін қосқанда тұнбаға түсетін катион
A) Al3+.
B) Zn2+.
C) Cr3+.
D) Fe3+.
E) Sn4+.
81. Қызыл қан тұзының ионы
A) [Fe(CN)6]3-.
B) [Fe(CN)6]4-.
C) [HgJ4]2-.
D) ClO3-.
E) NO2-.
82. Калий ионынмен микрокристаллоскопиялық реакция беретін реактив
A) Na3[Co(NO2) 6].
B) Na2Pb[Cu(NO2)6].
C) K2[HgJ4].
D) NaHC4H4O6.
E) CH3COOН.
83. IV,V,VI топ гидроксидтері ерітінділеріне концентрлі аммиак ерітіндісімен әсер еткенде ерітінідіге өтетін катиондар тобы
A) II.
B) VI.
C) IV.
D) V.
E) III.
84. Калий ионын Na3 [Co(NO2)6] реактивімен ашуда кедергі келтіретін реагент
A) H2O.
B) Na2SO4.
C) NH4Cl.
D) NaCl.
E) NaNO3.
85. Ca2+ ионын Ba2+ ионынан бөледі
A) Сірке қышқылының еритін тұздарымен.
B) Калий хроматымен.
C) Алдымен құмырсқа қышқылымен, кейін калий дихроматы.
D) Калий дихроматымен,рН = 5 ортада.
E) Құмырсқа қышқылы және калий хроматымен.
86. Жүйелік талдауда барий ионын калий дихроматымен K2Cr2O7 бөлетін және ашатын буферлік жүйе
A) Na2HPO4 + NH2PO4.
B) CH3COOH + CH3COONa.
C) HCOOH + HCOONa.
D) NH4OH + NH4Cl.
E) H2CO3 + NaHCO3.
87. Кобальт және никель сульфиттерін еріту үшін қолданатын реактив
A) H2SO4.
B) NaOH.
C) (NH4)2S.
D) HCl + H2O2.
E) H2O.
88. Мырыш, қалайы және кадмий тұздары ерітінділері қоспасына KOH ерітіндісінің артық мөлшерін қосқанда тұнбаға түседі
A) Zn(OH)2.
B) Sn(OH)2.
C) Барлық иондар тұнбаға бірге түседі.
D) Cd(OH)2.
E) Тұнбаға түспейді.
89. Барий, қорғасын және кальций тұздары ерітінділері қоспасына аммоний сульфаты ерітіндісінің артық мөлшерін қосқанда тұнбаға түседі
A) PbSO4, BaSO4, CaSO4.
B) BaSO4.
C) PbSO4, BaSO4.
D) BaSO4, CaSO4.
E) PbSO4.
90. Мышьяк (III) және сурьма (III) сульфидтерін еріту үшін қолданатын реактив
A) CH3COOH.
B) (NH4)2Sx.
C) (NH4)2CO3.
D) (NH4)2S.
E) H2S.
91. Ag2S тұнбасын ерітетін реактив
A) HCl.
B) Na2S.
C) NaOH.
D) KCN.
E) H2SO4.
92. Қорғасын мен барий сульфаттарын бөлу үшін қолданатын реагент
A) HCl.
B) NH4Cl.
C) CH3COONH4.
D) NH4OH.
E) NaOH.
93. Hg2(NO3)2 ерітіндісіне SnCl2 реагентін қосқанда түзілетін өнімдер
A) HgCl2+Sn0.
B) Hg0+SnCl4.
C) HgCl2+Sn(NO3)2.
D) Hg2Cl2
+Sn0.
E) Hg0+Sn0.
94. Al3+ ионымен ашық қызыл түсті қосылыс түзетін реактив
A) Ализарин .
B) Несслер реактиві.
C) Дитизон.
D) Тиомочевина.
E) Бензидин.
94. Алғашқы байқауда Fe (III) иондарын ашатын реактив
A) Na3[Co(NO2)6.
B) NH4OH.
C) Na2S2O3.
D) K4[Fe(CN)6].
E) K3[Fe(CN)6].
95. VI аналитикалық топтың катиондарымен негіздік тұз түзетін реактив
A) Na2SO4.
B) NH4OH(конц).
C) NaOH.
D) NaH2PO4.
E) H2S.
96. Жүйелік талдауда никель ионын ашатын реактив
A) Ильинский.
B) Чугаев.
C) Ринман.
D) Фишер.
E) Тенаров.
97. AI3+ ионының топ реагентімен әрекеттесуінен түзілетін қосылыс
A) AI(OH)3.
B) AI2O3.
C) NaAIO2.
D) HAIO2.
Е) КAIO2
98. Cr3+ ионының Н2О2 қатысында топ реагентімен әрекеттесуінен түзілетін қосылыс
A) Cr2O3.
B) (CrOH)3.
C) Na2CrO4.
D) NaCrO2.
E) Na2Cr2O7.
99. Топ реагентінің Co2+ ионымен әрекеттесуінен түзілетін қосылыс
A) [Cо(NH3)6]2+.
B) Co(OH)2.
C) CoO.
D) Co(OH)3.
E) CoSO4.
100. Hg22+ ионының топ реагентімен әрекеттесуінен түзілетін қосылыс
A) HgO.
B) Hg2(OH)2.
C) Hg(NO3)2.
D) Hg2CI2.
E) HgSO4.
101. Аммиакатты комплексті қосылыс түзетін катиондар
A) Na+, Ca2+, Zn2+.
B) K+, Ba2+, Zn2+.
C) Ag+, Cd2+, Cu2+.
D) Ca2+, K+, Cu2+.
E) Ba2+, Na+, Cd2+.
102. Массаны дәл өлшеуге негізделген талдау
A) Титриметрия.
B) Потенциометрия.
C) Гравиметрия.
D) Амперометрия.
E) Кулонометрия.
103. 2, 5324 г өлшенген массаның дәлдігі
A) 1.
B) 0,1.
C) 0,01.
D) 0,001.
C) 0,0001.
104. Аморфты тұнба түзілетін жағдайдағы гравиметриялық түрдің массасы (г) болу керек
A) 0,01.
B) 0,1.
C) 0,5.
D) 1,0.
E) 10,0.
105. Кристалды тұнба түзілетін жағдайдағы гравиметриялық түрдің массасы (г) болу керек
A) 0,01.
B) 0,1.
C) 0,5.
D) 1,0.
E) 10,0.
106. Темірді гравиметриялық анықтаудағы пайдаланылатын аналитикалық көбейткіштің F(Fe/Fe2O3)=
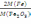 = 0,6994 алымындағы шама
= 0,6994 алымындағы шамаA) Анықтайтын заттың түр.
B) Тұндырушының түр.
C) Сынама формуласы.
D) Өлшенетін түрі.
E) Тұндырылған түрі.
107. Өлшеудегі ауытқу немесе қателік
A) Өлшенетін шаманың нақты мәнінен өлшеу нәтижесінің ауытқуы.
B) Абсолютті ауытқудың орташа мәнге қатынасы.
C) Өлшеу қателігі қайта өлшеу кезінде тұрақты болады немесе белгілі бір зандылықпен өзгереді.
D) Өлшеу қателігінің қайта өлшеу кезінде кездейсоқ өзгеруі.
E) Белгілі жағдайда байқалатын қателіктен артық болатын өрескел қате.
108. Аналитикалық таразыда өлшеу дәлдігі
A) 1,0 • 10-1г.
B) 1,0 • 10-5г.
C) 1,0 • 10-2г.
D) 1,0 • 10-4г.
E) 1,0 • 10-3г.
109. Тұнбаға түсіруші реагенттің қосылатын мөлшері артық болу керек
A) 5 есе.
B) 2 есе.
C) 6 есе.
D)1,5 есе.
E) 0,5 есе.
110. Мор тұзының құрамындағы темірді анықтауда тұнбаны қай ионнан жуады
A) SO42-.
B) NO3-.
C) OH-.
D) Cl-.
E) NH4+.
111. Барий хлоридінен барийді гравиметриялық анықтауда тұнбаны қай ионнан жуады
A) SO42-.
B) NO3-.
C) OH-.
D) Cl-.
E) NH4+.
112. Магнийді анықтаудағы оның гравиметриялық түрі
A) MgNH4PO4.
B) Mg2P2O7.
C) Mg(PO3)2.
D) MgH PO4.
E) Жоқ.
113. Кристалл тұнба түзілетін жағдайда сынама өлшендісінің массасын есептейтін қатынас
A) M(A) · 0,5/ nM(A1).
B) mMA· 0,1/ nM(A)1.
C) nMA1· 0,5/ mM(A1).
D) nMA1· 0,1/ mM(A).
E) M(A1) / M(A)
114. Гравиметриялық анықтауда тұндырылған және гравиметриялық түрлері бірдей қосылыстар
A) CaCO3 , Fe2O3.
B) CaC2O4 , Al(OH)3.
C) Fe2O3 , CaC2O4.
D) Al(OH)3 , CaCO3.
E) BaSO4 , AgCl.
115. H3PO4 + 3KOH = K3PO4 + 3H2O реакциясындағы фосфор қышқылының эквиваленттік
факторы
A) 1.
B) 1/2.
C)
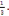
D) 3.
E) 5.
116. Na2CO3 + HCl = NaHCO3 + NaCl реакциясындағы натрий карбонатының эквивалентінің молярлық массасы (г/моль)
A) 106.
B)
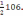
C)10,6.
D)
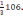
E)5,3.
117. Na2CO3 + 2HCl = Na2CO3 + 2NaCl реакциясындағы натрий карбонатының эквивалентінің молярлық массасы (г/моль)
A) 106.
B)
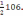
C) 10,6.
D)
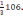
E) 5,3.
118. Көлемі 1 литр ерітіндідегі еріген заттың массасымен анықталатын концентрация (г/л)
A) Массалық концентрация.
B) Мольдік үлес.
C) Молярлық концентарция.
D) Эквиваленттің молярлық концентрациясы.