Файл: Методы получения аминокислот и их специфические особенности и различия.docx
Добавлен: 10.01.2024
Просмотров: 228
Скачиваний: 12
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «РОСТОВСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ
ФЕДЕРАЦИИ
ФАРМАЦЕВТИЧЕСКИЙ ФАКУЛЬТЕТ
кафедра УЭФ, фармацевтической технологии
Реферат по дисциплине:
«Биотехнология»
На тему:
«Методы получения аминокислот и их специфические особенности и различия»
Выполнила:
студентка 4 курса группы 2А
Грекова Анастасия Андреевна
Преподаватель:
Зав. кафедрой, д.ф.н.
Косякова Наталья Владимировна
г. Ростов-на-Дону
2023 г.
Содержание
Введение 3
Аминокислоты как продукт биотехнологии 4
Промышленные способы получения аминокислот 5
Микроорганизмы-продуценты аминокислот 8
Микробиологический метод получения лизина 10
Биотехнологический процесс производства триптофана 12
Биосинтез аргинина, глутамина, пролина и треонина 13
Заключение 16
Список источников 17
Введение
Биотехнология, по существу, сводится к использованию микроорганизмов, животных и растительных клеток или же их ферментов для синтеза, разрушения или трансформации (превращения) различных материалов с целью получения полезных продуктов для различных нужд человека.
Аминокислоты стали получать в промышленности примерно в середине 60-х годов XX века, после того как были изучены важнейшие этапы обмена веществ. Их производство составляет более 2 000 000 т/год, что оценивается в сумму более 4 млрд долларов США. Значительная часть предприятий, производящих аминокислоты, расположена в азиатском регионе. Лидирует производство L-глутамата натрия (более 1 500 000 т/год), за ним следуют производства L-лизина (700 000 т/год) и L-метионина (600 000 т/год). L-Аспарагиновая кислота и L-фенилаланин – сырье для получения подсластителя аспартама – производятся в количествах 10 000 т/год.
Около 65% производимых аминокислот используются в пищевой промышленности, 30% – как кормовые добавки для скота и лишь 5% аминокислот после дополнительной очистки применяют в медицинских целях, прежде всего для инфузионных растворов, а также в производстве косметических препаратов. Тенденция сегодняшнего дня – использование препаратов, содержащих весь комплекс аминокислот (или, по меньшей мере, 18 из них), т.е. в оптимальном для человеческого организма соотношении.
Аминокислоты как продукт биотехнологии
Аминокислоты – это органические соединения, содержащие одновременно щелочную аминную группу (NH2-) и кислотную карбоксильную (СООН-). Отсюда и их название: Амино-Кислоты.
Важным свойством аминокислот является их способность к поликонденсации и образованию полимеров в виде полиамидов, в том числе пептидов, белков, нейлона, капрона, энанта. Из определённого класса аминокислот (альфа-аминокислоты) собираются молекулы природных белков.
По объему производства среди соединений, производимых биотехнологическими способами, аминокислоты стоят на первом месте, а по стоимости – на втором, уступая в этом только антибиотикам.
Объем мирового производства аминокислот составляет более 500 тыс. т. в год. Из них 300 тыс. т. – глутамат натрия, 140 тыс. т. – метионин, 100 тыс. т. – лизин. Однако эти объемы – лишь небольшая часть требуемого.
По данным ВОЗ мировая потребность в наиболее востребованных аминокислотах составляет:
1. Лизин - 5 млн. т.
2. Метионин - 4 млн.т.
3. Треонин - 3,7 млн.т.
4. Триптофан - 2 млн. т.
Помимо применения в качестве пищевых добавок, биодобавок (БАДов), приправ и усилителей вкуса аминокислоты используются как сырье в химической, парфюмерной и фармацевтической промышленности и при производстве других веществ:
- глицин - как подсластитель, антиоксидант, бактеориостатик,
- аспарагиновая кислота – усилитель вкуса, сырье для синтеза аспартама (подсластителя),
- гистидин – противовоспалительное средство,
- глутаминовая кислота - усилитель вкуса, препарат для лечения психических заболеваний,
- метионин – пищевая и кормовая добавка,
- треонинин триптофан - пищевая и кормовая добавка,
- триптофан - пищевая и кормовая добавка,
- цистеин – фармацевтический препарат,
- фенилаланин – сырье для получения аспартама,
- лизин – пищевая и кормовая добавка, сырье для получения искусственных волокон и пленок.
Промышленные способы получения аминокислот
Производство аминокислот относится к одной из наиболее передовых областей биотехнологии. Аминокислоты получили широкое применение в парфюмерной и фармацевтической промышленности, в пищевой – в качестве усилителей вкуса (глицин добавляют как подсластитель, натриевая соль глутаминовой кислоты имеет мясной вкус), они используются как пищевые добавки для обогащения растительных белков (лизин, треонин, триптофан).
В настоящее время аминокислоты получают методами:
1) биологическим (применение гидролиза белоксодержащих субстратов);
2) химическим (тонкий органический синтез);
3) химико-энзиматическим (энзиматическая трансформация химически синтезированных предшественников аминокислот с образованием биологически активных L-изомеров);
4) микробиологическим (получение L-аминокислот).
Древнейший способ получения аминокислот — кислотный, щелочной или ферментативный гидролиз белоксодержащих субстратов (мясо, молоко и т.д.). При высокой температуре белок расщепляется на соответствующие аминокислоты или фрагменты, состоящие из нескольких аминокислот. При этом образуется смесь аминокислот и пептидов. Извлечение из этой смеси какой-либо определенной аминокислоты — довольно сложная, но, тем не менее выполнимая задача. Само по себе сырье (мясо и белок молока — казеин) — дорогостоящий продукт, и этот метод применяется, когда имеют дело с «бросовым» сырьем, т.е. с отходами производства (таким сырьем являются рога, копыта, волосы, перья и пух, состоящие из кератина, в котором содержится очень много серосодержащей кислоты цистеина, и – в небольших количествах — других аминокислот).
При гидролизе отходы пищевой и молочной промышленности нагревают с растворами кислот или щелочей при 100-105 С в течение 20-48 час. Чаще всего используют 20% р-р соляной к-ты, обеспечивающий глубокий гидролиз белка. Лучшим способом уменьшения потерь белка при гидролизе является проведение его в вакууме или в атмосфере инертного газа, а также соблюдение высокого соотношения количества к-ты, взятой для гидролиза и массы белка (200:1). Раньше методом гидролиза получали аминокислоты исключительно для фармацевтических и научных целей. Сейчас сфера использования белковых гидролизатов существенно расширилась. Их применяют в медицине, животноводстве, пищевой и микробиологической промышленности.
Следующий способ получения чистых аминокислот – химический синтез. Их синтезируют подобно другим органическим кислотам, это не сложно. Однако в процессе химического синтеза получается смесь D- и L- стереоизомеров (иногда получается и большее количество изомеров), а как известно, в белках человека биологически активны только L-стереоизомеры аминокислот, поэтому существуют трудности разделения этих изомеров. Кроме того, химическое производство аминокислот, как правило, связано с использованием дорогостоящего оборудования и нередко агрессивных токсических соединений в качестве исходного сырья. Процесс протекает при высокой температуре, требует дорогостоящих катализаторов и как всякое химическое производство сопровождается образованием побочных продуктов, загрязняет окружающую среду, небезопасно и небезвредно для обслуживающего персонала.
Тем не менее, некоторые аминокислоты получают химическим синтезом, например глицин, а также D-, L-метионин, D-изомер которого малотоксичен, поэтому медицинский препарат на основе метионина содержит D- и L-формы. Хотя за рубежом в медицине используется препарат, содержащий только L-форму метионина, где рацемическую смесь метионина разделяют биоконверсией D-формы в L-форму под влиянием специальных ферментов живых клеток микроорганизмов.
Следующий способ получения аминокислот — химико-энзиматический. Как видно из названия, этот метод получения аминокислот предполагает два этапа. Сначала химическим методом синтезируется «предшественник» — соответствующая карбоновая кислота, а затем эта карбоновая кислота (обычно в присутствии аммиака) превращается в соответствующую аминокислоту. Эта биотрансформация (биоконверсия) осуществляется ферментами живых клеток. Причем полученные L-стереоизомеры аминокислот сами по себе необходимы для жизнедеятельности этих клеток, т.е. фактически этот способ наполовину биотехнологический. Таким методом получают, например, аспарагиновую кислоту (на основе фумаровой кислоты). Раствор фумаровой кислоты пропускают через колонки, в которых иммобилизованы или ферменты, или клетки микроорганизмов с высокой активностью аспартазы, например, Escherichia coli или Serratia marcesceus; туда же подается аммиак и осуществляется биотрансформация.
Химико-энзиматически можно производить практически все аминокислоты, однако из-за дороговизны и сложности получения соответствующих органических кислот-предшественников этот метод не всегда экономически выгоден и в большинстве случаев уступает методу прямого микробиологического синтеза.
Четвертый способ получения аминокислот — их прямой микробиологический синтез — целиком основан на использовании биообъектов (т.е. является полностью биотехнологическим). В качестве биообъектов в нем применяются штаммы-продуценты аминокислот. Этим методом аминокислоты чаще всего получают на основе Escherichia coli (кишечная палочка — симбионт человека), Bacillus subtilis (сенная палочка — почвенный микроорганизм) и Corynebacterium glutamicum (почвенный микроорганизм).
Микроорганизмы-продуценты аминокислот
Для получения аминокислот, органических кислот, ферментов, биологически активных веществ биотехологическими способами используют ауксотрофные мутанты, т.е. штаммы, приобретшие способность к сверхсинтезу нужных нам веществ. Это происходит за счет потери способности синтезировать другие необходимые соединения, которые приходится добавлять в питательную среду.
Бактерии для производства аминокислот стали использовать с начала 50-х годов ХХ века. Их штаммы улучшали генетическими методами, выделяя ауксотрофные мутанты и мутанты с измененными регуляторными свойствами. В основе большинства производственных процессов при получении аминокислот лежит регулирование условий среды (изменение концентрации субстрата, рН, ионов металлов, органических добавок), что приводит к синтезу избыточных количеств необходимого продукта.
Микроорганизмы-продуценты аминокислот на сегодняшний день прекрасно изучены. Для кишечной палочки разработаны многообразные способы генетического обмена, позволяющие легко комбинировать разные гены и изменять процесс метаболизма. В меньшей степени это относится к Bacillus subtilis, и еще в меньшей степени к Corynebacterium glutamicum.
Использование этих микроорганизмов для получения аминокислот основано на их способности самостоятельно синтезировать все 20 аминокислот. Также они являются гетеротрофными бактериями, которые в качестве источника углерода используют органические соединения (углевод или какую-нибудь органическую кислоту), а все остальные компоненты получают из неорганических соединений.
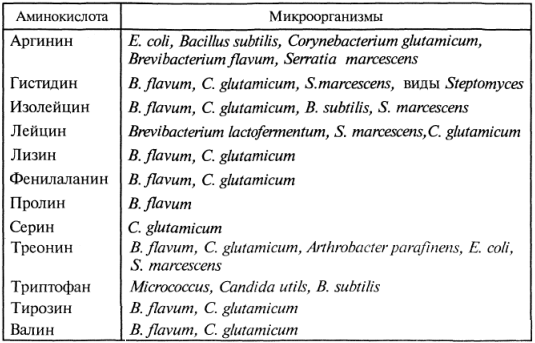
Рисунок 1 – Микроорганизмы-продуценты аминокислот (по Н. Б. Градовой и О. А. Решетник, 1987)
Применение микроорганизмов гетеротрофов позволяет существенно сократить по времени процесс ферментации. Так, кишечная палочка в богатой питательной среде делится каждые 20-30 мин, коринебактерии – каждый час. В бедных средах – время регенерации в два раза больше (1 ч для кишечной палочки, 1,5-2 ч для коринебактерии и сенной палочки). Вместе с тем существуют бактерии, так называемые ауксотрофные мутанты — микроорганизмы, которые, с одной стороны, утратили способность самостоятельно синтезировать необходимые для построения всех компонентов своей клетки разные аминокислоты, а с другой – приобрели способность к сверхсинтезу целевой аминокислоты. Такие мутанты получают либо воздействием различных мутагенов физической и химической природы на исходную культуру микроорганизма с последующей селекцией штамма по заранее заданным признакам