Добавлен: 24.10.2023
Просмотров: 389
Скачиваний: 35
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ
«БАШКИРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
(ФГБОУ ВО БГМУ МИНЗДРАВА РОССИИ)
РЕФЕРАТ
на тему: «Амины»
Выполнил: Нгуен Хоанг Лонг
группа 11Ф
специальность: Фармация
Проверил: Мельников А.С.
(Вузовский руководитель практики (ФИО, кафедра)
______________________________________________
______________________________________________
Оценка «___________»__________________________
(цифрой, прописью) (подпись вузовского руководителя практики)
Уфа 2023г
СОДЕРЖАНИЕ
-
Введение -
Амины -
Заключение
-
Введение
Амины - производные аммиака, в молекуле которого атомы водорода замещены на углеводородные радикалы алифатического (R) или ароматического ряда (Ar).
В зависимости от числа углеводородных радикалов, связанных с атомом азота, различают первичные (-NH2), вторичные(-NH-) и третичные амины ( >N-).

Алифатические амины: R-NH2, R1-NH-R2, R1-N(R)2.
Ароматические амины: Ar-NH2, Ar-NH-Ar, (Ar)3 N.
Жирноароматические амины: Ar-NH- R.
Номенклатура. Названия аминов образуются из названий углеводородных радикалов и слова амин:
CH3-NH2 CH3-NH-CH3 CH3-CH2-CH(NH2)-CH2-CH2-CH3
метиламин диметиламин 3-гексиламин (3-аминогексан)
Для некоторых ароматических аминов сохраняются тривиальные названия:
анилин п-толуидин бензиламин N-метиланилин
-
Амины
Изомерия. Для аминов характерна, в основном, структурная изомерия. Для алифатических аминов:
а) изомерия углеродного скелета (на примере С3Н9N)
пропиламин изопропиламин
б) метамерия
триметиламин
Для ароматических аминов - различное расположение радикалов и аминогруппы в бензольном кольце. Например,
п-метиланилин N-метиланилин бензиламин
п-толуидин
Нахождение в природе. Природные амины животного происхождения: адреналин, норадреналин, серотонин, гистамин, тирамин - участвуют в регуляции центральной нервной, пищеварительной, эндокринной, сердечно-сосудистой и других систем.
Амины растительного происхождения - алкалоиды, характеризующиеся высокой физиологической активностью.
Получение.
1. Алкилирование аммиака и аминов (реакция Гофмана). Алкилирующие агенты: галогенопроизводные углеводородов, спирты.

2. Восстановление азотсодержащих органических соединений.
Нитросоединения, оксимы, нитрилыв присутствии катализаторовмогут быть восстановлены до аминов.
R-NO2 + [H] → R-NH2
3. Для получения алкиламинов разработано множество специальных методов, например расщепление амидов карбоновых кислот галогенами в щелочной среде (перегруппировка Гофмана):

4. Восстановление ароматических нитросоединений (реакция Зинина):
Строение. Атом азота в алкиламинах находится в sр3-гибридизации, ковалентная Ϭ-С-N-связь образована перекрыванием sр3 (С) – sр3 ( N) - орбиталей, дипольный момент этой связи отличен от нуля. Аминогруппа в алкиламинах обладает электроноакцепторным характером по отношению к углеводородному радикалу (-I- эффект): Rδ+ → NН2 δ-. Алкиламины образуют межмолекулярные водородные связи:

.
Пространственная форма аминов представляет собой искаженный тетраэдр.
В ароматических аминах атом азота находится в состоянии sр
2- гибридизации, неподеленная электронная пара азота участвует в р,π - сопряжении с бензольным кольцом
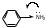 (-I,+М).
(-I,+М). Таким образом, аминогруппа в ароматических аминах проявляет электронодонорные свойства, в результате этого электронная плотность на атоме азота понижается, в орто- и пара- положениях кольца электронная плотность увеличивается.
Физические свойства аминов. Ассоциация молекул первичных и вторичных алкиламинов обусловливает более высокие температуры кипения и плавления по сравнению с близкими по массе углеводородами. Однако по сравнению со спиртами амины имеют более низкие значения температур плавления и кипения, что связано с образованием аминами менее прочных водородных связей. Низкомолекулярные амины смешиваются с водой в любых соотношениях благодаря образованию водородных связей. Ароматические амины - это жидкие или твердые вещества с характерными запахами, плохо растворимые в воде. Химические свойства. Химическое поведение аминов определяется главным образом присутствием неподеленной электронной пары у атома азота.
а) Основные и кислотные свойства. Основные свойства аминов обусловлены наличием неподеленной электронной пары у атома азота аминогруппы и зависят от природы и числа радикалов в их составе. Увеличиваются основные свойства в следующем направлении:
ароматические амины < аммиак < алифатические амины.
Уменьшение основности ароматических аминов по сравнению с алифатическими (почти в миллион раз) связано со значительной делокализацией неподеленной электронной парой атома азота. При этом электронодонорные заместители кольца увеличивают основные свойства, электроноакцепторные - уменьшают. Так, пара-метиланилин более сильное основание по сравнению с пара-нитроанилином:

Амины как основания легко присоединяют протон с образованием солей:
СН3NH2 + HCl → СН3NH3+ Cl -..
метиламин хлорид метиламмония
анилин хлорид фениламмония
Аммонийные соли неустойчивы, особенно в ароматическом ряду, и способны разлагаться в присутствии щелочей:
СН3NH3+ Cl - + NаОН → СН3NH2 + NаCl.
Водные растворы алифатических аминов имеют щелочную реакцию:
СН3NH2 + HОН → СН3NH3 ОН ↔ СН3NH3+ + ОН-
гидроксид метиламмония
Первичные и вторичные алифатические амины являются слабыми N-H кислотами (рКа=33-35). При взаимодействии с активными металлами образуют соли﴾амиды﴿:
RNH2 + Na → RNH- Na+ + 1/2 H2
б) Нуклеофильные свойства. Нуклеофильные свойства амины проявляют в реакциях нуклеофильного замещения (SN) и нуклеофильного присоединения (АN).
1. Нуклеофильное замещение (SN):
Алкилирование аминов
Амины алкилируются спиртами, галогенпроизводными углеводородов:
С2Н5 ОН + СН3NН2 → С2Н5-NН-СН3 + НОН
Ацилирование аминов
Амины ацилируются карбоновыми кислотами и их производными с образованием амидов карбоновых кислот:

В результате сопряжения неподеленной электронной пары атома азота с карбонильной группой (р,π-сопряжение) основные и нуклеофильные свойства аминогруппы в амидах слабо выражены.
2. Нуклеофильное присоединение (АN):
в) Взаимодействие аминов с азотистой кислотой
Первичные, вторичные и третичные амины по-разному взаимодействуют с азотистой кислотой. Эта реакция может служить качественной реакцией для определения строения аминов. Неустойчивую азотистую кислоту генерируют действием сильной кислоты на нитриты.
Первичные алифатические амины реагируют с азотистой кислотой с выделением газообразного азота и образованием молекулы спирта:
Первичные ароматические амины при взаимодействии с азотистой кислотой образуют соли диазония (диазотирование):
Особенности реакции диазотирования: 1) температура реакционной среды 00 - +50; 2) реакция идет в кислой среде; 3) реагентом служит смесь нитритов натрия или калия и минеральной кислоты.
Соли диазония широко используют в органическом синтезе для получения различных классов ароматических соединений и азокрасителей, при этом превращения солей диазония могут протекать с выделением или без выделения азота.
Вторичные алифатические и ароматические амины образуют с азотистой кислотой N-нитрозоамины – жидкие или твердые вещества желтого цвета:
R2NH + NaNO2 + HCl → R2N-N=O + NaCl + H2O
амин нитрозоамин
Третичные алифатические амины при обычной температуре с азотистой кислотой не взаимодействуют, ароматические амины образуют пара-нитрозопроизводные:
г) Электрофильное замещение в ароматических аминах
В ароматических аминах аминогруппа как заместитель 1 рода значительно облегчает электрофильную атаку ароматического кольца и направляет входящие группы в орто- и пара-положения.
Галогенирование. Бромирование и хлорирование ароматических аминов протекает очень легко. В случае анилина образуются тригалогенамины:

Сульфирование. Действием концентрированной серной кислотой на ароматические амины получают соли - гидросульфаты, которые при нагревании образуют сульфопроизводные ароматических аминов:
В случае анилина образуется сульфаниловая кислота, имеющая биполярную структуру. Огромный практический интерес представляют амиды этой кислоты (сульфаниламиды), многие из которых являются эффективными лекарственными препаратами (красный и белый стрептоцид, сульфадиметоксин, фталазол и другие).
Нитрование. Реакции нитрования проводят с предварительной защитой аминогруппы (например, ацилирование уксусным ангидридом), в противном случае происходит её окисление. После проведения реакции ацильную защиту снимают кислотным или щелочным гидролизом:

Алкилирование и ацилирование. Амины способны вступать в реакции алкилирования и ацилирования путем замещения атома водорода в аминогруппе на алкильный или ацильный остаток (см. «Получение аминов. Защита аминогруппы»).
Окисление. Характер окисления аминов зависит от природы радикала и аминогруппы, окислителя. Легко окисляются ароматические амины (особенно первичные), при этом образуется смесь продуктов, в том числе нитросоединения. Первичные алифатические амины могут быть окислены до нитросоединений. Горение алифатических аминов сопровождается образованием углекислого газа, азота, воды: