Файл: Рассчитать величину давления в системе, если при протекании процесса изменение внутренней энергии .docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 24.10.2023
Просмотров: 1192
Скачиваний: 12
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
273 °С
 0 °С
0 °С
Отзыв
Правильный ответ: 0 °С, 273 К
Вопрос 5
Нет ответа
Текст вопроса
Рассчитать величину стандартного химического потенциала μ0 идеального газа при температуре 0 °С и давлении р = 2,7 атм, если величина химического потенциала газа μ = 27,3 кДж/моль. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 2,27 кДж/моль
2,27 кДж/моль
 0,227 кДж/моль
0,227 кДж/моль
 22,7 кДж/моль
22,7 кДж/моль
 227 кДж/моль
227 кДж/моль
Отзыв
Правильный ответ: 22,7 кДж/моль
Вопрос 6
Нет ответа
Текст вопроса
Рассчитать величину температуры идеального газа, если при изменении химического потенциала Δμ = 2,5 Дж/моль давление изменяется от 1 атм до 3 атм. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один или несколько ответов:
 273 К
273 К
 0 °С
0 °С
 0 К
0 К
 273 °С
273 °С
Отзыв
Правильный ответ: 0 °С, 273 К
Вопрос 7
Нет ответа
Текст вопроса
Рассчитать температуру протекания реакции, если изменение внутренней энергии ΔU реакции = 61,9 кДж/моль, а величина температурного коэффициента константы равновесия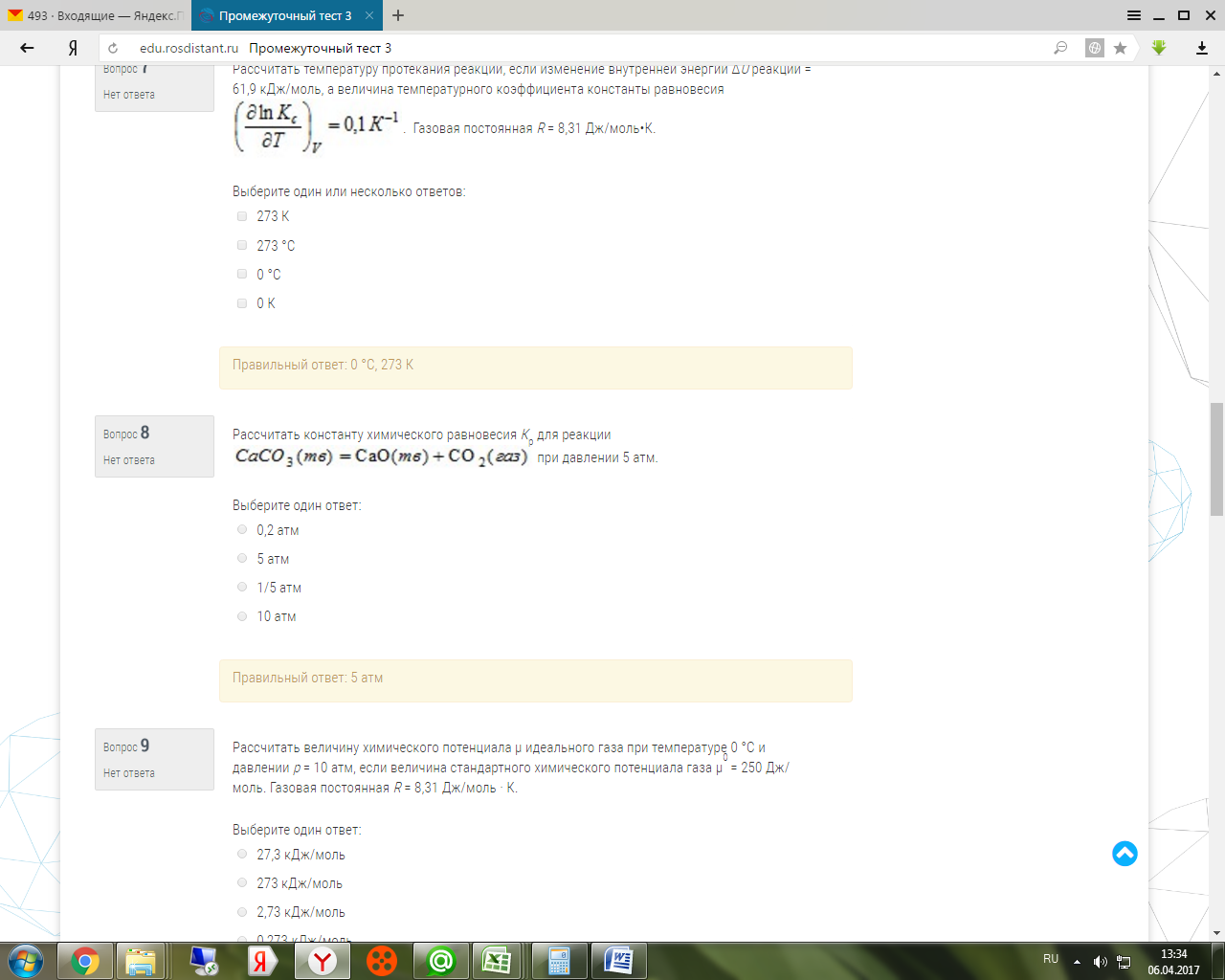 . Газовая постоянная R = 8,31 Дж/моль•К.
. Газовая постоянная R = 8,31 Дж/моль•К.
Выберите один или несколько ответов:
 273 К
273 К
 273 °С
273 °С
 0 °С
0 °С
 0 К
0 К
Отзыв
Правильный ответ: 0 °С, 273 К
Вопрос 8
Нет ответа
Текст вопроса
Рассчитать константу химического равновесия Кр для реакции при давлении 5 атм.
при давлении 5 атм.
Выберите один ответ:
 0,2 атм
0,2 атм
 5 атм
5 атм
 1/5 атм
1/5 атм
 10 атм
10 атм
Отзыв
Правильный ответ: 5 атм
Вопрос 9
Нет ответа
Текст вопроса
Рассчитать величину химического потенциала μ идеального газа при температуре 0 °С и давлении р = 10 атм, если величина стандартного химического потенциала газа μ0 = 250 Дж/моль. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 27,3 кДж/моль
27,3 кДж/моль
 273 кДж/моль
273 кДж/моль
 2,73 кДж/моль
2,73 кДж/моль
 0,273 кДж/моль
0,273 кДж/моль
Отзыв
Правильный ответ: 27,3 кДж/моль
Вопрос 10
Нет ответа
Текст вопроса
Рассчитать величину изменения энергии Гиббса ΔG реакции 2Н = Н2 при температуре 0 °С, если константа скорости реакции Кр = 0,5 атм-1, парциальное давление атомарного водорода р = 1 атм и парциальное давление молекулярного водородар = 2,73 атм. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 11,35 кДж/моль
11,35 кДж/моль
 1135 кДж/моль
1135 кДж/моль
 1,135 кДж/моль
1,135 кДж/моль
 113,5 кДж/моль
113,5 кДж/моль
Отзыв
Правильный ответ: 11,35 кДж/моль
Вопрос 11
Нет ответа
Текст вопроса
Рассчитать изменение энтальпии ΔН реакции при температуре 0 °С, если температурный коэффициент константы равновесия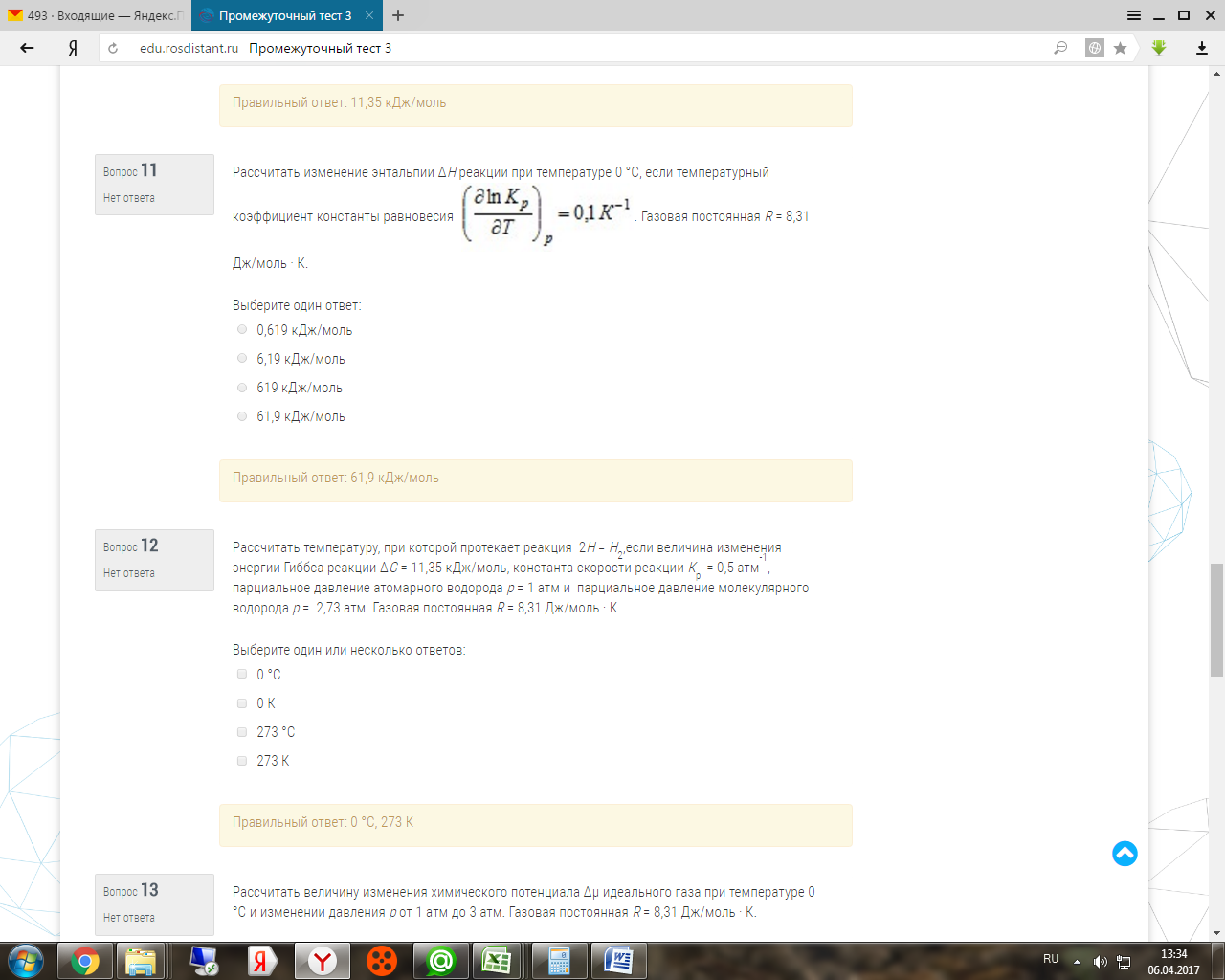 . Газовая постоянная R = 8,31 Дж/моль · К.
. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 0,619 кДж/моль
0,619 кДж/моль
 6,19 кДж/моль
6,19 кДж/моль
 619 кДж/моль
619 кДж/моль
 61,9 кДж/моль
61,9 кДж/моль
Отзыв
Правильный ответ: 61,9 кДж/моль
Вопрос 12
Нет ответа
Текст вопроса
Рассчитать температуру, при которой протекает реакция 2Н = Н2,если величина изменения энергии Гиббса реакции ΔG = 11,35 кДж/моль, константа скорости реакции Кр = 0,5 атм-1, парциальное давление атомарного водорода р = 1 атм и парциальное давление молекулярного водорода р = 2,73 атм. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один или несколько ответов:
 0 °С
0 °С
 0 К
0 К
 273 °С
273 °С
 273 К
273 К
Отзыв
Правильный ответ: 0 °С, 273 К
Вопрос 13
Нет ответа
Текст вопроса
Рассчитать величину изменения химического потенциала Δμ идеального газа при температуре 0 °С и изменении давления р от 1 атм до 3 атм. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 2,5 кДж/моль
2,5 кДж/моль
 250 кДж/моль
250 кДж/моль
 0,25 кДж/моль
0,25 кДж/моль
 25 кДж/моль
25 кДж/моль
Отзыв
Правильный ответ: 2,5 кДж/моль
Вопрос 14
Нет ответа
Текст вопроса
Рассчитать температуру, при которой протекает реакция В + D = BD, если величина изменения энергии Гельмгольца реакции ΔА = 11,35 кДж/моль, константа скорости реакции Кс = 0,5 л/моль, концентрация веществ B и D одинаковы и составляют с = 1 моль/л, а концентрация вещества BD составляет с = 2,73 моль/л.
Выберите один или несколько ответов:
 0 К
0 К
 273 °С
273 °С
 0 °С
0 °С
 273 К
273 К
Отзыв
Правильный ответ: 0 °С, 273 К
Вопрос 15
Нет ответа
Текст вопроса
Рассчитать изменение внутренней энергии ΔU реакции при температуре 0 °С, если температурный коэффициент константы равновесия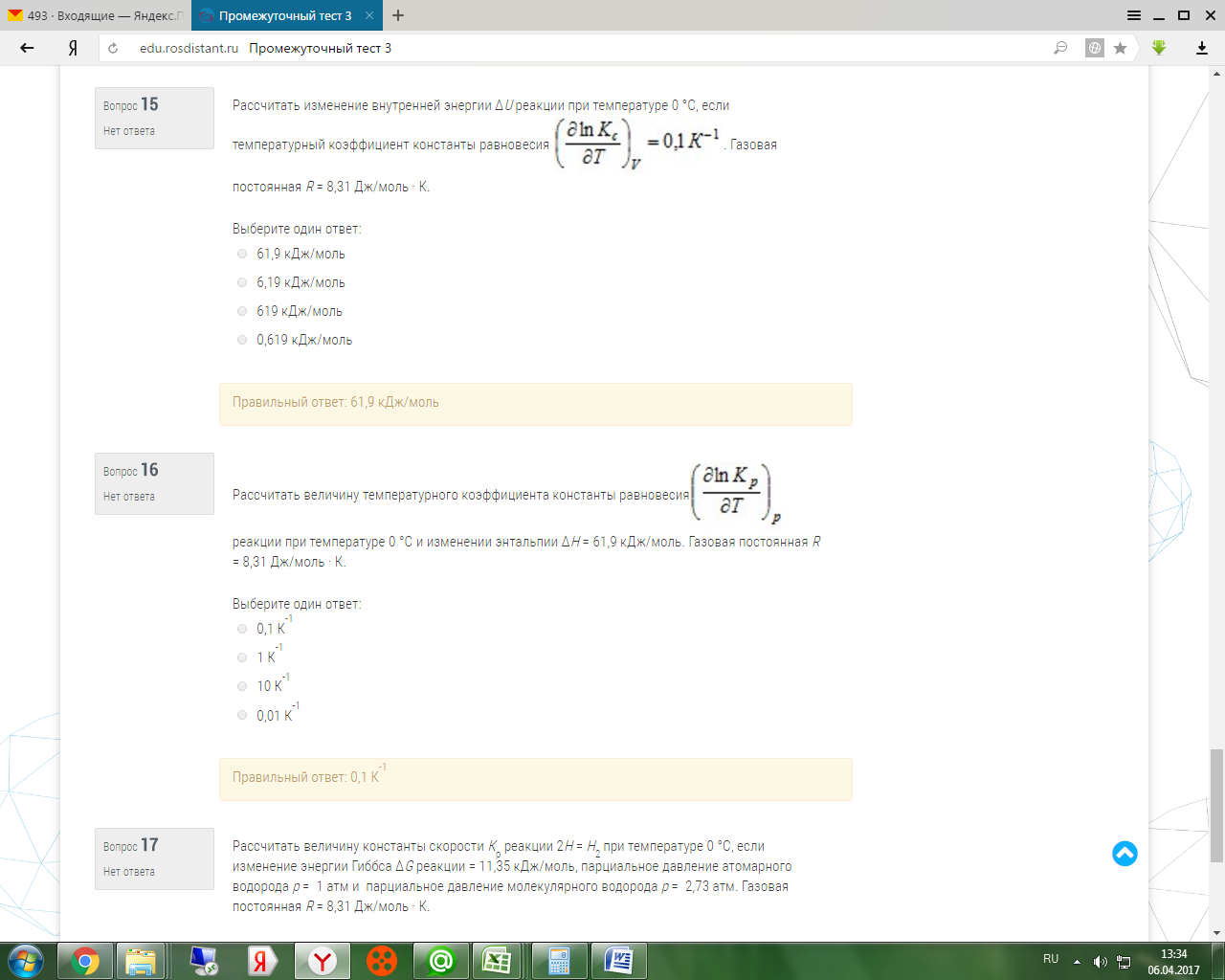
. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 61,9 кДж/моль
61,9 кДж/моль
 6,19 кДж/моль
6,19 кДж/моль
 619 кДж/моль
619 кДж/моль
 0,619 кДж/моль
0,619 кДж/моль
Отзыв
Правильный ответ: 61,9 кДж/моль
Вопрос 16
Нет ответа
Текст вопроса
Рассчитать величину температурного коэффициента константы равновесия реакции при температуре 0 °С и изменении энтальпии ΔН = 61,9 кДж/моль. Газовая постоянная R = 8,31 Дж/моль · К.
реакции при температуре 0 °С и изменении энтальпии ΔН = 61,9 кДж/моль. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 0,1 К-1
0,1 К-1
 1 К-1
1 К-1
 10 К-1
10 К-1
 0,01 К-1
0,01 К-1
Отзыв
Правильный ответ: 0,1 К-1
Вопрос
17
Нет ответа
Текст вопроса
Рассчитать величину константы скорости Кр реакции 2Н = Н2 при температуре 0 °С, если изменение энергии Гиббса ΔG реакции = 11,35 кДж/моль, парциальное давление атомарного водорода р = 1 атм и парциальное давление молекулярного водорода р = 2,73 атм. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 5 атм-1
5 атм-1
 0,05 атм-1
0,05 атм-1
 50 атм-1
50 атм-1
 0,5 атм-1
0,5 атм-1
Отзыв
Правильный ответ: 0,5 атм-1
Промежуточный тест 4
Начало формы
Рассчитать изменение объема V (м3) при фазовом переходе, если тепловой эффект фазового перехода ΔН = 5,46 кДж/моль, температураt = 0 °С, а величина dp/dT = 10 Па/К.
Выберите один ответ:
 1
1
 3
3
 2
2
 4
4
Отзыв
Правильный ответ: 2
Вопрос 2
Нет ответа
Текст вопроса
Рассчитать температуру фазового перехода, если при фазовом переходе объем системы увеличивается от 1 м2 до 3 м2, величина теплового эффекта фазового перехода ΔН = 5,46 кДж/моль, а величина dp/dT = 10 Па/К.
Выберите один или несколько ответов:
 0 °С
0 °С
 273 °С
273 °С
 273 К
273 К
 0 К
0 К
Отзыв
Правильный ответ: 0 °С, 273 К
Вопрос 3
Нет ответа
Текст вопроса
Рассчитать тепловой эффект фазового перехода ΔН (кДж/моль) при температуре 0 °С, если при фазовом переходе объем системы V увеличивается от 1 м2 до 3 м2, а величина dp/dT = 10 Па/К.
Выберите один ответ:
 54,6
54,6

 0 °С
0 °СОтзыв
Правильный ответ: 0 °С, 273 К
Вопрос 5
Нет ответа
Текст вопроса
Рассчитать величину стандартного химического потенциала μ0 идеального газа при температуре 0 °С и давлении р = 2,7 атм, если величина химического потенциала газа μ = 27,3 кДж/моль. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 2,27 кДж/моль
2,27 кДж/моль 0,227 кДж/моль
0,227 кДж/моль 22,7 кДж/моль
22,7 кДж/моль 227 кДж/моль
227 кДж/мольОтзыв
Правильный ответ: 22,7 кДж/моль
Вопрос 6
Нет ответа
Текст вопроса
Рассчитать величину температуры идеального газа, если при изменении химического потенциала Δμ = 2,5 Дж/моль давление изменяется от 1 атм до 3 атм. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один или несколько ответов:
 273 К
273 К 0 °С
0 °С 0 К
0 К 273 °С
273 °СОтзыв
Правильный ответ: 0 °С, 273 К
Вопрос 7
Нет ответа
Текст вопроса
Рассчитать температуру протекания реакции, если изменение внутренней энергии ΔU реакции = 61,9 кДж/моль, а величина температурного коэффициента константы равновесия
Выберите один или несколько ответов:
 273 К
273 К 273 °С
273 °С 0 °С
0 °С 0 К
0 КОтзыв
Правильный ответ: 0 °С, 273 К
Вопрос 8
Нет ответа
Текст вопроса
Рассчитать константу химического равновесия Кр для реакции
Выберите один ответ:
 0,2 атм
0,2 атм 5 атм
5 атм 1/5 атм
1/5 атм 10 атм
10 атмОтзыв
Правильный ответ: 5 атм
Вопрос 9
Нет ответа
Текст вопроса
Рассчитать величину химического потенциала μ идеального газа при температуре 0 °С и давлении р = 10 атм, если величина стандартного химического потенциала газа μ0 = 250 Дж/моль. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 27,3 кДж/моль
27,3 кДж/моль 273 кДж/моль
273 кДж/моль 2,73 кДж/моль
2,73 кДж/моль 0,273 кДж/моль
0,273 кДж/мольОтзыв
Правильный ответ: 27,3 кДж/моль
Вопрос 10
Нет ответа
Текст вопроса
Рассчитать величину изменения энергии Гиббса ΔG реакции 2Н = Н2 при температуре 0 °С, если константа скорости реакции Кр = 0,5 атм-1, парциальное давление атомарного водорода р = 1 атм и парциальное давление молекулярного водородар = 2,73 атм. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 11,35 кДж/моль
11,35 кДж/моль 1135 кДж/моль
1135 кДж/моль 1,135 кДж/моль
1,135 кДж/моль 113,5 кДж/моль
113,5 кДж/мольОтзыв
Правильный ответ: 11,35 кДж/моль
Вопрос 11
Нет ответа
Текст вопроса
Рассчитать изменение энтальпии ΔН реакции при температуре 0 °С, если температурный коэффициент константы равновесия
Выберите один ответ:
 0,619 кДж/моль
0,619 кДж/моль 6,19 кДж/моль
6,19 кДж/моль 619 кДж/моль
619 кДж/моль 61,9 кДж/моль
61,9 кДж/мольОтзыв
Правильный ответ: 61,9 кДж/моль
Вопрос 12
Нет ответа
Текст вопроса
Рассчитать температуру, при которой протекает реакция 2Н = Н2,если величина изменения энергии Гиббса реакции ΔG = 11,35 кДж/моль, константа скорости реакции Кр = 0,5 атм-1, парциальное давление атомарного водорода р = 1 атм и парциальное давление молекулярного водорода р = 2,73 атм. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один или несколько ответов:
 0 °С
0 °С 0 К
0 К 273 °С
273 °С 273 К
273 КОтзыв
Правильный ответ: 0 °С, 273 К
Вопрос 13
Нет ответа
Текст вопроса
Рассчитать величину изменения химического потенциала Δμ идеального газа при температуре 0 °С и изменении давления р от 1 атм до 3 атм. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 2,5 кДж/моль
2,5 кДж/моль 250 кДж/моль
250 кДж/моль 0,25 кДж/моль
0,25 кДж/моль 25 кДж/моль
25 кДж/мольОтзыв
Правильный ответ: 2,5 кДж/моль
Вопрос 14
Нет ответа
Текст вопроса
Рассчитать температуру, при которой протекает реакция В + D = BD, если величина изменения энергии Гельмгольца реакции ΔА = 11,35 кДж/моль, константа скорости реакции Кс = 0,5 л/моль, концентрация веществ B и D одинаковы и составляют с = 1 моль/л, а концентрация вещества BD составляет с = 2,73 моль/л.
Выберите один или несколько ответов:
 0 К
0 К 273 °С
273 °С 0 °С
0 °С 273 К
273 КОтзыв
Правильный ответ: 0 °С, 273 К
Вопрос 15
Нет ответа
Текст вопроса
Рассчитать изменение внутренней энергии ΔU реакции при температуре 0 °С, если температурный коэффициент константы равновесия
. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 61,9 кДж/моль
61,9 кДж/моль 6,19 кДж/моль
6,19 кДж/моль 619 кДж/моль
619 кДж/моль 0,619 кДж/моль
0,619 кДж/мольОтзыв
Правильный ответ: 61,9 кДж/моль
Вопрос 16
Нет ответа
Текст вопроса
Рассчитать величину температурного коэффициента константы равновесия
Выберите один ответ:
 0,1 К-1
0,1 К-1 1 К-1
1 К-1 10 К-1
10 К-1 0,01 К-1
0,01 К-1Отзыв
Правильный ответ: 0,1 К-1
Вопрос
17
Нет ответа
Текст вопроса
Рассчитать величину константы скорости Кр реакции 2Н = Н2 при температуре 0 °С, если изменение энергии Гиббса ΔG реакции = 11,35 кДж/моль, парциальное давление атомарного водорода р = 1 атм и парциальное давление молекулярного водорода р = 2,73 атм. Газовая постоянная R = 8,31 Дж/моль · К.
Выберите один ответ:
 5 атм-1
5 атм-1 0,05 атм-1
0,05 атм-1 50 атм-1
50 атм-1 0,5 атм-1
0,5 атм-1Отзыв
Правильный ответ: 0,5 атм-1
Промежуточный тест 4
Начало формы
Рассчитать изменение объема V (м3) при фазовом переходе, если тепловой эффект фазового перехода ΔН = 5,46 кДж/моль, температураt = 0 °С, а величина dp/dT = 10 Па/К.
Выберите один ответ:
 1
1 3
3 2
2 4
4Отзыв
Правильный ответ: 2
Вопрос 2
Нет ответа
Текст вопроса
Рассчитать температуру фазового перехода, если при фазовом переходе объем системы увеличивается от 1 м2 до 3 м2, величина теплового эффекта фазового перехода ΔН = 5,46 кДж/моль, а величина dp/dT = 10 Па/К.
Выберите один или несколько ответов:
 0 °С
0 °С 273 °С
273 °С 273 К
273 К 0 К
0 КОтзыв
Правильный ответ: 0 °С, 273 К
Вопрос 3
Нет ответа
Текст вопроса
Рассчитать тепловой эффект фазового перехода ΔН (кДж/моль) при температуре 0 °С, если при фазовом переходе объем системы V увеличивается от 1 м2 до 3 м2, а величина dp/dT = 10 Па/К.
Выберите один ответ:
 54,6
54,6