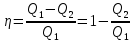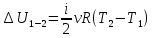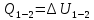Файл: Решение Поскольку процесс 12 изотермический, то т 2 т поскольку процесс 23 изохорный, то V.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 25.10.2023
Просмотров: 22
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Задача 1
Один моль идеального газа переходит из начального состояния 1 в конечное состояние 3 в результате двух изопроцессов 1-2 и 2-3. Значение давления и объема газа в состояниях 1 и 3 равны соответственно Р1, V1 и Р3, V3. Найти давление, объем и температуру газа Р2, V2, Т2 в промежуточном состоянии 2. Изобразить процессы в координатах Р-V, P-T и T-V.
| Дано: Процесс 1-2 изотермический 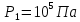 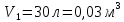 Процесс 2-3 изохорный 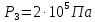 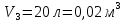 | Решение: Поскольку процесс 1-2 изотермический, то Т2 = Т1. Поскольку процесс 2-3 изохорный, то V2 = V3 = 0,02 м3. Запишем уравнение Менделеева-Клапейрона для 2 состояния газа: P2V2 = νRT2 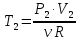 При изотермическом процессе: 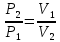 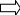 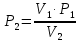 = =  = 1,5∙105 Па = 1,5∙105 Па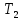 = =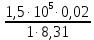 = 361 К, = 361 К, где R = 8,31 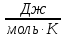 - универсальная газовая постоянная. - универсальная газовая постоянная.Запишем уравнение Менделеева-Клапейрона для 3 состояния газа: P3V3 = νRT3 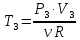 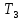 = =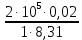 = 481 К, = 481 К, Температура Т1 = Т2 = 361 К. | | |||
| Найти: P2 - ? V2 - ? Т2 - ? Изобразить Р-V P-T T-V | | ||||
| Для построения графиков процессов запишем параметры газа в каждой точке: В 1-й точке - Т1 = 361 К, Р1 = 105 Па, V1 = 0,03 м3 Во 2-й точке - Т2 = 361 К, Р2 = 1,5∙105 Па, V2 = 0,02 м3 В 3-й точке - Т3 = 481 К, Р3 = 2 ∙105 Па, V3 = 0,02 м3 Изобразим процесс в координатах Р – V 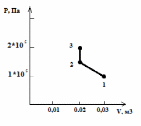 Изобразим процесс в координатах Р – Т 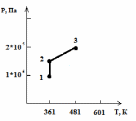 Изобразим процесс в координатах V – T 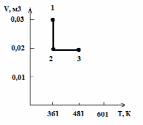 Ответ: Р2 = 1,5∙105 Па V2 = 0,02 м3 | |||||
| Т2 = 361 К Задача 2 Идеальный газ совершает замкнутый цикл, состоящий из трех процессов 1-2, 2-3, 3-1. Значение давления и объема газа в состояниях 1, 2 и 3 равны соответственно Р1, V1, P2, V2 и P3, V3. Найти термический КПД цикла. | |||||
| |||||
Запишем уравнение Менделеева-Клапейрона для процесса 1-2:
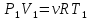
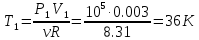
где R = 8,31
 - универсальная газовая постоянная.
- универсальная газовая постоянная.При изохорном процессе давление газа прямо пропорционально его абсолютной температуре.
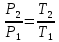
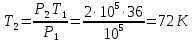
Тогда
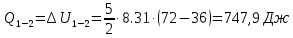 ,
,где i=5 – степень свободы молекул двухатомного газа.
Для адиабатного процессa 2-3 Q2-3 = 0.
Учитывая, что для изотермического процесса 3-1
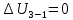 , по первому закону термодинамики получаем:
, по первому закону термодинамики получаем: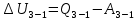
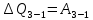
Работа газа при изотермическом процессе вычисляется по формуле:
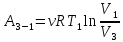
Согласно уравнению Менделеева – Клапейрона для первого состояния газа, получаем:
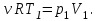
После подстановки, получаем:
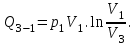
Найдём объём
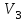 для третьего состояния.
для третьего состояния.Для изохорного процесса 1 – 2
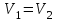 .
.Для изотермического процесса 3 – 1, имеем:
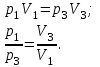
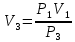
Для адиабатного процесса 2 – 3, получаем:
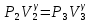
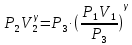
Где
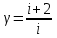 - показатель адиабаты.
- показатель адиабаты.
Следовательно:
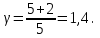
Подставим численные значения и произведём вычисления объём азота
 для третьего состояния:
для третьего состояния: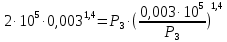
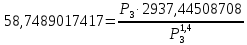
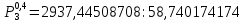
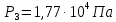
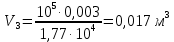
Подставим численные значения и произведём вычисления
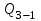 :
: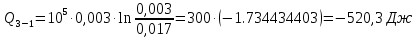
Количество теплоты, полученное газом за цикл от нагревателя:
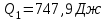
Количество теплоты, отданое газом за цикл холодильнику:
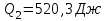
Теперь вычисляем КПД цикла:
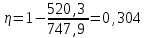
Ответ:
Задача 3
Идеальный газ находится в однородном поле тяжести Земли. Молярная масса газа М = 29 ∙ 10-3 кг/моль. Абсолютная температура газа меняется с высотой h по закону Т(h)=T0(1+ah). Найти давление газа P на высоте h. На высоте h=0 давление газа Р0=105 Па.
| Дано: М=29∙10-3 кг/моль h=0 P0=105 Па T0=250 K a=10-5 м-1 h=100 м | Применим барометрическую формулу: 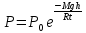 , ,где g=9,81 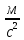 - ускорение свободного падения, R=8,31 - ускорение свободного падения, R=8,31 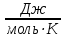 - универсальная газовая постоянная. - универсальная газовая постоянная.Учитывая условие задачи, получаем: 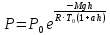 Подставим числовые значения из условия задачи и вычислим: 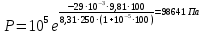 Ответ: Р = 98641 Па |
| Р - ? |