Файл: Вср 10 индикаторные электроды в потенциометрии Потенциометрия.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.10.2023
Просмотров: 36
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Шнякин 70СМ
ВСР 10 индикаторные электроды в потенциометрии
Потенциометрия
Основана на измерении потенциала ячейки, т.е. разности потенциалов между двумя электродами (индикаторным электродом и электродом сравнения) в отсутствие тока (I = 0) во внешней цепи.
Подразделяется на методы:
Прямые (напр. рН-метрия);
Косвенные (потенциометрическое титрование)
Потенциометрическая ячейка
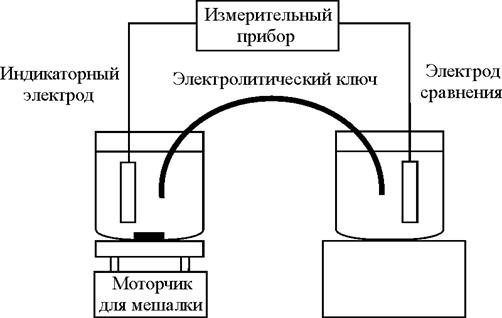
Электроды потенциометрического метода анализа
Электрод первого рода – металл, погруженный в раствор соли этого же металла;
Электрод второго рода – металл, покрытый слоем его труднорастворимой соли.
В потенциометрическом анализе из электродов составляется гальванический элемент, э.д.с. которого контролируется в ходе анализа.
Гальванический элемент образуют два
электрода: индикаторный электрод и электрод сравнения
Индикаторный электрод
Важными требованиями к электроду сравнения являются: обратимость,
воиспроизводимость и стабильность во времени.
1)Классические электроды:
Класс0.Инертные металлы;
Класс 1. Обратимые: металл /ион металла;
Класс 2. Обратимые: металл в равновесии с насыщенным раствором соли иона металла и избытком аниона Х+;
Класс 3. Обратимые: металл в равновесии с двумя малорастворимыми солями с общим анионом (или растворимым комплексом иона второго металла) и избытком второго катиона;
2) Мембранные (ион-селективные) электроды.
Должны удовлетворять следующим требованиям:
равновесный потенциал электрода должен быть воспроизводимым и устанавливаться быстро, иначе анализ потребует много времени;
обратимость: потенциал должен изменяться с изменением концентрации иона;
химическая устойчивость: не должен реагировать с другими компонентами, находящимися в растворе.
В качестве индикаторных электродов используют:
водородный электрод;
хингидронный электрод;
ионоселективные мембранные электроды;
стеклянный электрод;
металлические электроды 1-го и 2-го рода (изготавливают из Ag, Hg, Cd).
Рис.2. Электроды сравнения: а - хлоридсеребряный; б – хлоридсеребряный электрод с двойным жидкостным соединением; в – каломельный электрод.
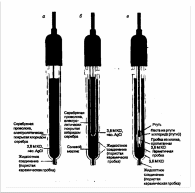
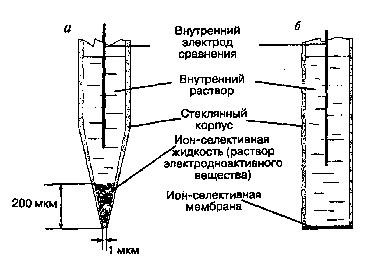
Рис.3. Ион-селективные электроды: а – микроэлектрод; б – мембранный макроэлектрод
Первичные ион-селективные электроды:
а) электроды со стеклянной мембраной;
б) кристаллические (твердофазные) мембранные электроды;
в) электроды с жидкой мембраной:
г) жидкие ионообменные мембранные электроды;
д) электроды с жидкой мембраной с нейтральными носителями.
Сложные или многомембранные ион-селективные электроды:
молекулярно-чувствительные устройства, такие, как газочувствительные или ферментные электроды.
Ион-селективные полевые транзисторы ИСТП:
Эти типы электродов – гибриды ион-селективных электродов и полевых транзисторов из оксидов металлов
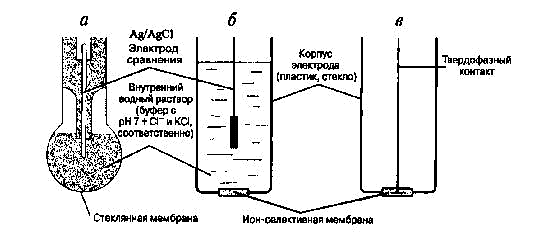
Рис.4. Ион-селективные электроды: а – стеклянный электрод; б – электрод с кристаллической мембраной; в – твердотельный электрод с кристаллической мембраной.
Преимуществами метода потенциометрического титрования по сравнению с обычным титрованием являются возможность:
титровать окрашенные растворы, когда цветные индикаторы неприменимы;
определять нескольких веществ в смеси, не прибегая к их предварительному разделению