ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 89
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
с1,c2,… процесс парообразования завершается и данные точки образуют верхнюю пограничную кривую, соответствующую сухому насыщенному пару (х = 1). Точки d1, d2,… (рис. 1) и f1, f2,… (рис. 2) соответствуют состоянию перегретого пара, а точка а – жидкости. Степень сухости:
х = ,
,
где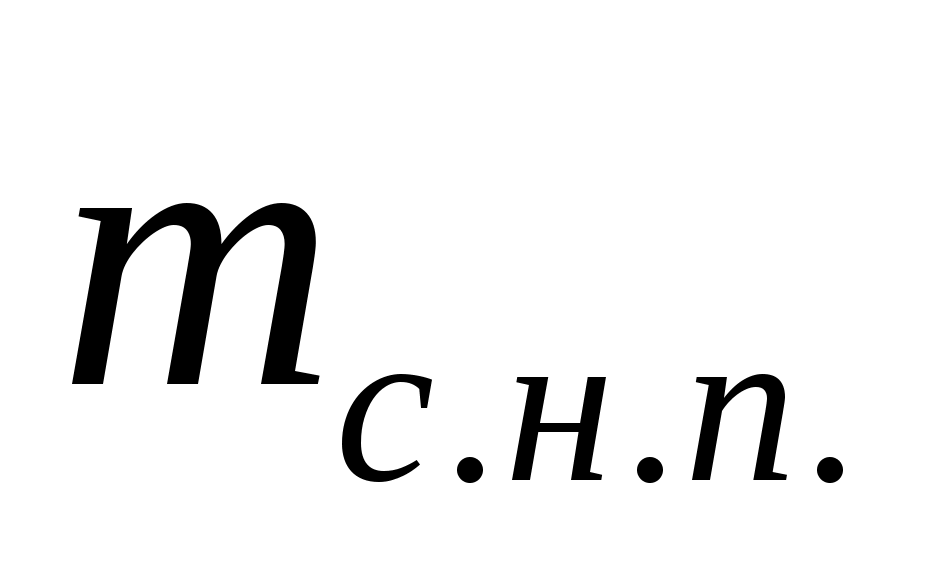 масса сухого насыщенного пара;
масса сухого насыщенного пара;
 масса влажного насыщенного пара;
масса влажного насыщенного пара;
 масса кипящей жидкости.
масса кипящей жидкости.
Н
Ψ1=pн(v”- v’)
а участках b1c1, b2c2,…, где происходит переход жидкости в пар, в равновесии находятся системы, состоящие из двух фаз (двух агрегатных состояний) – жидкой и парообразной, причем температура и давление этих фаз одинаковы. Участки b1c1, b2c2,… на обеих диаграммах являются одновременно изобарой и изотермой, т.е. переход жидкости в пар совершается при рн = const, tн = const.
Таким образом, на обеих диаграммах можно выделить три характерные области состояний:
Переход вещества из одной фазы в другую называется фазовым переходом. Вещества, находящиеся в разных агрегатных состояниях, имеют различные физические свойства. Это различие объясняется характером межмолекулярного взаимодействия.
Количество теплоты, которое необходимо подвести к 1 кг жидкости для перехода её в пар в изобарно-изотермическом (
рн и tн = const) процессе называется теплотой парообразования r, кДж/кг. Она расходуется на работу расширения и на преодоление сил межмолекулярного взаимодействия
и на преодоление сил межмолекулярного взаимодействия  :
:
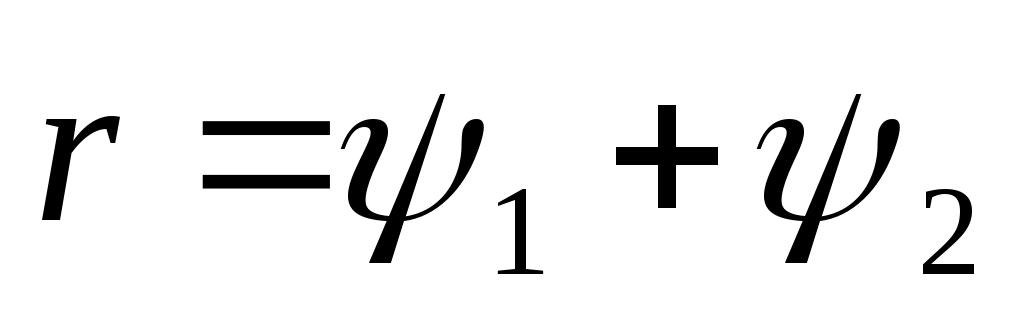 , (1)
, (1)
где внешняя составляющая теплоты парообразования, она рассчитывается как
внешняя составляющая теплоты парообразования, она рассчитывается как
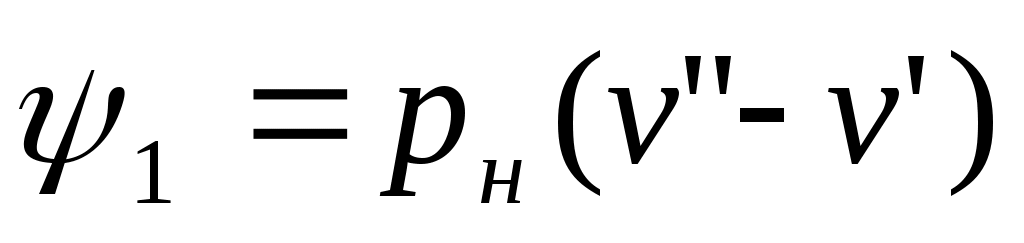 , (2)
, (2)
где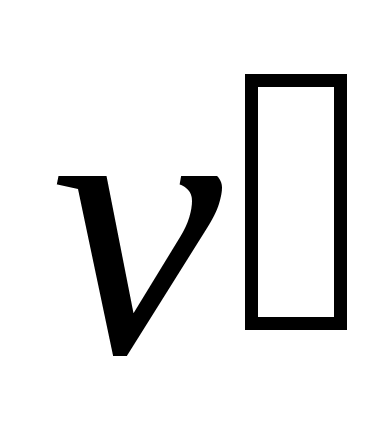 и
и 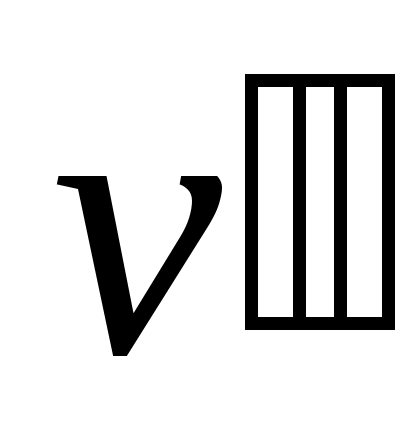 удельные объемы кипящей жидкости и сухого насыщенного пара соответственно;
удельные объемы кипящей жидкости и сухого насыщенного пара соответственно;
 внутренняя составляющая теплоты парообразования.
внутренняя составляющая теплоты парообразования.
На pv-диаграмме (рис. 1), как следует из уравнения (2), величина показана заштрихованной площадкой. На Ts-диаграмме (рис.2) заштрихованной площадкой показана величина теплоты парообразования, которая может быть рассчитана как:
показана заштрихованной площадкой. На Ts-диаграмме (рис.2) заштрихованной площадкой показана величина теплоты парообразования, которая может быть рассчитана как:
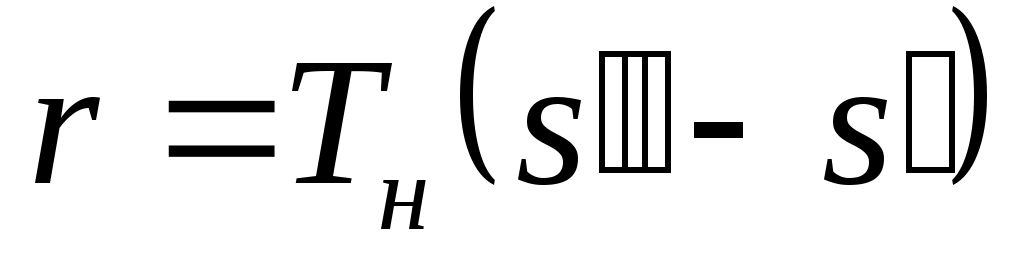 , (3)
, (3)
где и
и  энтропия кипящей жидкости и сухого насыщенного пара соответственно,
энтропия кипящей жидкости и сухого насыщенного пара соответственно, 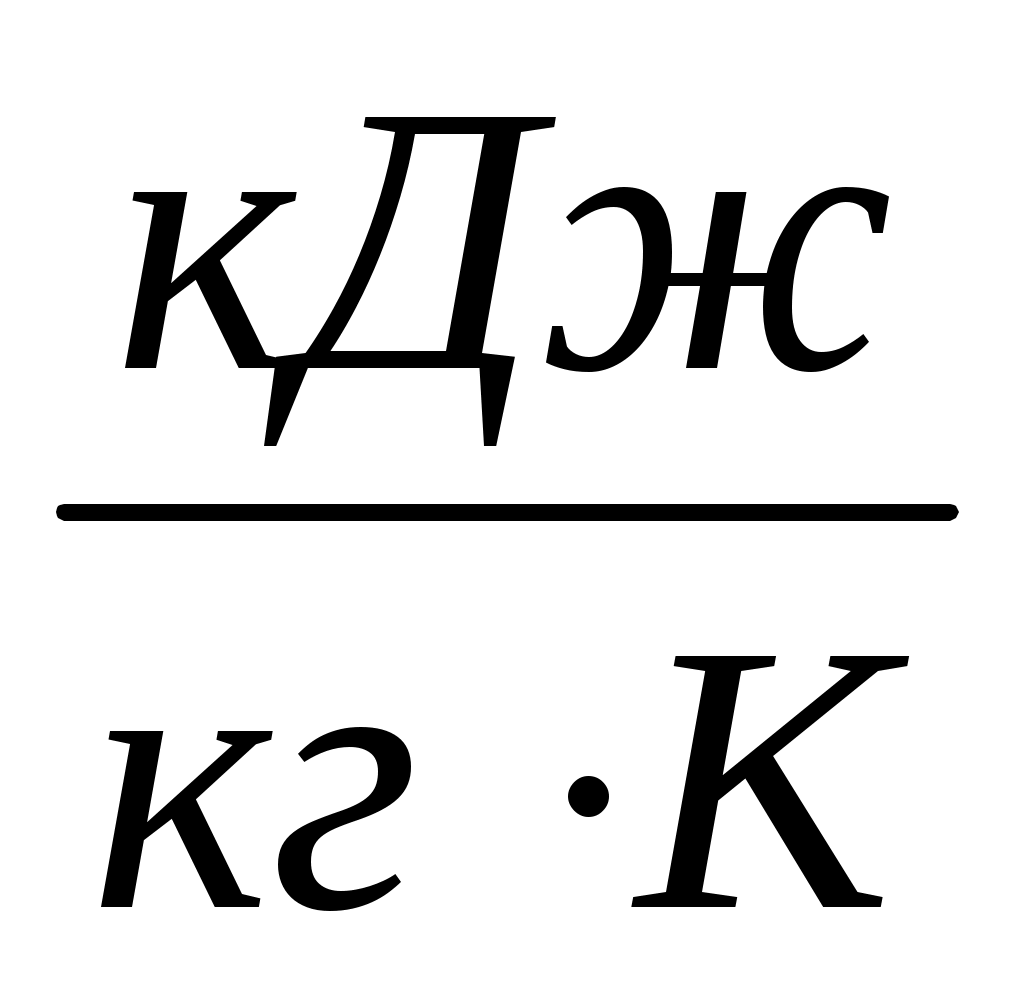 ;
;
Тн температура насыщения, К.
Из pv- и Тs-диаграмм видно, что с увеличением давления р точки b1, b2,… на нижней пограничной кривой сближаются с точками с1, с2, …на верхней пограничной кривой и в критической точке они сходятся. Так, для воды критические параметры в точке К имеют следующие значения: ркр. = 22,13 МПа, tкр. = 374,2 С, vкр. = 0,00326 м3/кг.
Выше критической точки К при p > pкр. и Т > Ткр. двухфазного состояния не наблюдается. Жидкая фаза находится под весьма большим внутренним давлением. Фактором, определяющим интенсивность межмолекулярных взаимодействий, является не давление, а температура. С ростом температуры и давления теплота парообразования
r уменьшается, а в критической точке r = 0,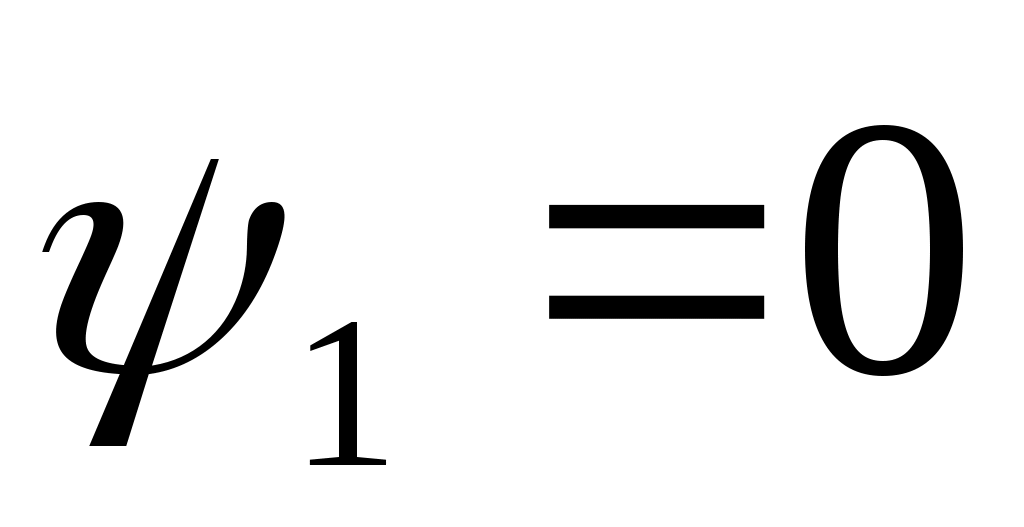 и
и 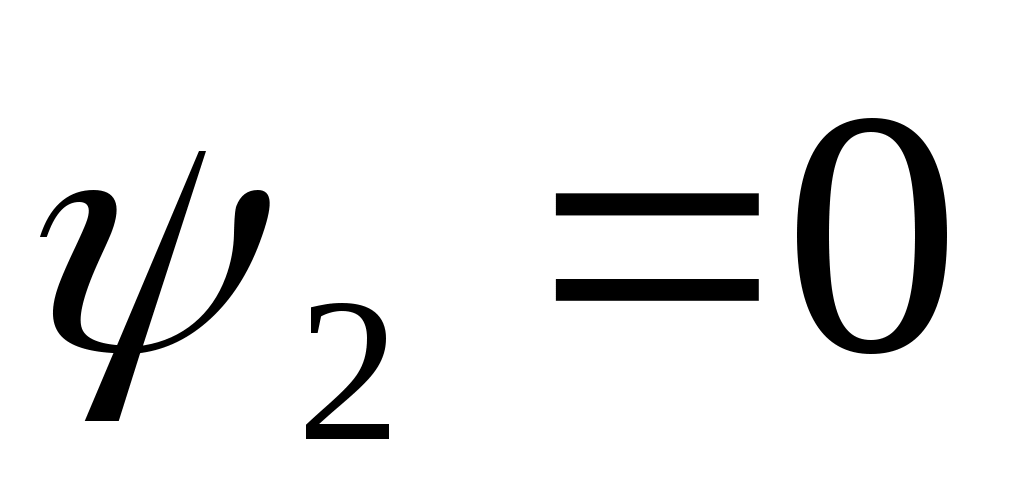 , т.к. в этом состоянии исчезает различие между жидкостью и ее паром и процесс парообразования отсутствует.
, т.к. в этом состоянии исчезает различие между жидкостью и ее паром и процесс парообразования отсутствует.
О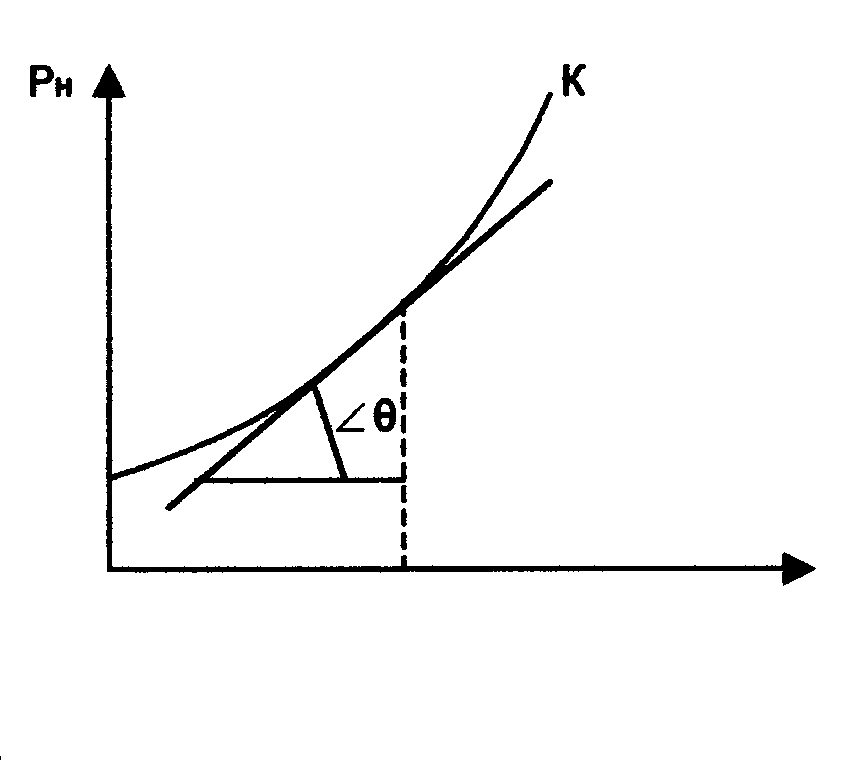
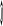
Δp
пытным путем было установлено, что каждому давлению р соответствует определенная температура насыщения tнас. (кипения) данной жидкости, являющаяся одновременно температурой насыщения пара, с которым жидкость находится в равновесии. Кривая зависимости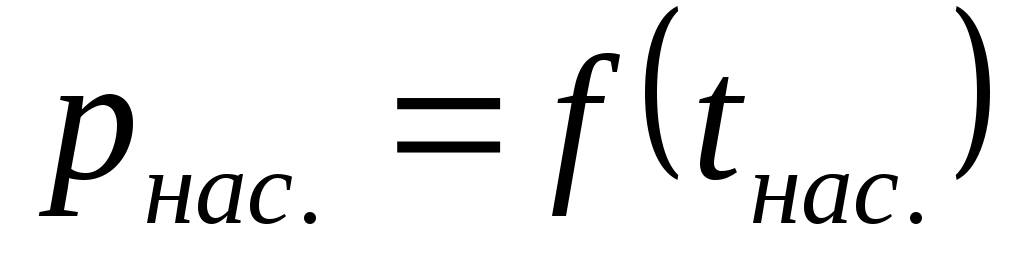 называется кривой насыщения, рис. 3.
называется кривой насыщения, рис. 3.
С
t*н tн
Рис.3. Кривая насыщения


Δt

вязь между температурой и давлением насыщения выражается уравнением Клапейрона-Клаузиуса.
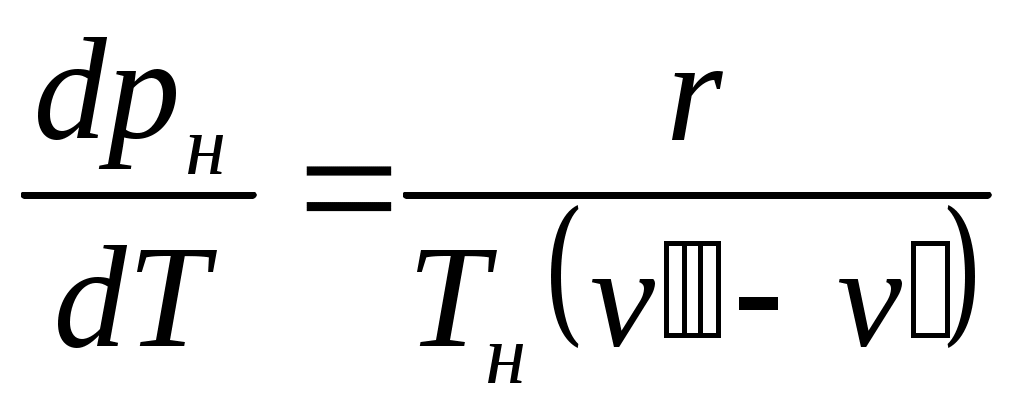 , (4)
, (4)
где ,
,  удельные объемы соответственно жидкости и сухого насыщенного пара на линии насыщения при Тнас. и рнас., м3/кг.
удельные объемы соответственно жидкости и сухого насыщенного пара на линии насыщения при Тнас. и рнас., м3/кг.
Поскольку >
>  , из уравнения (4) следует, что при фазовом переходе «жидкость-пар» производная
, из уравнения (4) следует, что при фазовом переходе «жидкость-пар» производная 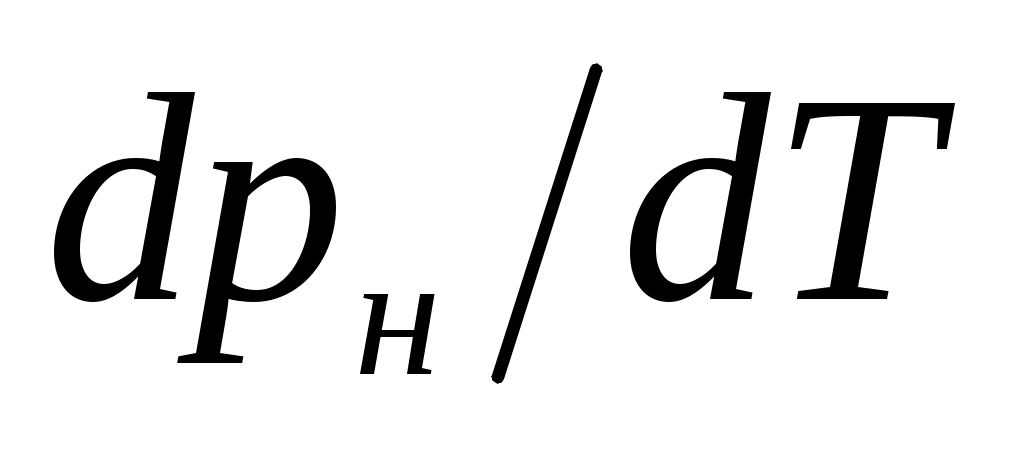 всегда больше нуля, т.е. с ростом давления температура насыщения увеличивается.
всегда больше нуля, т.е. с ростом давления температура насыщения увеличивается.
Уравнение Клапейрона-Клаузиуса (4) имеет важные достоинства. Во-первых, оно устанавливает связь между калорическими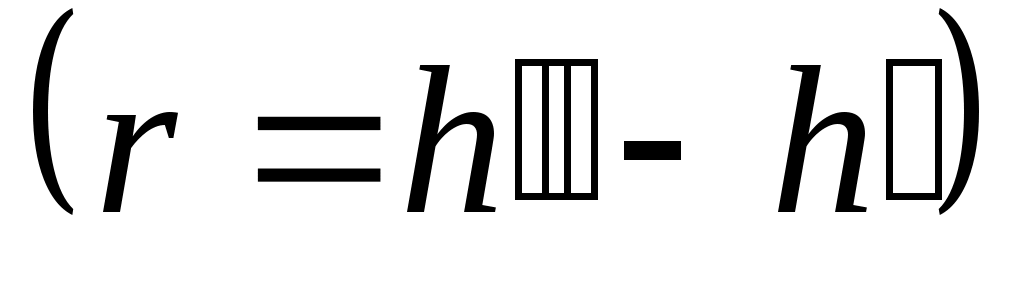 и термодинамическими (р, v, Т) параметрами. Во-вторых, дает связь между параметрами жидкого (
и термодинамическими (р, v, Т) параметрами. Во-вторых, дает связь между параметрами жидкого (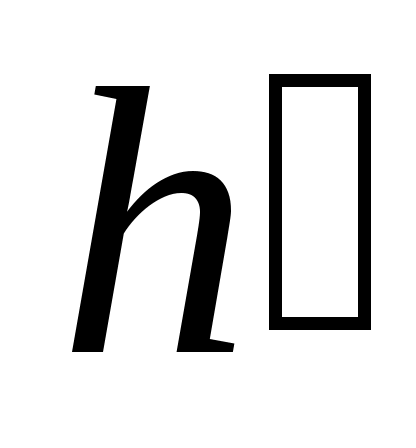 ,
,  ) и парообразного (
) и парообразного (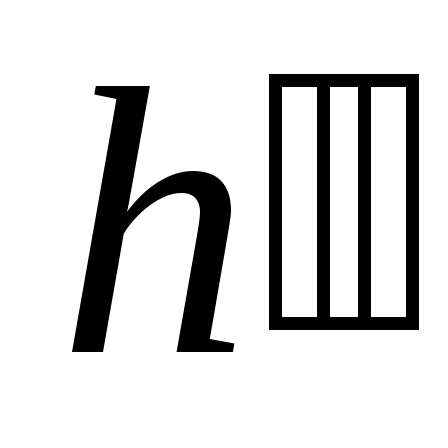 ,
,  ) состояний.
) состояний.
Первое из этих достоинств уравнения (4) в данной работе используется для определения теплоты парообразования r по кривой насыщения, полученной по результатам измерения термодинамических параметров рн и tн.
220 B
3
x
1-x
кспериментальная установка, рис. 4, представляет собой замкнутый сосуд высокого давления, содержащий такое количество воды, при котором удельный объем vx двухфазной системы «жидкость-пар» (влажного насыщенного пара) равен критическому значению в точке К:
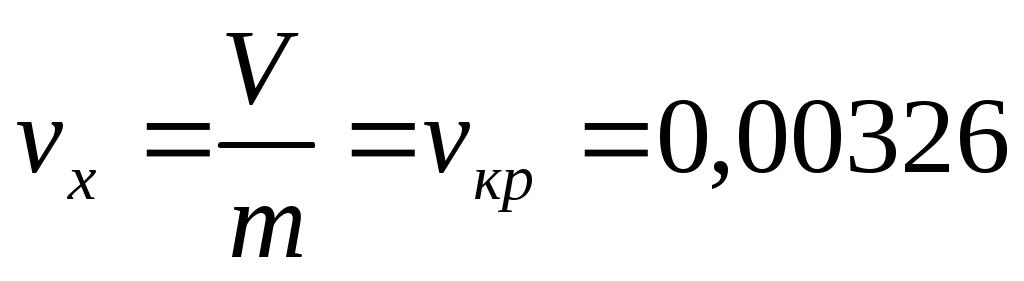 , м3/кг, (5)
, м3/кг, (5)
где V внутренний объем сосуда, м3;
т масса системы «жидкость-пар», кг;
vкр удельный объем системы в критической точке, м3/кг.
При изохорном (v = vx= const) электрическом нагревании система «жидкость-пар» проходит ряд равновесных двухфазных состояний до критической точки К (на рис. 1 и 2 процесс изображен пунктирными линиями). В опыте измеряются избыточные давления манометром 7. Соответствующие температуры насыщения tн устанавливаются по измеренным значениям э.д.с. дифференциальных термопар.
Порядок работ следующий:
Таблица 1
 задается преподавателем каждому студенту индивидуально.
задается преподавателем каждому студенту индивидуально.
Обработка опытных данных
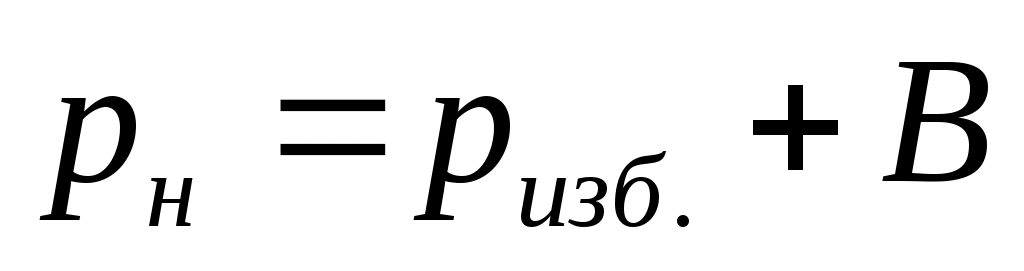 , Па;
, Па;
1 кгс/см2 = 735,6 мм рт. ст.;
750 мм рт. ст = 105 Па = 0,1 МПа.
Результаты занести в таблицу 1.
 = 1МПа
= 1МПа  1 см;
1 см;
 = 10 С
= 10 С 1 см.
1 см.
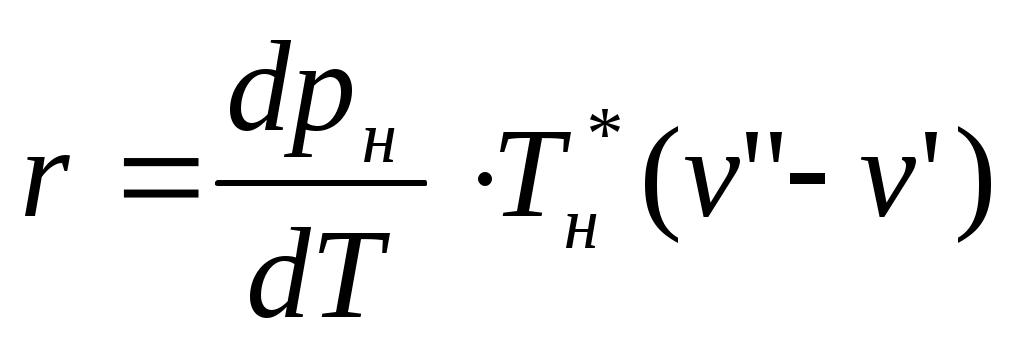 , кДж/кг.
, кДж/кг.
Значение производной определить графически как тангенс угла наклона касательной
определить графически как тангенс угла наклона касательной 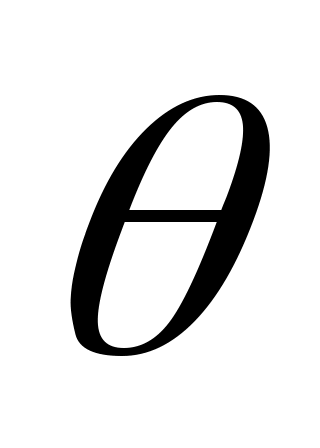 к кривой насыщения в точке с температурой
к кривой насыщения в точке с температурой  (геометрический смысл первой производной!) (рис. 3), т.е. с учетом размерностей:
(геометрический смысл первой производной!) (рис. 3), т.е. с учетом размерностей:
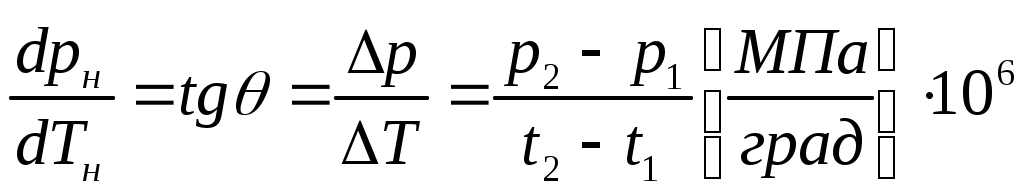 , Па/град.
, Па/град.
Точность теплоты парообразования
х =
где
Н
Ψ1=pн(v”- v’)
а участках b1c1, b2c2,…, где происходит переход жидкости в пар, в равновесии находятся системы, состоящие из двух фаз (двух агрегатных состояний) – жидкой и парообразной, причем температура и давление этих фаз одинаковы. Участки b1c1, b2c2,… на обеих диаграммах являются одновременно изобарой и изотермой, т.е. переход жидкости в пар совершается при рн = const, tн = const.
Таким образом, на обеих диаграммах можно выделить три характерные области состояний:
-
область жидкого состояния – расположена левее кривой кипящей жидкости х = 0,t < tн; -
область влажного насыщенного пара – двухфазное состояние, где пар и жидкость находятся в равновесии и имеют одинаковые рн и tн. Эта область расположена между пограничными кривыми х = 0 и х = 1, т.е. в этой области 0 < x < 1; -
область перегретого пара – расположена правее кривой сухого насыщенного пара, х = 1 ,t>tнпри данном давлении.
Переход вещества из одной фазы в другую называется фазовым переходом. Вещества, находящиеся в разных агрегатных состояниях, имеют различные физические свойства. Это различие объясняется характером межмолекулярного взаимодействия.
Количество теплоты, которое необходимо подвести к 1 кг жидкости для перехода её в пар в изобарно-изотермическом (
рн и tн = const) процессе называется теплотой парообразования r, кДж/кг. Она расходуется на работу расширения
где
где
На pv-диаграмме (рис. 1), как следует из уравнения (2), величина
где
Тн температура насыщения, К.
Из pv- и Тs-диаграмм видно, что с увеличением давления р точки b1, b2,… на нижней пограничной кривой сближаются с точками с1, с2, …на верхней пограничной кривой и в критической точке они сходятся. Так, для воды критические параметры в точке К имеют следующие значения: ркр. = 22,13 МПа, tкр. = 374,2 С, vкр. = 0,00326 м3/кг.
Выше критической точки К при p > pкр. и Т > Ткр. двухфазного состояния не наблюдается. Жидкая фаза находится под весьма большим внутренним давлением. Фактором, определяющим интенсивность межмолекулярных взаимодействий, является не давление, а температура. С ростом температуры и давления теплота парообразования
r уменьшается, а в критической точке r = 0,
О

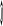
Δp
пытным путем было установлено, что каждому давлению р соответствует определенная температура насыщения tнас. (кипения) данной жидкости, являющаяся одновременно температурой насыщения пара, с которым жидкость находится в равновесии. Кривая зависимости
С
t*н tн
Рис.3. Кривая насыщения


Δt

вязь между температурой и давлением насыщения выражается уравнением Клапейрона-Клаузиуса.
где
Поскольку
Уравнение Клапейрона-Клаузиуса (4) имеет важные достоинства. Во-первых, оно устанавливает связь между калорическими
Первое из этих достоинств уравнения (4) в данной работе используется для определения теплоты парообразования r по кривой насыщения, полученной по результатам измерения термодинамических параметров рн и tн.
Проведение опытов
Э
Рис.4. Схема экспериментальной установки:
1 – сосуд высокого давления; 2 – спираль электронагревателя; 3 – переключатель электронагревателя; 4 – вентилятор; 5 – переключатель вентилятора; 6 – кожух; 7 – образцовый манометр; 8 – контактный манометр, автоматически отключающий нагреватель по достижении давления 216 бар (55 дел.); 9 – милливольтметр; 10 – дифференциальная термопара.
tнас
tокр
220 B
220 BПроведение опытов
Э

Рис.4. Схема экспериментальной установки:
1 – сосуд высокого давления; 2 – спираль электронагревателя; 3 – переключатель электронагревателя; 4 – вентилятор; 5 – переключатель вентилятора; 6 – кожух; 7 – образцовый манометр; 8 – контактный манометр, автоматически отключающий нагреватель по достижении давления 216 бар (55 дел.); 9 – милливольтметр; 10 – дифференциальная термопара.
tнас
tокр
3
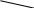
x
1-x
кспериментальная установка, рис. 4, представляет собой замкнутый сосуд высокого давления, содержащий такое количество воды, при котором удельный объем vx двухфазной системы «жидкость-пар» (влажного насыщенного пара) равен критическому значению в точке К:
где V внутренний объем сосуда, м3;
т масса системы «жидкость-пар», кг;
vкр удельный объем системы в критической точке, м3/кг.
При изохорном (v = vx= const) электрическом нагревании система «жидкость-пар» проходит ряд равновесных двухфазных состояний до критической точки К (на рис. 1 и 2 процесс изображен пунктирными линиями). В опыте измеряются избыточные давления манометром 7. Соответствующие температуры насыщения tн устанавливаются по измеренным значениям э.д.с. дифференциальных термопар.
Порядок работ следующий:
-
Установка включается преподавателем; -
Измерения начинать по достижении показания манометра 5 делений и далее через каждые 5 делений. Одновременно с показаниями манометра в таблицу 1 записывать показания э.д.с. термопары е, мВ, измеряемые милливольтметром 9. -
По достижении показаний манометра 50 делений показать результаты преподавателю. -
Определить температуру окружающей среды tокр и атмосферное давление В. Заполнить таблицу 1. -
С разрешения преподавателя установку можно отключить.
Таблица 1
| ризб. | рн, МПа | е, мВ | | tокр, С | tн, С | В, мм рт. ст. | |
| делений | кгс/см2 | ||||||
| 5 | | | | | | | |
| 10 | | | | | | ||
| 15 | | | | | | | Дата и подпись преподавателя: |
| 20 | | | | | | ||
| 25 | | | | | | ||
| 30 | | | | | | ||
| 35 | | | | | | ||
| 40 | | | | | | | |
| 45 | | | | | | ||
| 50 | | | | | | ||
Обработка опытных данных
-
Рассчитать абсолютное давление насыщенного пара для всех точек:
1 кгс/см2 = 735,6 мм рт. ст.;
750 мм рт. ст = 105 Па = 0,1 МПа.
-
По величинам е из градуировочного графика определить значения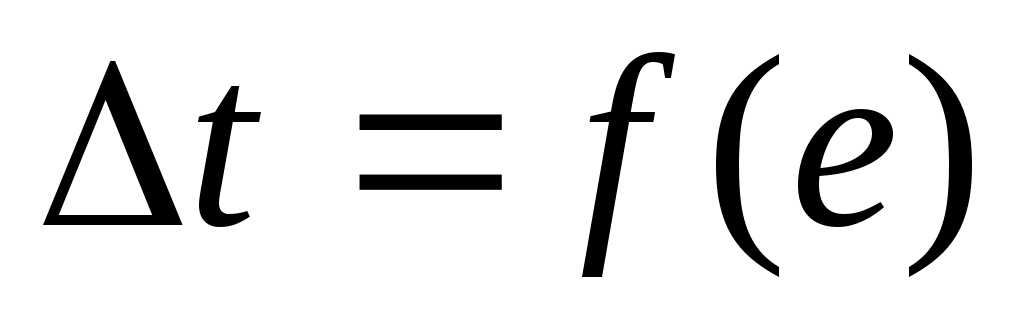 , где
, где 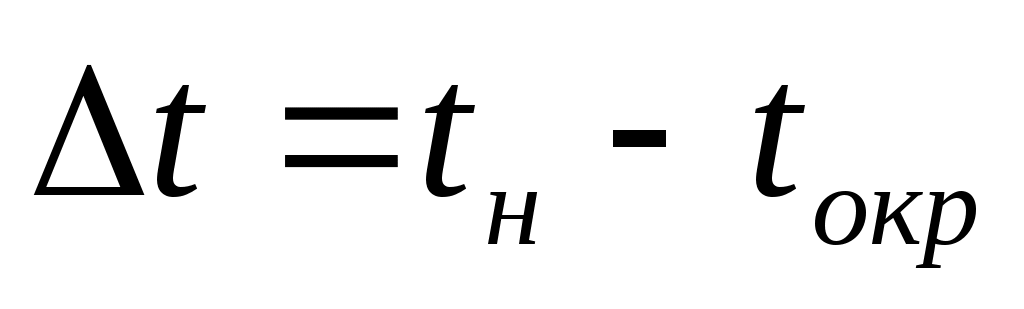 .Искомая температура насыщения
.Искомая температура насыщения 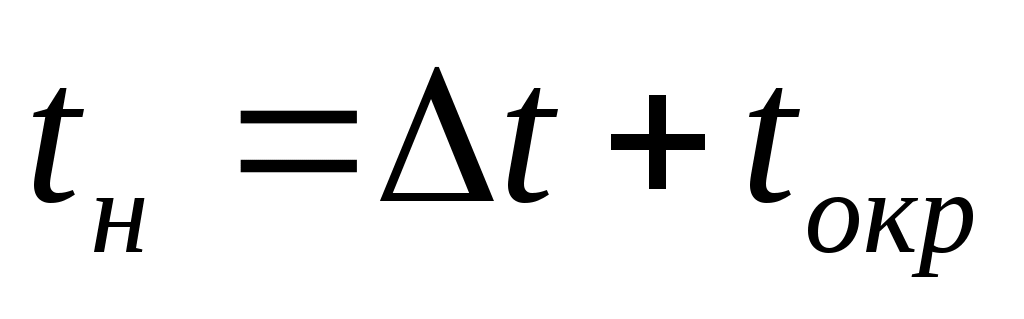 , С.
, С.
Результаты занести в таблицу 1.
-
На миллиметровой бумаге по опытным данным рн и tн построить кривую насыщения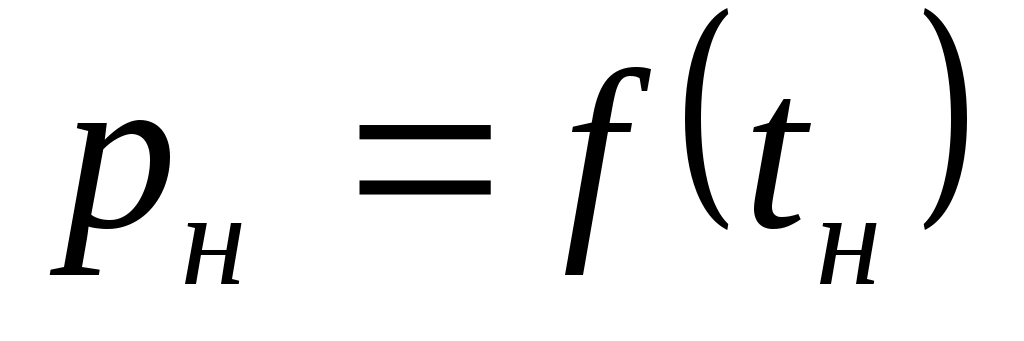 (рис. 3), выбрав масштабы по осям
(рис. 3), выбрав масштабы по осям
-
С помощью уравнения (4) рассчитать теплоту парообразования r при заданной температуре :
:
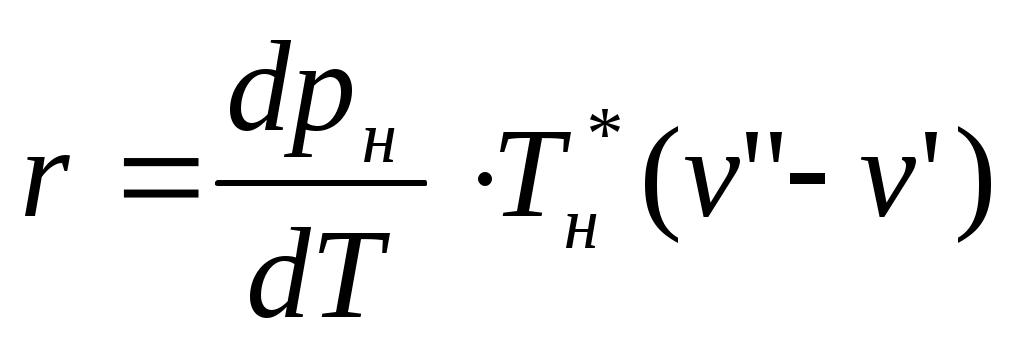 , кДж/кг.
, кДж/кг.Значение производной
Точность теплоты парообразования