ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 17.11.2021
Просмотров: 1079
Скачиваний: 1
СОДЕРЖАНИЕ
Протипожежне скло – армоване скло.
Організація та методика проведення лабораторних робіт
4. Постійно стежить за справністю машин і приладів, проводить їх профілактичний і поточний ремонти.
5. Виконує інші роботи за завданням завідувача лабораторіями.
Розділ
1. Матеріалознавство.
Особливості
атомно-кристалічної будови металів
-
Загальні поняття про матеріалознавство
Матеріалознавство – це наука про взаємозв'язки електронної будови, структури матеріалів з їх складом, фізичними, хімічними, технологічними й експлуатаційними властивостями.
Створення наукових основ металознавства по праву належить Д. К. Чернову, який встановив критичні температури фазових перетворень у сталях і їх зв'язок із кількістю вуглецю в сталях. Цим були закладені основи для найважливішої в металознавстві діаграми стану залізовуглецевих сплавів.
Відкриттям алотропічних перетворень у сталі Д. К. Чернов заклав фундамент термічної обробки сталі. Критичні точки фазових перетворень у сталі, дозволили раціонально вибирати температуру її гартування, відпуску і пластичної деформації у виробничих умовах.
У своїх роботах із проблем кристалізації сталі і будови злитка Д. К. Чернов виклав основні положення теорії лиття, що не втратили свого наукового і практичного значення в даний час.
Великий російський металург П. П. Аносов уперше застосував мікроскоп для дослідження структури металів. Йому належить пріоритет у створенні легованих сталей. Він розробив теорію і технологію виготовлення клинків із булатної сталі. З його робіт стало зрозуміло, що так званий булатний узор на поверхні сталі безпосередньо залежить від її внутрішньої структури.
У 1873–1876 роках Джозія Уіллард Гіббс виклав основні закони фазової рівноваги і, зокрема, правило фаз, ґрунтуючись на законах термодинаміки. Для вирішення практичних завдань знання фазової рівноваги в тій або іншій системі необхідне, але не достатнє для визначення складу і відносної кількості фаз. Обов'язково потрібно знати структуру сплавів, тобто атомну будову фаз, складових сплавів, а також розподіл, розмір і форму кристалів кожної фази.
Визначення атомної будови фаз стало можливим після відкриття Макс фон Лауе (1912 р.), який довів, що атоми в кристалі регулярно заповнюють простір, утворюючи просторові дифракційні решітки, і що рентгенівські промені мають хвилеву природу. Дифракція рентгенівських променів на таких решітках дає можливість досліджувати будову кристалів.
Останнім часом для структурного аналізу окрім рентгенівських променів використовують також електрони і нейтрони. Відповідні методи дослідження називаються електронографією і нейтронографією. Електронна оптика дозволила удосконалити мікроскопію. В даний час на електронних мікроскопах корисне максимальне збільшення доведене до 100000 разів.
У п'ятидесятих роках, коли почалося дослідження природи властивостей металевих матеріалів, було доведено, що більшість найважливіших властивостей, зокрема опір пластичній деформації і руйнуванню в різних умовах вантаження, залежать від особливостей тонкої кристалічної будови. Цей висновок сприяв залученню фізичних теорій про будову реальних металів для пояснення багатьох незрозумілих явищ і для конструювання сплавів із заданими механічними властивостями. Завдяки теорії дислокацій вдалося отримати достовірні відомості про зміни в металах за їх пластичних деформацій.
Особливо інтенсивно розвивається металознавство в останні десятиліття. Це пояснюється потребою в нових матеріалах для дослідження космосу, розвитку електроніки, атомної енерґетики.
Основними напрямами в розвитку металознавства є розробка способів виробництва чистих і надчистих металів, властивості яких значною мірою відрізняються від властивостей металів технічної чистоти, з яких переважно виготовляють вироби. Головним завданням матеріалознавства є створення матеріалів із заздалегідь розрахованими властивостями стосовно заданих параметрів і умов роботи. Велика увага приділяється вивченню металів у екстремальних умовах (низькі і високі температури, тиск).
До теперішнього часу основною матеріальною базою машинобудування була чорна металургія, що застосовує сталі і чавуни. Ці матеріали мають багато позитивних якостей і, в першу чергу, забезпечують високу конструкційну міцність деталей машин. Проте ці класичні матеріали мають такі недоліки як велика щільність, низька корозійна стійкість. Втрати від корозії складають 20 % річного виробництва сталі і чавуну. Тому, за даними наукових досліджень, через 20–40 років усі розвинені країни перебудуються на масове використання металевих сплавів на базі титану, магнію, алюмінію. Ці легкі і міцні сплави дозволяють у 2–3 рази полегшити верстати і машини, в 10 разів зменшити витрати на їх ремонт.
За даними інституту імені А. Н. Байкова, в наший країні є всі умови для того, щоб протягом 10–15 років машинобудування могло перейти на випуск алюмінієво-титанової рухомої техніки, яка відрізняється легкістю, корозійною стійкістю і великим безремонтним ресурсом.
Важливе значення має усунення відставання нашої країни в галузі використання нових матеріалів замість традиційних (металевих) – пластмас, кераміки, матеріалів порошкової металургії, особливо композиційних матеріалів, що економить дефіцитні метали, знижує витрати енергії на виробництво матеріалів, зменшує масу виробів.
Розрахунками встановлено, що заміна ряду металевих деталей легкового автомобіля на вуглепластики з епоксидної смоли, армованої вуглецевими волокнами, дозволить зменшити масу машини на 40 %; вона стане міцнішою; зменшиться витрата палива, різко зросте стійкість проти корозії.
1.2. Метали, особливості атомно-кристалічної будови
З-поміж величезної кількості матеріалів метали з давніх часів завжди займали особливе місце.
Підтвердження цьому: в назвах епох (золоте, срібне, бронзове, залізне століття), на які греки ділили історію людства; в археологічних знахідках металевих виробів (ковані мідні прикраси, сільськогосподарські знаряддя); в побутовому використанні металів і сплавів в сучасній техніці.
Причина цього – в особливих властивостях металів, що вигідно відрізняють їх від інших матеріалів і роблять у багатьох випадках незамінними.
Метали – один із класів конструкційних матеріалів, що характеризується відповідним набором властивостей: «металевий блиск» (добра відбивна здатність), пластичність, висока теплопровідність, висока електропровідність.
Дані властивості обумовлені особливостями будови металів. Згідно теорії металевого стану, металом є речовина, що складається з позитивних ядер, навколо яких по орбітах обертаються електрони. На останньому рівні число електронів невелике і вони слабо зв'язані з ядром. Ці електрони мають можливість переміщуватися по всьому об’єму металу, тобто належати цілій сукупності атомів.
Таким чином, пластичність, теплопровідність і електропровідність забезпечуються наявністю «електронного газу».
Усі метали, що твердіють у нормальних умовах, є кристалічними речовинами, тобто укладання атомів у них характеризується відповідним порядком – періодичністю як у різних напрямах, так і у різних площинах. Цей порядок визначається поняттям «кристалічна решітка».
Іншими словами, кристалічна решітка – це уявні просторові ґрати, у вузлах яких розташовуються частинки, створюючи тверде тіло.
Елементарний осередок – елемент об’єму з мінімального числа атомів, багаторазовим перенесенням якого в просторі можна побудувати весь кристал.
Елементарний осередок характеризує особливості будови кристала. Основними параметрами кристала є (рис. 1.1):
-
розміри ребер елементарного осередку (а, в, с);
-
відстані між центрами найближчих атомів;
-
кути між вісями (α, β, χ);
-
координаційне число (К) вказує на число атомів, розташованих на найближчій однаковій відстані від будь-якого атома в ґратах;
-
щільність упаковки атомів у кристалічній решітці – об'єм, зайнятий атомами, які умовно розглядаються як жорсткі кулі. Її визначають як відношення об'єму, зайнятого атомами, до об'єму осередку (для об'ємноцентрованих кубічних ґрат – 0,68, для гранецентрованих кубічних ґрат – 0,74).
Класифікація можливих видів кристалічних решіток була проведена французьким вченим О. Браве; відповідно, вони отримали назву «Ґрати Браве».
Усього для кристалічних тіл існує чотирнадцять видів ґрат, розбитих на чотири типи;
-
примітивний – вузли ґрат співпадають із вершинами елементарних осередків;
-
базцентрований – атоми займають вершини осередків і два місця в протилежних гранях;
-
об'ємно-центрований – атоми займають вершини осередків і їх центр;
-
гранецентрований – атоми займають вершини осередків і центри всіх шести граней.
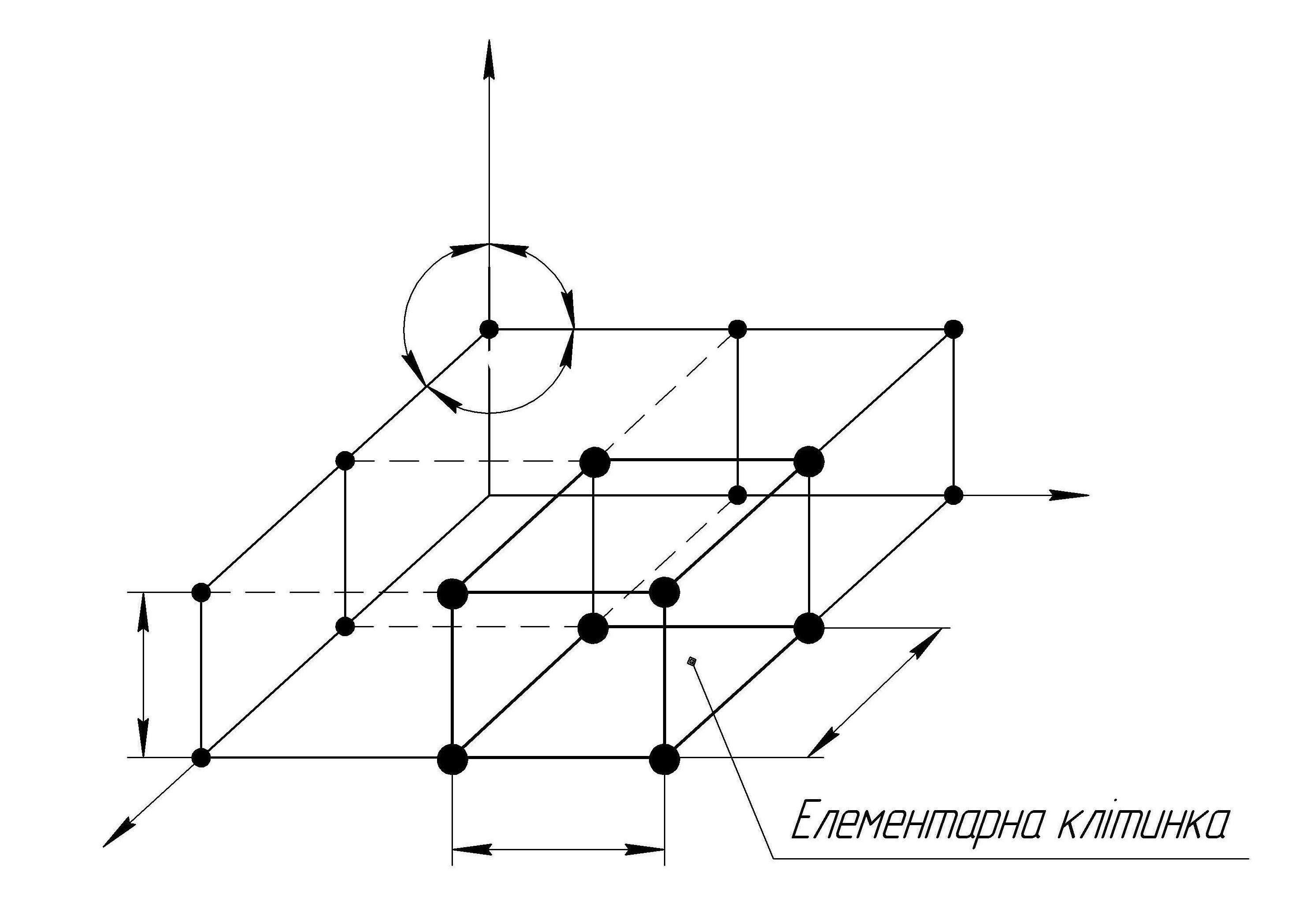
Рис. 1.1. Схема кристалічної решітки
Основними типами кристалічних ґрат є:
-
Об'ємно-центрована кубічна (ОЦК) (рис. 1.2 а): атоми розташовуються у вершинах куба і в його центрі (V, W, Ti, Fe).
-
Гранецентрована кубічна (ГЦК) (рис. 1.2 б): атоми розташовуються у вершинах куба і по центру кожної з 6 граней (Ag, Au, Fe).
-
Гексагональна, в основі якої лежить шестикутник: проста – атоми розташовуються у вершинах осередку і по центру двух основ (вуглець у вигляді графіту);
-
Щ
ільноупакована з трьома додатковими атомами в середній площині (Zn).
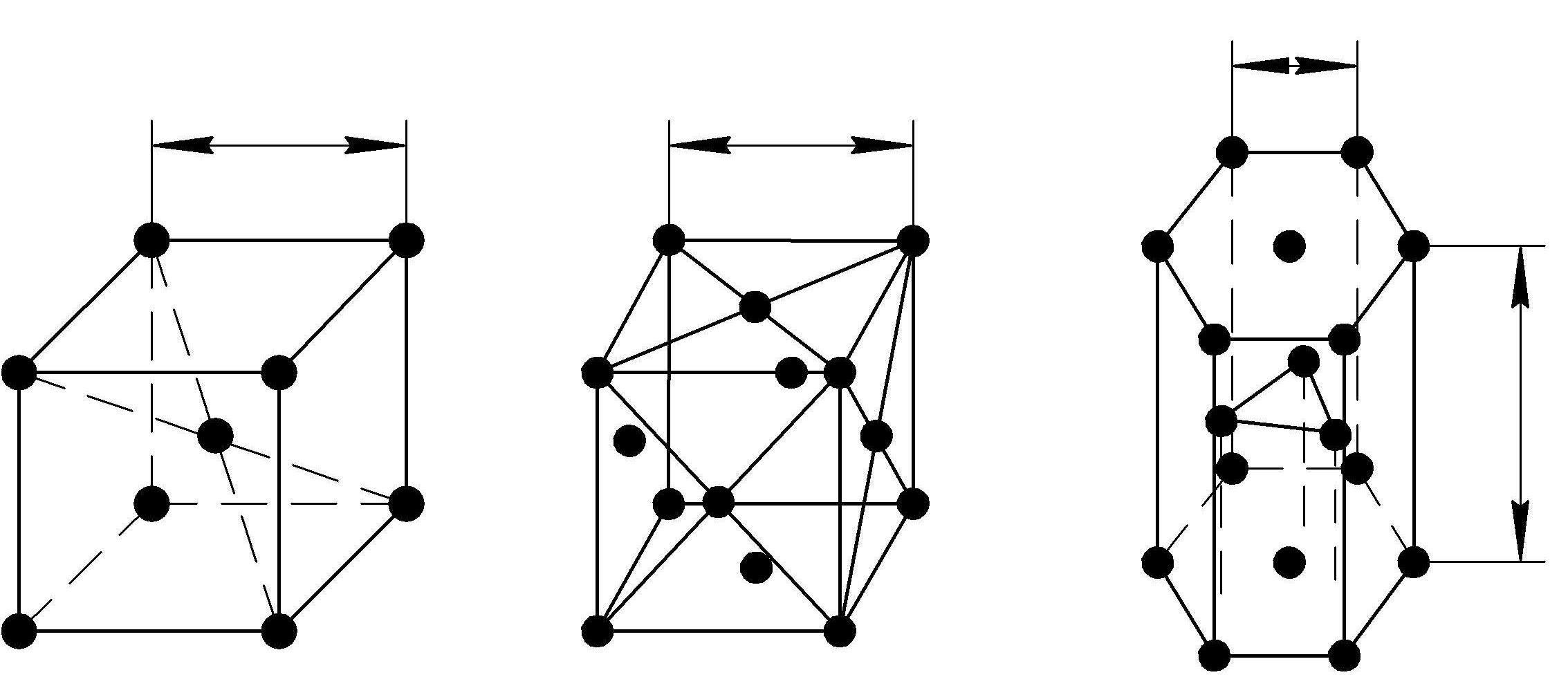
Рис.
1.2. Основні типи кристалічних решіток:
а – об'ємно-центрована кубічна; б –
гранецентрована кубічна;
в –
гексагональна щільноупакована
1.3. Поняття про ізотропію і анізотропію
Властивості тіла залежать від природи атомів, з яких воно складається, і від сили взаємодії між цими атомами. Сили взаємодії між атомами в значній мірі визначаються відстанями між ними. В аморфних тілах із хаотичним розташуванням атомів у просторі відстані між атомами в різних напрямах рівні, отже, властивості будуть однакові, тобто аморфні тіла ізотропні.
У кристалічних тілах атоми правильно розташовуються в просторі, причому по різних напрямах відстані між атомами неоднакові, що зумовлює істотні відмінності в силах взаємодії між ними і, в кінцевому підсумку, різні властивості. Залежність властивостей від напряму називається анізотропією.
1.4. Алотропія, або поліморфні перетворення
Здатність деяких металів існувати в різних кристалічних формах залежно від зовнішніх умов (тиск, температура) називається алотропією, або поліморфізмом. Кожний вид ґрат є алотропічною видозміною, або модифікацією.
Прикладом алотропічної видозміни залежно від температури є залізо (Fe) рис. 1.3.
t
< 9110C
ОЦК
- Feα;
911
< t <13920C
ГЦК
- Feγ;
1392
< t <15390C
ОЦК
- Feδ
(високотемпературне
Feα
)
Рис. 1.3. Крива охолодження чистого заліза
Перетворення однієї модифікації на іншу протікає за постійної температури і супроводжується тепловим ефектом. Видозміни елементу позначаються буквами грецького алфавіту у вигляді індексу основного позначення металу.
Прикладом алотропічної видозміни, обумовленої зміною тиску, є вуглець: за низького тиску утворюється графіт, а за високого – алмаз.
Використовуючи явище поліморфізму, можна зміцнювати сплави за допомогою термічної обробки.
1.5. Магнітні перетворення
Деякі метали намагнічуються під дією магнітного поля. Після усунення магнітного поля вони володіють залишковим магнетизмом. Це явище вперше виявлене на залізі й отримало назву феромагнетизму. До феромагнетиків належать залізо, кобальт, нікель і деякі інші метали.
У разі нагріву феромагнітні властивості металу зменшуються поступово: спочатку слабо, потім різко і за відповідної температури (точка Кюрі для заліза -768 °С) зникають. Вище за цю температуру метали стають парамагнетиками. Магнітні перетворення не пов'язані зі зміною кристалічної решітки або мікроструктури – вони обумовлені змінами в характері електронної взаємодії.
Розділ 2. Будова реальних металів. Дефекти кристалічної будови
2.1. Дефекти кристалічної структури
Із рідкого розплаву можна виростити монокристал. Їх зазвичай використовують у лабораторіях для вивчення властивостей тієї або іншої речовини.
Метали і сплави, отримані в звичайних умовах, складаються з великої кількості кристалів, тобто, мають полікристалічну будову. Ці кристали називаються зернами. Вони мають неправильну форму і по-різному орієнтовані в просторі. Кожне зерно має своє орієнтування кристалічної решітки, відмінне від орієнтування сусідніх зерен, унаслідок чого властивості реальних металів усереднюються, і явища анізотропії не спостерігається.
У кристалічній решітці реальних металів є різні дефекти (недосконалість), які порушують зв'язки між атомами та впливають на властивості металів. Розрізняють наступну структурну недосконалостей:
-
точкові – малі в усіх трьох вимірюваннях;
-
лінійні – малі у двох вимірюваннях і скільки завгодно протяжні в третьому;
-
поверхневі – малі в одному вимірюванні.
Однією з поширених недосконалостей кристалічної будови є наявність точкових дефектів: вакансій, дислокованих атомів і домішок (рис. 2.1).
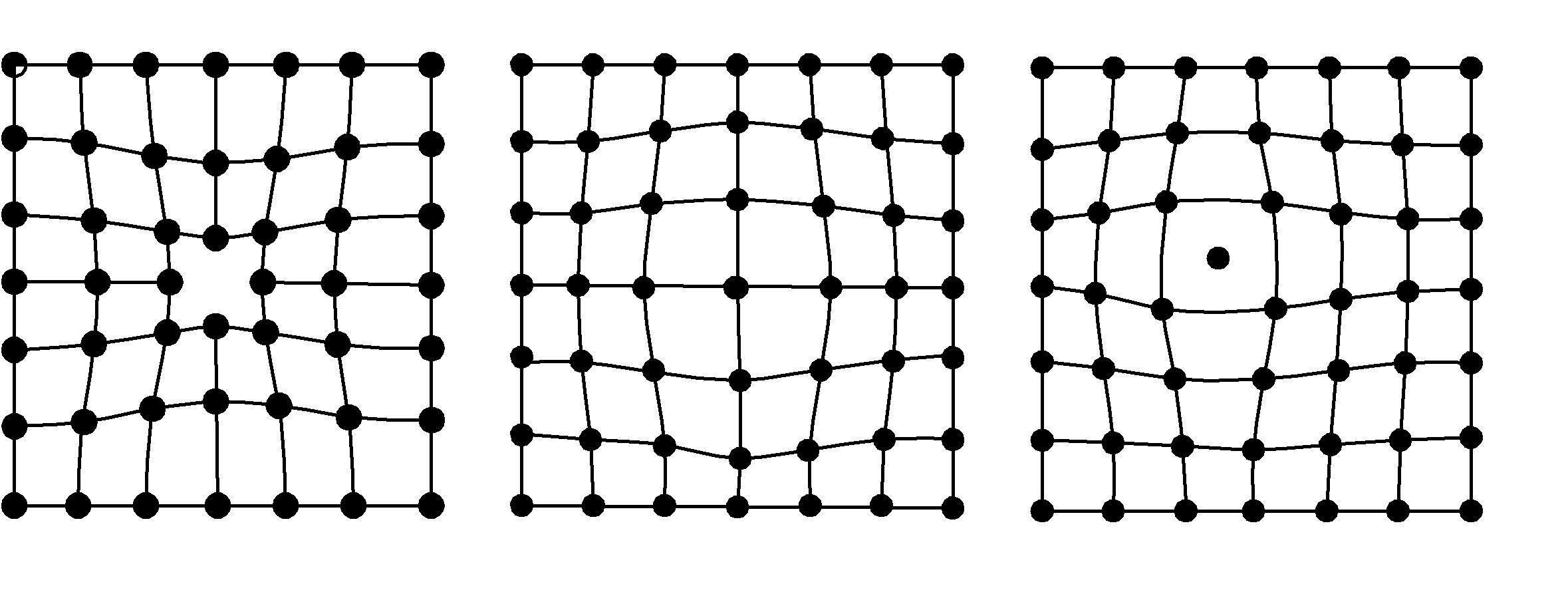
а) б) в)
Рис. 2.1. Точкові дефекти
Вакансія – відсутність атомів у вузлах кристалічної решітки, «дірки», що утворилися з різних причин. Утворюється під час переходу атомів із поверхні в навколишнє середовище або з вузлів ґрат на поверхню (межі зерен, порожнечі, тріщини і т. д.), у результаті пластичної деформації, під час «бомбардування» тіла атомами або частинками високих енерґій (опромінювання в циклотроні або нейтронні опромінювання в ядерному реакторі). Концентрація вакансій в значній мірі визначається температурою тіла. Переміщаючись по кристалу, одиночні вакансії можуть зустрічатися і об'єднуватися в девакансії. Скупчення багатьох вакансій може призвести до утворення пор і порожнеч.
Дислокований атом – це атом, що вийшов із вузла ґрат і зайняв місце в міжвузловині. Концентрація дислокованих атомів значно менша, ніж вакансій, оскільки для їх утворення потрібні істотні витрати енерґії. На місці атома, що перемістився, утворюється вакансія.
Домішкові атоми завжди присутні в металі, оскільки практично неможливо виплавити хімічно чистий метал. Вони можуть мати розміри більше або менше розмірів основних атомів і розташовуються у вузлах ґрат або між ними.
Точкові дефекти викликають незначні спотворення ґрат, що може призвести до зміни властивостей тіла (електропровідність, магнітні властивості). Їх наявність сприяє процесам дифузії і протіканню фазових перетворень у твердому стані. Дефекти можуть взаємодіяти.
П
θ
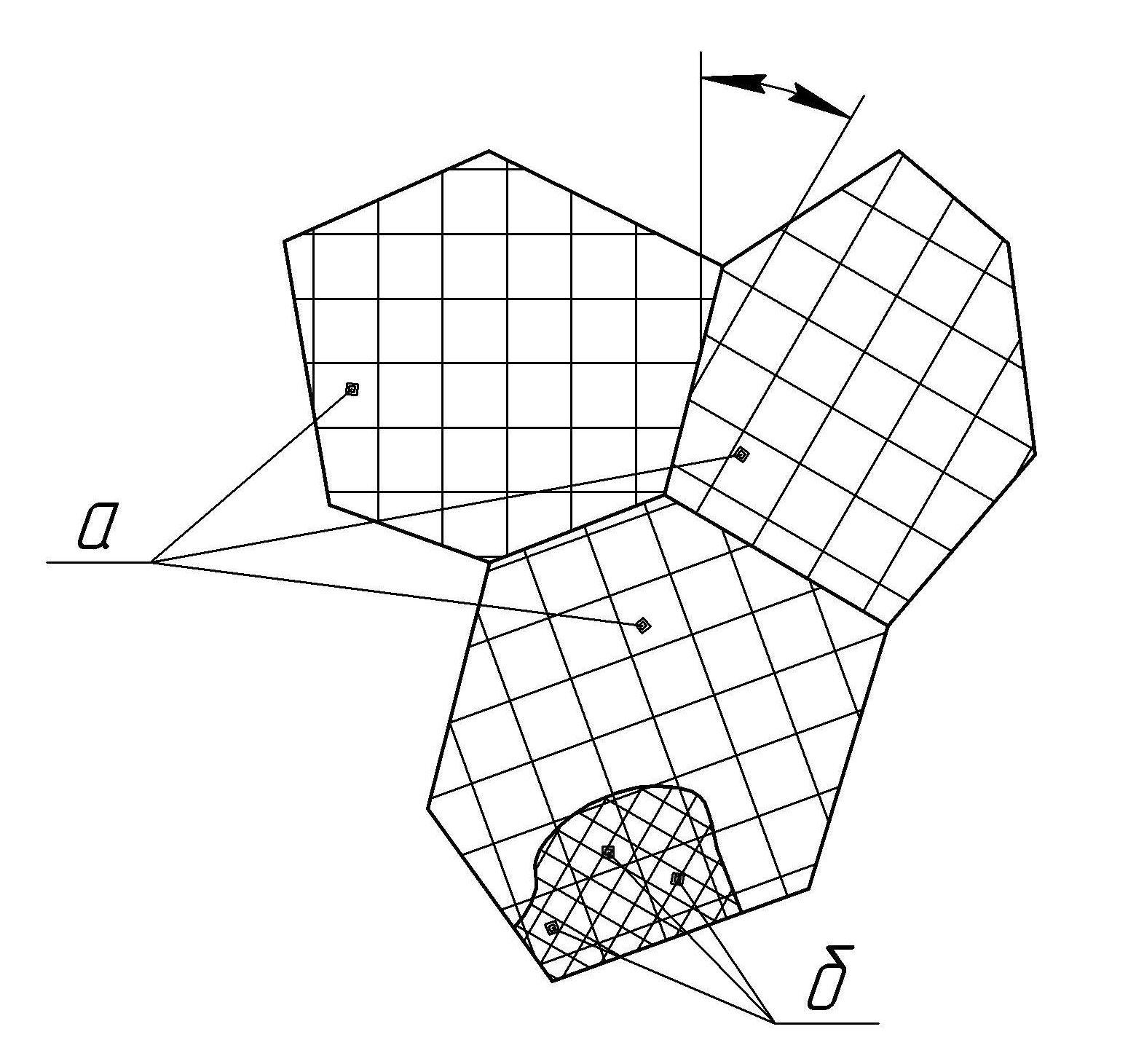
Рис. 2.2. Розорієнтація зерен і блоків в металі
Розміри зерен складають до 1000 мкм. Кути розорієнтації (θ) становлять до декількох десятків градусів.