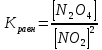Файл: Лабораторная работа 5 Химическое равновесие Студент, группы . зачетной книжки Принял.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 09.11.2023
Просмотров: 20
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Министерство науки и образования Российской Федерации
ИРКУТСКИЙ НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ
ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
Институт Заочно-вечернего обучения
Кафедра «Химии и биотехнологии имени В.В. Тутуриной»
Основы химии
Лабораторная работа №5
Химическое равновесие
Выполнил:
Студент, группы /
.
№ зачетной книжки
Принял:
Доцент /_____________/
Иркутск – 2023г.
Лабораторная работа
Опыт 1. Влияние изменения концентрации на смещение равновесия
Для опыта удобно воспользоваться реакцией
FeCl3 + 3KSCN
Из веществ этой системы только роданид железа (III) Fe(SCN)3 окрашен в красный цвет. Поэтому всякое изменение его концентрации можно легко заметить по изменению интенсивности окраски раствора, что позволяет сделать вывод о направлении смещения равновесия системы при изменении концентрации реагирующих веществ.
Смешать равные объемы разбавленных растворов хлорида железа (III) и роданида калия. Полученный раствор разлить поровну в 3 колбы.
В первую колбу добавить несколько капель концентрированного раствора хлорида железа (III), во вторую – несколько капель концентрированного раствора роданида калия, в третью – кристаллического хлорида калия. Сравнить окраску в трех колбах.
Требования к результатам опыта
1.В первую колбу добавляем одно из исходных веществ – хлорид железа. Окраска раствора становится более интенсивной. Это значит, что концентрация роданида железа увеличилась. Это демонстрирует принцип, что при увеличении концентрации исходных веществ равновесие реакции смещается в сторону образования продуктов реакции.
В вторую колбу добавим несколько капель концентрированного раствора роданида калия, увеличивается количество продукта реакции роданида железа. Так же, как и в первой колбе равновесие реакции смещается в сторону образования продуктов реакции.
В третью колбу добавляют один из продуктов реакции – хлорид калия. Наблюдается не потемнение раствора, как в первых двух случаях, а его осветление. Это значит, что концентрации роданида (конечного продукта реакции) уменьшается, а исходных веществ – увеличивается. То есть, добавление в раствор продуктов реакции сдвигает химическое равновесие реакции в сторону образования исходных веществ.
2. При увеличении концентрации исходных веществ равновесие смещается в сторону продуктов реакции. При увеличении продуктов реакции равновесие смещается в сторону исходных веществ.
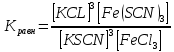
Опыт 2. Влияние изменения температуры на смещение равновесия
Прибор, состоящий из двух шаров, заполнен смесью оксида азота (IV) и его димером. Чистый оксид азота (IV) существует при температуре выше 140 °С. Ниже этой температуры NO2 частично поляризуется по уравнению
2NO2
NO2 – газ бурого цвета, N2O4 – бесцветен. Изменение температуры позволяет судить о смещении равновесия в системе по изменению интенсивности окраски газов.
Один шар прибора опустить в стакан с холодной, а второй – в стакан с горячей водой. Наблюдать изменение интенсивности окраски газов в шарах.
Требования к результатам опыта
1. Нагревание смещает равновесие в сторону эндотермического процесса (окраска усиливается), охлаждение смещает равновесие в сторону экзотермического процесса (окраска стала слабее)
2. При повышении температуры происходит смещение равновесия в сторону реагента 2NO2, то есть реакции, идущей с поглощением тепла. При понижении температуры равновесие смешается в сторону продукта реакции N2O4, идущей с выделением тепла