Добавлен: 09.11.2023
Просмотров: 228
Скачиваний: 11
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Вместе с тем, в зависимости от рН и щелочности, вода с жёсткостью выше 4 мг-экв/л может вызвать в распределительной системе отложение шлаков и накипи (карбоната кальция), особенно при нагревании. Именно поэтому нормами Котлонадзора вводятся очень строгие требования к величине жёсткости воды, используемой для питания котлов (0.05-0.1 мг-экв/л).
К сожалению, далеко не всем известно также о неблагоприятном влиянии жёсткости на здоровье человека при попадании воды на кожу.
Связано это с тем, что при взаимодействии солей жёсткости с моющими веществами (мыло, стиральные порошки, шампуни) может происходить образование нерастворимых "мыльных шлаков" в виде пены. Такая пена после высыхания остается в виде налета на сантехнике, белье, человеческой коже, на волосах (неприятное чувство "жёстких" волос хорошо известное многим). При этом разрушается естественная жировая плёнка, которой всегда покрыты здоровые волосы и нормальная кожа, забиваются поры, появляются сухость, шелушение, перхоть. Первым тревожным признаком такого негативного воздействия является характерный "скрип" чисто вымытой кожи или волос. Оказывается, что вызывающее у некоторых людей раздражение чувство "мылкости" после пользования мягкой водой, является признаком того, что защитная жировая плёнка на коже цела и невредима. Именно она-то и скользит. В противном случае, приходится пользоваться лосьонами, умягчающими и увлажняющими кремами, необходимые для восстановление защиты. Недаром косметологи рекомендуют использовать для умывания очень мягкую дождевую или талую воду..
Вместе с тем, необходимо упомянуть и о другой стороне медали. Мягкая вода с жёсткостью менее 2 мг-экв/л имеет низкую буферную ёмкость (щёлочность) и может, в зависимости от уровня рН и ряда других факторов, оказывать повышенное коррозионное воздействие на водопроводные трубы.
Раздел II. Экспериментальная часть
2.1. Методы проведения эксперимента
2.1.1 Определение карбонатной жесткости.
Методика выполнения работы
Бюретку заполняют раствором серной кислоты. В колбу для титрования вносят 100 мл исследуемой воды, прибавляют к ней 2-3 капли метилового оранжевого и титруют раствором серной кислоты до перехода желтой краски в розовую. Титрование повторяют до получения трех сходящихся результатов, из которых берут средний.
| V(H2O), мл | V(H2SO4), мл | индикатор |
| 100,00 100,00 100,00 | 10,30 10,20 10,30 Vср = 10,26 | метиловый оранжевый |
Расчеты результатов анализа
Карбонатную жесткость рассчитывают по формуле:
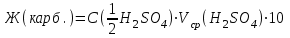
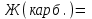 0,1
0,1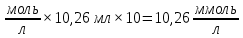
2.1.2. Определение общей жесткости.
Методика выполнения работы
В коническую колбу ёмкостью 250мл бюреткой отмеряют 50мл воды. Отобранную пробу разбавляют дистиллированной водой примерно до объёма 100мл и прибавляют 2 мл аммонийной буферной смеси. На кончике ложечки (20-30мг) отбирают индикатор– эриохром чёрный Т, высыпают его в колбу и перемешивают. Титруют находящуюся в колбе смесь раствором трилона Б до перехода вино-красной окраски раствора в ярко синюю. Перед концом титрования прибавляют раствор трилона Б по одной капле так, чтобы красноватый оттенок окраски совершенно исчез. Замеряют по бюретке объём раствора трилона Б, пошедшего на титрование. Титрование повторяют до получения трёх сходящихся результатов, из которых берут средний.
| V(H2O), мл | V(трилона Б), мл | Индикатор |
| 50,00 50,00 50,00 | 67,60 67,60 67,60 Vср. = 67,60 | Эриохром черный Т |
Расчёты результатов анализа
Общую жесткость воды рассчитывают по следующей формуле:

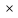 1000
1000Жо(Н2О) =
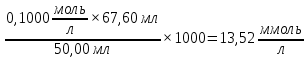
2.2.Обсуждение результатов.
Российские нормативы – СанПиН-ы 2.1.4.1074-01; ГН 2.1.5.1315-03 – определяют норму жёсткости питьевой воды в пределах 7°Ж с установлением нормативного значения для магния – в пределах 50 мг/л и не регламентируя его для кальция.
В России единица измерения содержания солей по данному параметру называется «градус жёсткости» (°Ж)
1° Ж = 20,04 мг Ca2+ или 12,15 Mg2+ в 1 дм3 .
Результаты показили, что вода очень жесткая и привышает все показели. нормы жесткости воды по России не боле 7мг х экв/л
Важно, что с 2014 года по России начал действовать международный стандарт подчета жесткости, который выражаеться (°Ж).
Для оценки жесткости воды, существует множество способов, но я выбрала самый надежный ,
комплексонометрическое титрование трилоном Б, который является самым точным.
Жесткая вода отрицательно влияет на организм человека, и это способствует: заболеванию суставов, снижение моторики желудка, заболевание сердечно сосудистой системы, вымывание кальция из костей , вымывание полезных бактерий и полезных веществ
Следовательно, если мы хотим заботиться о своем здоровье, мы должны больше знать о качестве воды, как жесткость, о способах изменения жесткости воды. В настоящее время ведутся научные разработки, и идет поиск удешевления процесса «смягчения» или увеличения жесткости воды. Но в домашних условиях мы можем и сами немного помочь себе и своему организму.
Заключение
Работа посвящена исследованию воды, я изучала и анализировала значение жёсткости воды, а также ее устранение. Жесткость воды обуславливается наличием растворимых солей магния и кальция, которые при нагревании образовывают осадок (налет), всем известный как накипь. Накипь – это твёрдые отложения, образующиеся на тех поверхностях теплообменных аппаратов, на которых происходит нагревание (кипение, испарение) воды с растворёнными солями жесткости.
При выполнении работы провела анализ определила общую и карбонатную жесткость. Для анализа взяла воду и определила, что вода очень жесткая, (диапазон воды по РФ считается, от 2,00 до 5,50), мои результаты превышают все показатели почти в 2 раза. Что бы эти показатели снизились, необходимо применять определенные методы, которые обуславливают устранения жесткости для начала можно поставить фильтр на кране, а так же существуют различные методы по устранению жесткости. В присутствии воды кальция и магния пагубно влияют на качество воды, которая не пригодная для использования. С точки зрения применения воды для питьевых нужд, её приемлемость по степени жёсткости может существенно варьироваться в зависимости от местных условий, на нашей территории из-за шахт. Порог вкуса для иона кальция в диапазоне 2-6 мг-экв/л, в зависимости от соответствующего аниона, а порог вкуса для магния и того ниже. В некоторых случаях для потребителей приемлема вода с жёсткостью выше 10 мг-экв/л. Высокая жёсткость ухудшает органолептические свойства воды, придавая ей горьковатый вкус.
Также следует отметить, что жесткая вода вредит здоровью человека, высокая жесткость воды:
-
Способствует росту мочевых камней и вследствие развитие болезней, -
При умывании вода сушит кожу, вызывает зуд кожи.
Качественной считается вода, не имеющая вкуса и привкуса. Согласно требованиям ГОСТа 2874-82 и ГСанПиН, интенсивность этих показателей для питьевой водопроводной воды не должна превышать 2 баллов жесткости. При изучении этой темы, я выяснила, что существуют различные виды воды: питьевая вода по ГОСТ 2874; естественная поверхностная и грунтовая вода; техническая вода; морская и засоленная вода; вода после промывки оборудования для приготовления и транспортирования бетонных и растворных смесей; комбинированная вода, представляющая собой смесь воды из двух или более указанных выше источников.
Хочу подвести итог, по всему изученному. Проблема жесткости воды очень актуальная: во-первых это из-за что пресной воды на планете очень мало, во-вторых многие источники загрязнены из-за своего расположения, в-третьих вода не предназначена для питья, только для технического использования и то не всегда. Для начала нужно подготовить воду и потом только использовать, это все из-за того, что на территории Донбасса очень много шахт. Угольная промышленность развита, но не на столько, что бы ни загрязнять природу и в частности подземные воды. Живя на денной территории, каждый человек должен заботиться самостоятельно, какую он пьет воду. Всему живому нужна вода.
Вода-это драгоценный дар природы, который обеспечивает жизнь на Земле живым организмам. Не смотря на то, что пресная вода не вся доступна для человека, мы обязаны экономить запасы воды и использовать по назначению.
Список использованных источников
-
"Лугансквода": на пути к водной независимости /Воронцова Л.// XXI ВЕК : общественно-политич. газ. еженед. Издается с 1996 года. 2015. -
Алексеев В.Н. Количественный анализ./ В. Н. Алексеев – М.: Химия, 1972, С. 16-34-204 с. -
Аналитическая химия промышленных сточных вод. М., 1984. -
Белянин В. Жизнь, молекула воды и золотая пропорция, наука и жизнь/ В.Беляни. – 2004г. - № 10. -
Бердоносов С.С., Химия. Новейший справочник./ С.С.Бердоносо, Е.А.Менделеев. – М.,«Махаон», 2006.‒223 с. -
Васильев В. П. Аналитическая химия. Кн. 1: Титриметрические и гравиметрические методы анализа. – М.: Дрофа, 2005. -
ИПК Издательство стандартов/‒М:, Издательстве на ПЭВМ -
Крешков А.П., Ярославцева А.А. Курс аналитической химии. Количественный анализ. – М.: Химия, 1982. -
Кульский Л.А. Основы химии и технологии воды. – Киев: "Наукова Думка", 1991. - 568 с -
Питьевая вода и здоровье, статья / О.А. Матальгина// Дошкольная педагогика -2010.-№2 С.4-8 -
Посыпайко В.И., Васина Н.А. Аналитическая химия и технический анализ /В.И.Посыпайка. – М.: Высшая школа, 1979. -
Руководство по. химическому анализу поверхностных вод суши, под ред. Л., 1977 -
Т.Х.Чен, Методика определения общей жесткости воды\ Т.Х Чен, Е.Ю.Раткевич, Е.А.Алферова.‒М.: Дрофа, 1998.‒ С 80. -
Чистая вода [Электронный ресурс] / Сайт компании "Чистая вода".Режим доступа:‒ http://www.cwc.ru. ? ,свободный. (Дата обращения 21.04.2019г.)
7>